Données techniques
| Formule | C22H22IN3O3 |
||||||||||||||
| Poids moléculaire | 503.33 | N° CAS | 444912-48-5 | ||||||||||||
| Solubilité (25°C)* | In vitro | DMSO | 100 mg/mL (198.67 mM) | ||||||||||||
| Water | Insoluble | ||||||||||||||
| Ethanol | Insoluble | ||||||||||||||
| In Vivo (Ajoutez les solvants au produit individuellement et dans lordre.) |
|
||||||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||||||
Préparation des solutions mères
Activité biologique
| Description | AM-1241 est un agoniste sélectif du récepteur cannabinoïde CB2 avec un Ki de 3,4 nM, et ce composé présente une sélectivité 82 fois supérieure au récepteur CB1. | ||||
|---|---|---|---|---|---|
| Cibles |
|
||||
| In vitro | AM-1241 est un agoniste protéen du CB2 basé sur les différents effets observés dans divers essais (afflux de calcium, phosphorylation de la kinase régulée par le signal extracellulaire (ERK) et mesure du cAMP) et sur le passage de l'antagonisme neutre à l'agonisme dans l'essai cAMP lorsque la concentration de forskoline est abaissée. Dans les essais de liaison par compétition [3H]CP 55,940, ce composé présente une forte affinité pour le récepteur CB2 humain avec une valeur Ki d'environ 7 nM, tandis que son affinité pour le récepteur CB1 humain est plus de 80 fois plus faible, en utilisant des préparations membranaires de lignées cellulaires HEK et CHO stables exprimant respectivement les récepteurs CB2 et CB1 humains recombinants. | ||||
| In Vivo | AM-1241 inverse de manière dose-dépendante l'hypersensibilité tactile et thermique produite par la ligature des nerfs spinaux L5 et L6 chez les rats. Ce composé est également actif pour bloquer l'hypersensibilité tactile et thermique induite par la ligature des nerfs spinaux chez les souris dépourvues de récepteurs CB1 (souris CB1-/ -), confirmant qu'il inverse l'hypersensibilité sensorielle indépendamment des actions sur les récepteurs CB1. Cette substance chimique (100, 330 μg/kg i.p.) supprime le développement de l'hyperalgésie et de l'allodynie thermiques et mécaniques évoquées par la carragénine. Et cette suppression est bloquée par l'antagoniste CB2 SR144528 mais pas par l'antagoniste CB1 SR141716A. Il produit une antinociception dose-dépendante à un stimulus thermique appliqué à la patte arrière, lorsqu'il est administré dans la patte arrière du côté du test (patte ipsilatérale), tandis qu'il est beaucoup moins actif dans le côté contralatéral. L'A50 (dose analgésique produisant un effet de 50%) de ce composé est de 847 μg/kg, l'effet maximal possible (100% MPE) étant atteint à 3,3 mg/kg. Il produit également une antinociception dose-dépendante lorsqu'il est administré par voie intrapéritonéale (i.p.), avec un A50 de 103 μg/kg. Les actions antinociceptives de cette substance chimique sont bloquées par l'antagoniste sélectif des récepteurs CB2 AM630, mais pas par l'antagoniste sélectif des récepteurs CB1 AM251. Ce composé ne produit pas les effets cannabinoïdes du SNC d'hypothermie, de catalepsie, d'inhibition de l'activité ou d'altération de la déambulation, tandis que cette tétrade d'effets est produite par l'agoniste mixte des récepteurs CB1/CB2 WIN55,212-2. Des injections quotidiennes de cette substance chimique par voie i.p., initiées au début des symptômes, augmentent l'intervalle de survie après l'apparition de la sclérose latérale amyotrophique (SLA) de 56% dans un modèle de souris transgénique de la SLA. |
Protocole (de référence)
| Test kinase :[1] |
|
|---|---|
| Test cellulaire :[2] |
|
| Étude animale :[1] |
|
Références
|
Validation du produit par le client
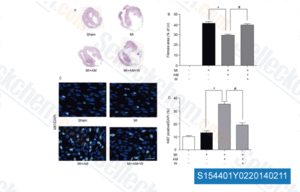
-
Données de [ Sci China Life Sci , 2014 , 57(2), 201-8 ]

-
Données de [ , , Cell Physiol Biochem, 2016, 39(4):1521-36 ]
De Selleck AM1241 A été cité par 18 Publications
| Cannabinoid CB2 receptor controls chronic itch by regulating spinal microglial activation and synaptic transmission [ Cell Rep, 2025, 44(4):115559] | PubMed: 40222011 |
| Cannabinoid Receptors CB1 and CB2 Activation Restores Hippocampal Lipid Profiles and Alleviates Autism-Like Behaviors in Valproic Acid-Induced ASD Rats [ CNS Neurosci Ther, 2025, 31(8):e70591] | PubMed: 40852923 |
| Therapeutic potential of EVs loaded with CB2 receptor agonist in spinal cord injury via the Nrf2/HO-1 pathway [ Redox Rep, 2024, 29(1):2420572] | PubMed: 39466990 |
| CB2R activation ameliorates late adolescent chronic alcohol exposure-induced anxiety-like behaviors during withdrawal by preventing morphological changes and suppressing NLRP3 inflammasome activation in prefrontal cortex microglia in mice [ Brain Behav Immun, 2023, 110:60-79] | PubMed: 36754245 |
| EVs-mediated delivery of CB2 receptor agonist for Alzheimer's disease therapy [ Asian J Pharm Sci, 2023, 18(4):100835] | PubMed: 37645682 |
| Activation of cannabinoid receptor 2 attenuates Angiotensin II-induced atrial fibrillation via a potential NOX/CaMKII mechanism [ Front Cardiovasc Med, 2022, 9:968014] | PubMed: 36312282 |
| Fast-Acting and Receptor-Mediated Regulation of Neuronal Signaling Pathways by Copaiba Essential Oil. [ Int J Mol Sci, 2020, 21(7)] | PubMed: 32218156 |
| The fatty-acid amide hydrolase inhibitor URB597 inhibits MICA/B shedding [ Sci Rep, 2020, 10(1):15556] | PubMed: 32968163 |
| Pharmacological activation of CB2 receptor protects against ethanol-induced myocardial injury related to RIP1/RIP3/MLKL-mediated necroptosis [ Mol Cell Biochem, 2020, 10.1007/s11010-020-03828-1] | PubMed: 32681290 |
| Crocetin Alleviates Inflammation in MPTP-Induced Parkinson's Disease Models through Improving Mitochondrial Functions [ Parkinsons Dis, 2020, 2020:9864370] | PubMed: 33101635 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
