uitsluitend voor onderzoeksdoeleinden
Decitabine DNA Methyltransferase remmer
Cat.Nr.S1200
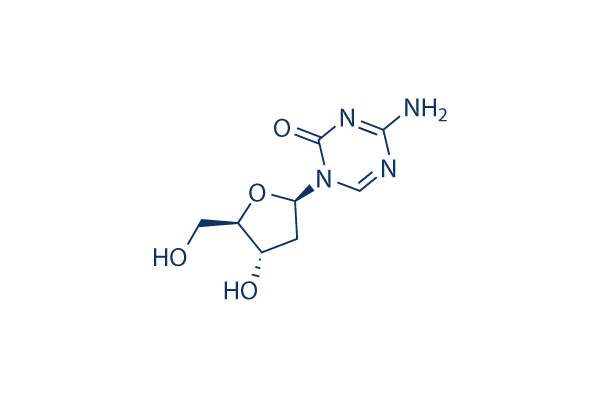
Chemische structuur
Moleculair gewicht: 228.21
Kwaliteitscontrole
| Gerelateerde doelwitten | HDAC JAK BET Histone Methyltransferase PKC PARP HIF PRMT EZH2 AMPK |
|---|---|
| Overige DNA Methyltransferase Inhibitoren | RG108 SGI-1027 Zebularine (NSC 309132) GSK3685032 Gamma-Oryzanol CM272 β-thujaplicin Bobcat339 DC-05 2'-Deoxy-5-Fluorocytidine |
Celkweek, behandeling & werkconcentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| Eca109 | Function Assay | 0.5 μM | 24 h | water | modulates the gene expression of MAGE-A members | 25123082 |
| Eca109 | Growth Inhibition Assay | 0.5/2.5/5 μM | 24/48/72 h | water | inhibits cell growth in both dose- and time- dependent manner | 25123082 |
| Eca109 | Function Assay | 0.5 μM | 6/12/24 h | water | inhibits cell migration | 25123082 |
| Eca109 | Function Assay | 0.5 μM | 24 h | water | inhibits cell invasion | 25123082 |
| Eca109 | Growth Inhibition Assay | 0.5 μM | 24 h | water | induces G2/M arrest in the cell cycle | 25123082 |
| Eca109 | Function Assay | 0.5/1 μM | 24 h | water | decreases expression of NF-κB2 and MMP2 | 25123082 |
| SW1116 | Growth Inhibition Assay | 0.5/1/2/5 μM | 48 h | DMSO | enhances the Gefitinib induced cell inhibition | 24874286 |
| LOVO | Growth Inhibition Assay | 0.5/1/2/5 μM | 48 h | DMSO | enhances the Gefitinib induced cell inhibition | 24874286 |
| SW1116 | Function Assay | 10 μM | 48 h | DMSO | increases the effective at inhibiting AKT and mTOR signaling pathways combined with gefitinib | 24874286 |
| LOVO | Function Assay | 10 μM | 48 h | DMSO | increases the effective at inhibiting AKT and mTOR signaling pathways combined with gefitinib | 24874286 |
| SW1116 | Apoptosis Assay | 10 μM | 48 h | DMSO | enhances Gefitinib-induced apoptosis | 24874286 |
| LOVO | Apoptosis Assay | 10 μM | 48 h | DMSO | enhances Gefitinib-induced apoptosis | 24874286 |
| RPMI-8226 | Apoptosis Assay | 1/2 μM | 48/72/96 h | DMSO | induces cell apoptosis | 24833108 |
| OPM-2 | Apoptosis Assay | 1/2 μM | 72/96/120 h | DMSO | induces cell apoptosis | 24833108 |
| JJN3 | Apoptosis Assay | 0.5/1 μM | 24/48 h | DMSO | induces cell apoptosis | 24833108 |
| NCI-H929 | Apoptosis Assay | 1/2 μM | 72/96/120 h | DMSO | induces cell apoptosis | 24833108 |
| RPMI-8226 | Growth Inhibition Assay | 1/2 μM | 24/48/72 h | DMSO | affects cell cycle progression negatively | 24833108 |
| OPM-2 | Growth Inhibition Assay | 1/2 μM | 24/48/72 h | DMSO | affects cell cycle progression negatively | 24833108 |
| JJN3 | Growth Inhibition Assay | 0.5/1 μM | 24/48/72 h | DMSO | affects cell cycle progression negatively | 24833108 |
| NCI-H929 | Growth Inhibition Assay | 1/2 μM | 24/48/72 h | DMSO | affects cell cycle progression negatively | 24833108 |
| HeLa | Kinase Assay | Ki=1000–5000 μM for hENT1 | 24780098 | |||
| HeLa | Kinase Assay | Ki=5.6 ± 0.5 μM for hENT2 | 24780098 | |||
| HeLa | Kinase Assay | Ki=21.6 ± 3.0 μM for hCNT1 | 24780098 | |||
| HeLa | Kinase Assay | Ki=14.4 ± 4.6 μM for hCNT3 | 24780098 | |||
| NB4 | Function Assay | 2.5/5/7.5/10 μM | 24 h | DMSO | increasea the expression of precursor miR-125a | 24484870 |
| CD4+ CD25− T | Function Assay | 1/5 μM | reduceS global DNA methylation | 24476360 | ||
| BV-173 | Apoptosis Assay | 0.25/0.5/0.75/1 μM | 48/72/96 h | PBS | induces cell apoptosis in both dose- and time- dependent manner | 24423613 |
| ML-1 | Apoptosis Assay | 0.25/0.5/0.75/1 μM | 48/72/96 h | PBS | induces cell apoptosis in both dose- and time- dependent manner | 24423613 |
| HL-60 | Apoptosis Assay | 0.25/0.5/0.75/1 μM | 48/72/96 h | PBS | induces cell apoptosis in both dose- and time- dependent manner | 24423613 |
| KG-1a | Apoptosis Assay | 0.25/0.5/0.75/1 μM | 48/72/96 h | PBS | induces cell apoptosis in both dose- and time- dependent manner | 24423613 |
| BV-173 | Function Assay | 250/500nM | 48 h | PBS | induces delayed and sustained ROS increase | 24423613 |
| CEM | Function Assay | 250/500nM | 48 h | PBS | induces delayed and sustained ROS increase | 24423613 |
| HL-60 | Function Assay | 250/500nM | 48 h | PBS | induces delayed and sustained ROS increase | 24423613 |
| ML-1 | Function Assay | 250/500nM | 48 h | PBS | induces delayed and sustained ROS increase | 24423613 |
| DLD-1 | Function Assay | 250/500nM | 48 h | PBS | do not induces delayed and sustained ROS increase | 24423613 |
| HCT-116 | Function Assay | 250/500nM | 48 h | PBS | do not induces delayed and sustained ROS increase | 24423613 |
| U937-A/E-9/14/18 | Apoptosis Assay | 0.01/0.1/1/10 μM | 48 h | induces cell apoptosis in a dose-dependent manner | 24300456 | |
| HT29 | Growth Inhibition Assay | 72 h | IC50=1400±179 μM | 24172061 | ||
| SW48 | Growth Inhibition Assay | 72 h | IC50=15.2±6.2 μM | 24172061 | ||
| HCT116 | Growth Inhibition Assay | 72 h | IC50=1.7±0.4 μM | 24172061 | ||
| HepG2 | Function Assay | 0.5/1 μM | 24 h | DMSO | up-regulated the relative OCTN2 mRNA and protein expression | 24146874 |
| LS174T | Function Assay | 0.5/1 μM | 24 h | DMSO | lead to an increase of OCTN2 levels | 24146874 |
| HepG2 | Apoptosis Assay | 1/10/100 μM | 7 d | DMSO | induces cell apoptosis in a dose-dependent manner | 24146874 |
| LS174T | Apoptosis Assay | 1/10/100 μM | 7 d | DMSO | induces cell apoptosis in a dose-dependent manner | 24146874 |
| QBC-939 | Apoptosis Assay | 1/10/100 μM | 7 d | DMSO | induces cell apoptosis in a dose-dependent manner | 24146874 |
| U251 | Apoptosis Assay | 1/10/100 μM | 7 d | DMSO | induces cell apoptosis in a dose-dependent manner | 24146874 |
| HL-60 | Growth Inhibition Assay | 1 μM | 48 h | increases G2-phase cell fraction | 24000324 | |
| MDA‑MB‑453 | Function Assay | 0.2/1 μM | 72 h | causes re-expression of claudin 1 | 23844228 | |
| HCC1569 | Function Assay | 0.2/1 μM | 72 h | causes re-expression of claudin 1 | 23844228 | |
| BT‑474 | Function Assay | 0.2/1 μM | 72 h | causes re-expression of claudin 1 | 23844228 | |
| AGS | Apoptosis Assay | 5/10/20/50 μM | 48 h | DMSO | inhibits the cell viability | 23582784 |
| A549 | Apoptosis Assay | 5/10/20/50 μM | 48 h | DMSO | inhibits the cell viability | 23582784 |
| AGS | Growth Inhibition Assay | 5/10/20/50 μM | 48 h | DMSO | induces G2/M phase arrest | 23582784 |
| Kasumi-1 | Apoptosis Assay | 0.5 μM | 48 h | decreases the cell viability co-treated with Tf-NP-sc | 23493348 | |
| OCI-AML3 | Apoptosis Assay | 2.5 μM | 48 h | decreases the cell viability co-treated with Tf-NP-sc | 23493348 | |
| MV4-11 | Apoptosis Assay | 2.5 μM | 48 h | decreases the cell viability co-treated with Tf-NP-sc | 23493348 | |
| NK | Cytotoxity Assay | 0.02-20 μM | 5 d | decreases the cytolytic activity of NK cells at intermediate concentrations resulting in a U-shaped dose–response curve | 23328088 | |
| NK | Apoptosis Assay | 0.02-20 μM | 5 d | decrease NK cell proliferation and viability as the concentration increased | 23328088 | |
| NK | Function Assay | 0.01-20 μM | 5 d | causes hypomethylation of NK cells in a dose–response | 23328088 | |
| MOLT4/DNR | Function Assay | 5 μM | 4 d | reduces ABCB1 mRNA expression | 23060570 | |
| Jurkat/DOX | Function Assay | 5 μM | 4 d | reduces ABCB1 mRNA expression | 23060570 | |
| MOLT4/DNR | Growth Inhibition Assay | 5 μM | 4 d | reduces the IC50 value for daunorubicin sensitivity | 23060570 | |
| Jurkat/DOX | Growth Inhibition Assay | 5 μM | 4 d | reduces the IC50 value for daunorubicin sensitivity | 23060570 | |
| ccRCC | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | has minimal effect on cell proliferation | 22826467 |
| TNBC | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | has minimal effect on cell proliferation | 22826467 |
| A498 | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | induces synergistic responses with romidepsin | 22826467 |
| KIJ265T | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | induces synergistic responses with romidepsin | 22826467 |
| MDA-231 | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | induces synergistic responses with romidepsin | 22826467 |
| BT-20 | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | induces synergistic responses with romidepsin | 22826467 |
| U937 | Growth Inhibition Assay | 5-20 μM | 24/48/72 h | induces a decrease in cell viability in a concentration- and time-dependent manner | 22767021 | |
| HL60 | Growth Inhibition Assay | 5-20 μM | 24/48/72 h | induces a decrease in cell viability in a concentration- and time-dependent manner | 22767021 | |
| U937 | Apoptosis Assay | 15 μM | 24/48/72 h | induces cell apoptosis | 22767021 | |
| HL60 | Apoptosis Assay | 15 μM | 24/48/72 h | induces cell apoptosis | 22767021 | |
| LS411N | Apoptosis Assay | 0.5 μM | 72 h | increases Fas mRNA level | 22461695 | |
| MDA-MB-231 | Apoptosis Assay | 10 μM | 48 h | reduces cell viability in a dose-dependent manner | 21887697 | |
| MCF-7 | Apoptosis Assay | 10 μM | 48 h | reduces cell viability in a dose-dependent manner | 21887697 | |
| A375 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| SKMEL1 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| SKMEL3 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| SKMEL28 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| MeWo | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| B16 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| Ly 1 | Growth Inhibition Assay | 24 h | IC50=7.3 μM | 21772049 | ||
| Ly 7 | Growth Inhibition Assay | 24 h | IC50=10.7 μM | 21772049 | ||
| Su-DHL6 | Growth Inhibition Assay | 24 h | IC50>20 μM | 21772049 | ||
| Ly 10 | Growth Inhibition Assay | 24 h | IC50>20 μM | 21772049 | ||
| RIVA | Growth Inhibition Assay | 24 h | IC50>20 μM | 21772049 | ||
| Su-DHL2 | Growth Inhibition Assay | 24 h | IC50>20 μM | 21772049 | ||
| Ly 1 | Growth Inhibition Assay | 48 h | IC50=0.34 μM | 21772049 | ||
| Ly 7 | Growth Inhibition Assay | 48 h | IC50=0.025 μM | 21772049 | ||
| Su-DHL6 | Growth Inhibition Assay | 48 h | IC50>20 μM | 21772049 | ||
| Ly 10 | Growth Inhibition Assay | 48 h | IC50=1.8 μM | 21772049 | ||
| RIVA | Growth Inhibition Assay | 48 h | IC50>20 μM | 21772049 | ||
| Su-DHL2 | Growth Inhibition Assay | 48 h | IC50=17.4 μM | 21772049 | ||
| Ly 1 | Growth Inhibition Assay | 72 h | IC50=0.01 μM | 21772049 | ||
| Ly 7 | Growth Inhibition Assay | 72 h | IC50=0.018 μM | 21772049 | ||
| Su-DHL6 | Growth Inhibition Assay | 72 h | IC50=1.6 μM | 21772049 | ||
| Ly 10 | Growth Inhibition Assay | 72 h | IC50=1.2 μM | 21772049 | ||
| RIVA | Growth Inhibition Assay | 72 h | IC50>20 μM | 21772049 | ||
| Su-DHL2 | Growth Inhibition Assay | 72 h | IC50=11.2 μM | 21772049 | ||
| U373-MAGI | Antiviral assay | 0.25 to 8 uM | 2 to 72 hrs | Antiviral activity against VSV-G pseudotyped HIV-1 NL4-3 infected in human U373-MAGI cells assessed as reduction in U5-gag level at 0.25 to 8 uM after 2 to 72 hrs by qPCR method | 27117260 | |
| U373-MAGI | Antiviral assay | 0.25 to 8 uM | 2 to 72 hrs | Antiviral activity against VSV-G pseudotyped HIV-1 NL4-3 infected in human U373-MAGI cells assessed as reduction in gag level at 0.25 to 8 uM after 2 to 72 hrs by qPCR method | 27117260 | |
| Klik om meer experimentele gegevens over de cellijn te bekijken | ||||||
Chemische informatie, Opslag en Stabiliteit
| Moleculair gewicht | 228.21 | Formule | C8H12N4O4 |
Opslag (Vanaf de ontvangstdatum) | |
|---|---|---|---|---|---|
| CAS-nr. | 2353-33-5 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | Deoxycytidine, 5-aza-2'-deoxycytidine, 5-AZA-dC, 5-aza-CdR,NSC 127716 | Smiles | C1C(C(OC1N2C=NC(=NC2=O)N)CO)O | ||
Oplosbaarheid
|
In vitro |
DMSO
: 45 mg/mL
(197.18 mM)
Water : 22.5 mg/mL Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo Formuleringscalculator (Heldere oplossing)
Stap 1: Voer de onderstaande informatie in (Aanbevolen: Een extra dier voor het geval van verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in het gedeelte Oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-mastervloeistof: mg geneesmiddel vooraf opgelost in μL DMSO ( Concentratie mastervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de partij geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toeμL PEG300, mengen en helder maken, voeg vervolgens toeμL Tween 80, mengen en helder maken, voeg vervolgens toe μL ddH2O, mengen en helder maken.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toe μL Maïsolie, mengen en helder maken.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysische methoden zoals vortexen, echografie of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
DNA methylation
(HL-60, KG1a cells) |
|---|---|
| In vitro |
Decitabine remt de celgroei op een dosis- en tijdsafhankelijke manier met een IC50 van ongeveer 438 nM en 43,8 nM voor een blootstelling van respectievelijk 72 uur en 96 uur in HL-60 en KG1a leukemische cellen. Een recente studie toont aan dat deze verbinding een hoge anti-proliferatieve en pro-apoptotische activiteit vertoont tegen anaplastisch grootcellig lymfoom (ALCL), en de [3H]–thymidine-opname in KARPAS-299 cellen remt met een EC50 van 0,49 μM. |
| Kinase Assay |
DNA-synthese assay
|
|
De snelheid van DNA-synthese wordt gemeten door de incorporatie van radioactief thymidine in DNA. HL-60 en KG1a cellen worden gesuspendeerd in 2 mL RPMI medium dat 10% foetaal serum bevat in 6-wells (35 mm diameter) schaaltjes en geïncubeerd met verschillende concentraties van de overeenkomstige geneesmiddelen gedurende 48 uur (geneesmiddelen worden gelijktijdig toegevoegd). Na 48 uur wordt 0,5 μCi [3H] thymidine (6,7 Ci/mmol) aan elke put toegevoegd en nog eens 24 uur geïncubeerd. De cellen worden op GF/C glasvezelfilters (2,4 cm diameter) geplaatst, gewassen met koud 0,9% NaCl, 5% koud trichloorazijnzuur en ethanol. De filters die het DNA bevatten, worden vervolgens gedroogd, in EcoLite scintillatievloeistof (ICN) geplaatst en de radioactiviteit wordt gemeten met een Beckman LS 6000IC scintillatieteller. De IC50 wordt gedefinieerd als de concentratie van het geneesmiddel die 50% van de DNA-synthese van de leukemische cellijnen remt, afgeleid van de dosis-respons curve.
|
|
| In vivo |
In een ALK+ KARPAS-299 muis-xenograftmodel veroorzaakt Decitabine in een dosis van 2,5 mg/kg een verhoogde apoptose en verminderde proliferatie van tumorcellen, en resulteert het ook in demethylatie van tumorsuppressor p16INK4A. |
Referenties |
|
Toepassingen
| Methoden | Biomarkers | Afbeeldingen | PMID |
|---|---|---|---|
| Western blot | Survivin / Bcl-2 / p53 / c-Myc / DNMT1 p-AKT / AKT / p-GSK3β / GSK3β / p-Myc / Myc / p-P70 / P70 / p-4EBP-1 / 4EBP-1 / PTEN phospho-p38 / p38 / phospho-NFκB / NFκB p-JAK1 / JAK1 / p-JAK2 / JAK2 / p-STAT3 / STAT3 E-cadherin / N-cadherin / Snail / MMP-2 / MMP-9 / Bcl-2 / Bax |
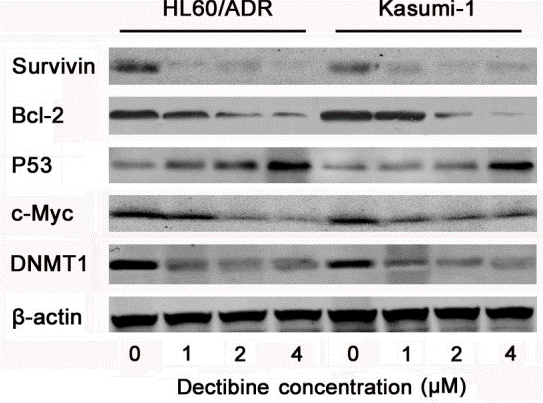
|
26384351 |
| Immunofluorescence | DNMT1 E-cadherin / MMP-9 |
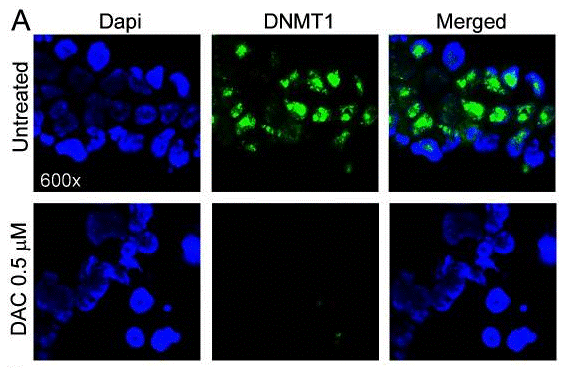
|
21303982 |
| Growth inhibition assay | Cell viability |
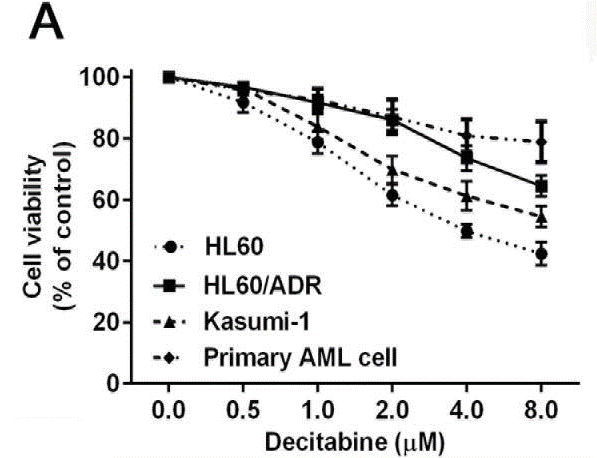
|
26384351 |
Informatie klinische proef
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Rekrutering | Aandoeningen | Sponsor/Medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT06291285 | Not yet recruiting | Healthy Volunteers |
Novo Nordisk A/S |
February 27 2024 | Phase 1 |
| NCT05960773 | Recruiting | Mesothelioma|Malignant Mesothelioma (MM)|Early-stage Mesothelioma|Subclinical Mesothelioma|BRCA1-Associated Protein-1 (BAP1) Mutations|Early-stage BAP1-associated Malignancies |
National Cancer Institute (NCI)|National Institutes of Health Clinical Center (CC) |
January 31 2024 | Phase 2 |
| NCT05835011 | Terminated | Myelodysplastic Syndromes |
Astex Pharmaceuticals Inc. |
July 14 2023 | Phase 2 |
| NCT05816356 | Recruiting | Healthy |
EpiDestiny Inc.|Worldwide Clinical Trials |
March 24 2023 | Phase 1 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, kunt u een bericht achterlaten.
Veelgestelde vragen
Vraag 1:
Is it a racemic mixture or a monomer?
Antwoord:
Its S1200 is R form.
