Technische Daten
| Formel | C17H19FN4O2S |
||||||
| Molekulargewicht | 362.42 | CAS-Nr. | 860352-01-8 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 73 mg/mL (201.42 mM) | ||||
| Ethanol | 5 mg/mL (13.79 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | AZD7762 ist ein potenter und selektiver Inhibitor von Chk1 mit einem IC50 von 5 nM in einem zellfreien Assay. Es ist gleichermaßen potent gegen Chk2 und weniger potent gegen CAM, Yes, Fyn, Lyn, Hck und Lck. Phase 1. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | AZD7762, ein selektiverer Chk1-Inhibitor, hemmt die Chk1-Phosphorylierung eines cdc25C-Peptids durch reversible Bindung an die ATP-Bindungsstelle von Chk1, mit einem IC50 von 5 nM und einem Ki von 3,6 nM. Diese Verbindung induziert einen Zellstopp mit einem EC50 von 0,620 μM und hebt den durch Camptothecin induzierten G2-Arrest mit einem EC50 von 10 nM signifikant auf, indem sie den Chk1-abhängigen Abbau von Cdc25A und die Aktivierung von Cyclin A blockiert. Es (300 nM) verstärkt die Antitumorwirksamkeit gegen SW620 und gegen MDA-MB-231 durch Reduzierung der GI50-Werte von 24,1 nM und 2,25 μM auf 1,08 nM bzw. 0,15 μM. Diese Chemikalie zeigt Zytotoxizität gegen eine Vielzahl von Neuroblastom-Zelllinien, die p53 Wildtyp, p53-Mutation, Mdm2-Amplifikation oder p14-Deletion aufweisen, mit IC50-Werten im Bereich von 82,6-505,9 nM. |
||||
| In vivo | AZD7762 allein bei 25 mg/kg zeigt wenig Antitumoraktivität in H460-DNp53-Xenograft-Mäusen und SW620-Xenograft-Mäusen, aber bei kombinierter Verabreichung zeigt diese Verbindung eine signifikante Antitumorwirksamkeit in den beiden Xenograft-Mäusen mit einem Log-Zelltod von 0,9 oder einem prozentualen behandelten/Kontroll-Verhältnis (%T/C) von 26 sogar bei niedriger Dosis von 12,5 mg. Die Dosis dieser Chemikalie in Kombination bei H460-DNp53-Xenograft-Ratten hemmt das Tumorvolumen dosisabhängig mit %T/C-Werten von 48 und 32 für 10 bzw. 20 mg/kg. Diese Verbindung (25 mg/kg) in Kombination führt zu einer vollständigen Tumorregression bei den SW620-Xenograft-Mäusen, wobei das %T/C signifikant auf -66% bzw. -67% ansteigt. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
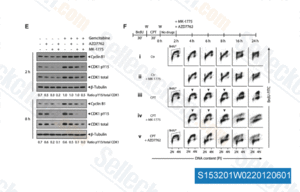
-
Daten von [ Cancer Discov , 2012 , 2, 524-39 ]
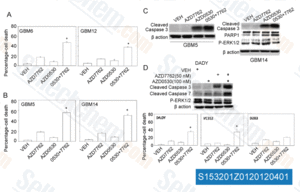
-
Daten von [ Cancer Biol Ther , 2012 , 13 ]
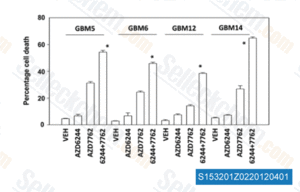
-
Daten von [ Cancer Biol Ther , 2012 , 13 ]
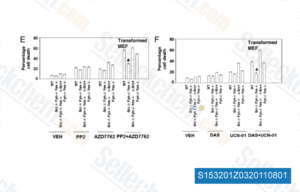
-
Daten von [ Cancer Biol Ther , 2011 , 12, 215-28 ]
Sellecks AZD7762 Wurde zitiert von 136 Publikationen
| ATR promotes mTORC1 activity via de novo cholesterol synthesis [ EMBO Rep, 2025, 26(14):3574-3593] | PubMed: 40514450 |
| Quantitative Chromatin Protein Dynamics During Replication Origin Firing in Human Cells [ Mol Cell Proteomics, 2025, 24(3):100915] | PubMed: 39880081 |
| Efficacy of NAMPT inhibition in T-cell acute lymphoblastic leukemia [ PLoS One, 2025, 20(6):e0324443] | PubMed: 40526635 |
| Dual Disruption of DNA Repair by a Novel CHK2 Inhibitor, ART-446, and Olaparib is a Promising Strategy for Triple-Negative Breast Cancer Therapy [ Biomol Ther (Seoul), 2025, 33(3):458-469] | PubMed: 40195731 |
| The MYCN oncoprotein is an RNA-binding accessory factor of the nuclear exosome targeting complex [ Mol Cell, 2024, S1097-2765(24)00285-5] | PubMed: 38703770 |
| Natural pentacyclic triterpenoid from Pristimerin sensitizes p53-deficient tumor to PARP inhibitor by ubiquitination of Chk1 [ Pharmacol Res, 2024, 201:107091] | PubMed: 38316371 |
| ELK3 destabilization by speckle-type POZ protein suppresses prostate cancer progression and docetaxel resistance [ Cell Death Dis, 2024, 15(4):274] | PubMed: 38632244 |
| Loss of POLE3-POLE4 unleashes replicative gap accumulation upon treatment with PARP inhibitors [ Cell Rep, 2024, 43(5):114205] | PubMed: 38753485 |
| Crispr-mediated genome editing reveals a preponderance of non-oncogene addictions as targetable vulnerabilities in pleural mesothelioma [ Lung Cancer, 2024, 197:107986] | PubMed: 39383772 |
| Multiplex single-cell chemical genomics reveals the kinase dependence of the response to targeted therapy [ Cell Genom, 2024, 4(2):100487] | PubMed: 38278156 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
