Technische Daten
| Formel | C17H14ClF2IN2O2 |
||||||||||
| Molekulargewicht | 478.67 | CAS-Nr. | 212631-79-3 | ||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 96 mg/mL (200.55 mM) | ||||||||
| Ethanol | 14 mg/mL (29.24 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | PD184352 (CI-1040) ist ein ATP-nicht-kompetitiver MEK1/2-Inhibitor mit einer IC50 von 17 nM in zellbasierten Assays, 100-fach selektiver für MEK1/2 als für MEK5. Diese Verbindung induziert selektiv apoptosis. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | CI-1040-Behandlung führt zu einer Reduktion der pMAPK-Spiegel in mehreren Tumorzellen, einschließlich Kolon-26-, BX-PC3-Pankreas-, A431-Zervix-, HT-29-Kolon-, ZR-25-1-Brust- und SKOV-3-Ovarialkarzinomen. Die Behandlung mit dieser Verbindung hemmt nicht die Phosphorylierung von Jun-Kinase, p38-Kinase oder Akt, was darauf hindeutet, dass sie spezifisch MEK angreift. Die Hemmung der MAPK-Aktivierung durch diese Chemikalie verhindert den Zellzyklusfortschritt und induziert einen G1-Block. Die IC50 für die Hemmung von MEK1 durch diesen Inhibitor beträgt 0,3 μM, 15-mal höher als die Konzentration, die zur Hemmung der EGF-induzierten Aktivierung von ERK2 in Swiss 3T3-Zellen erforderlich ist. Diese Ergebnisse zeigen, dass dieser Wirkstoff seine Wirkung auf Zellen ausübt, indem er die Aktivierung von MKK1 unterdrückt und nicht, indem er deren Aktivität blockiert. 2 nM dieser Verbindung hemmt die Aktivierung von MKK1 in Swiss 3T3-Zellen um 50%, während eine über 100-fache Konzentration davon MEK1 in vitro hemmt. Es hemmt auch die Raf-katalysierte Phosphorylierung von MEK1 ohne Einfluss auf die Raf-katalysierte Phosphorylierung von Myelin-Basismembran-Protein. Diese Chemikalie hemmt 86% des Wachstums von papillären Schilddrüsenkarzinom (PTC)-Zellen mit der RET/PTC1-Rearrangement bei 10 μM im Vergleich zu Zellen, die nur mit DMSO behandelt wurden. Sie zeigt eine starke Hemmung von PTC-Zellen (BRAF-Mutation) mit einem GI50 von 52 nM, aber eine geringe Aktivität bei RET/PTC1-Rearrangement-Typ mit einem GI50 von 1,1 μM. Eine aktuelle Untersuchung zeigt, dass dieser Wirkstoff die apoptotische Wirkung von BMS-214662 in einer CML-Blastenkrisen-Zelllinie, K562, und in primären chronischen Phase CD34+ CML-Zellen verstärkt. | ||||
| In vivo | Die orale Verabreichung von CI-1040 beeinträchtigt das Wachstum von Kolontumor-Xenotransplantaten von Maus und Mensch in einem breiten Dosisbereich von 48-200 mg/kg pro Dosis, jedoch nicht bei P388-Leukämie. Diese Verbindung hemmt die Tumorxenotransplantate von PTC-Zellen, die eine BRAF-Mutation tragen, mit einer Reduktion von 31,3% und von Zellen, die die RET/PTC1-Rearrangement tragen, mit einer Reduktion von 47,5% im Vergleich zu unbehandelten (Vehikel-)Mäusen nach 3 Wochen oraler Verabreichung (300 mg/kg/Tag). Es wurden keine toxischen Wirkungen bei Mäusen beobachtet, die mit dieser Chemikalie behandelt wurden. Eine vorübergehende Exposition von Mammakarzinomen gegenüber dieser Verbindung und UCN-01 führt zu Tumorzelltod in vivo und einer verlängerten Unterdrückung des Tumorwachstums. Die kombinierte Behandlung mit dieser Chemikalie (25 mg/kg) und UCN-01 (0,1-0,2 mg/kg) reduziert MDA-MB-231 signifikant und beseitigt weitgehend das MCF7-Tumorwachstum bei implantierten athymischen Mäusen, während jede Einzelbehandlung keine signifikante Aktivität aufweist. Die Medikamentenkombination führt zu einem tiefgreifenden Tumorzelltod, der mit einer Reduktion der Phosphorylierung von ERK1/2 und der Immunreaktivität von Ki67 und CD31 korreliert. | ||||
| Merkmale | Erster MEK-Inhibitor, der in die klinische Entwicklung ging. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung

-
Daten von [ J Natl Cancer Inst , 2012 , 104(21), 1673-9 ]

-
Daten von [ J Natl Cancer Inst , 2012 , 104(21), 1673-9 ]

-
Daten von [ Science , 2011 , 331, 912-916 ]
-
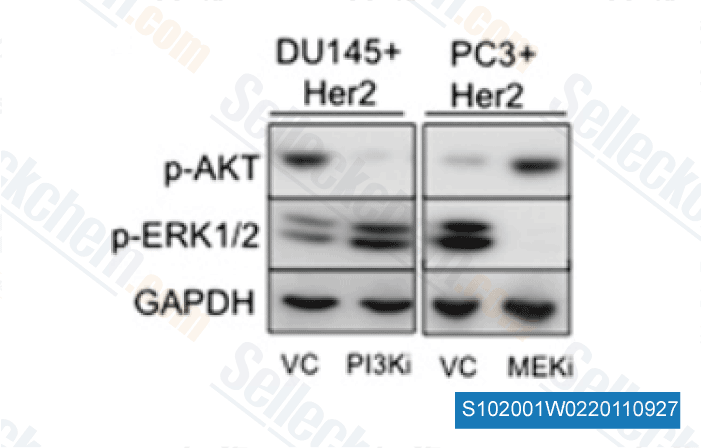
Daten von [ Proc Natl Acad Sci U S A , 2011 , 108, 16392-7 ]
Sellecks PD184352 (CI-1040) Wurde zitiert von 144 Publikationen
| Transcriptional repressor Capicua is a gatekeeper of cell-intrinsic interferon responses [ Cell Host Microbe, 2025, 33(4):512-528.e7] | PubMed: 40132591 |
| Establishing Bovine Embryonic Stem Cells and Dissecting Their Self-Renewal Mechanisms [ Int J Mol Sci, 2025, 26(8)3536] | PubMed: 40331984 |
| Keratinocyte-derived VEGF-A is an essential pro-migratory autocrine mediator, acting through the KDR/GEF-H1/RhoA pathway [ Front Cell Dev Biol, 2025, 13:1601887] | PubMed: 40746859 |
| Inhibition of Retinoic Acid Receptor Gamma Improves Bovine Embryo Development [ Vet Sci, 2025, 12(10)924] | PubMed: 41150070 |
| GRB2 stabilizes RAD51 at reversed replication forks suppressing genomic instability and innate immunity against cancer [ Nat Commun, 2024, 15(1):2132] | PubMed: 38459011 |
| eIF4F controls ERK MAPK signaling in melanomas with BRAF and NRAS mutations [ Proc Natl Acad Sci U S A, 2024, 121(44):e2321305121] | PubMed: 39436655 |
| Dietary protein restriction regulates skeletal muscle fiber metabolic characteristics associated with the FGF21-ERK1/2 pathway [ iScience, 2024, 27(3):109249] | PubMed: 38450157 |
| MEK1/2 inhibition decreases pro-inflammatory responses in macrophages from people with cystic fibrosis and mitigates severity of illness in experimental murine methicillin-resistant Staphylococcus aureus infection [ Front Cell Infect Microbiol, 2024, 14:1275940] | PubMed: 38352056 |
| Forchlorfenuron-Induced Mitochondrial Respiration Inhibition and Metabolic Shifts in Endometrial Cancer [ Cancers (Basel), 2024, 16(5)976] | PubMed: 38473335 |
| The NF-κB-HE4 axis: A novel regulator of HE4 secretion in ovarian cancer [ PLoS One, 2024, 19(12):e0314564] | PubMed: 39621651 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
