Technische Daten
| Formel | C20H16N2O4 |
||||||
| Molekulargewicht | 348.35 | CAS-Nr. | 7689-03-4 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 4 mg/mL (11.48 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Camptothecin (CPT) ist ein spezifischer Inhibitor der DNA Topoisomerase I (Topo I) mit einem IC50-Wert von 0,68 μM in einem zellfreien Assay. Camptothecin induziert Apoptosis in Krebszellen über microRNA-125b-vermittelte mitochondriale Signalwege. Phase 2. | ||
|---|---|---|---|
| Ziele |
|
||
| In vitro | Camptothecin (CPT), ein Pflanzenalkaloid, das ursprünglich 1966 aus *Camptotheca acuminate* isoliert wurde, ist dafür bekannt, Zellen während der S-Phase der Mitose anzuhalten. Diese Verbindung zeigt eine nanomolare Potenz in der Zytotoxizität gegen viele menschliche Tumorzelllinien, einschließlich HT29, LOX, SKOV3 und SKVLB, mit IC50-Werten von 37 nM bis 48 nM. In Kombination mit TNF induziert es Apoptosis in primären Maushepatozyten mit einem IC50-Wert von 13 μM. Es abrogierte auch die TNF-induzierte NF-κB-Aktivierung sowie die Expression des TNF-Rezeptor-assoziierten Faktors 2 (TRAF2), des X-chromosomalen Inhibitors des Apoptosis-Proteins (X-IAP) und des FLICE-inhibitorischen Proteins (FLIP). In HCT116-Zellen induziert CPT (5 μM) den Proteasom-vermittelten Abbau des Mixed Lineage Leukemia 5 (MLL5)-Proteins, was zur Phosphorylierung von p53 an Ser392 führt. Aufgrund seiner geringen Löslichkeit und unerwünschten Wirkungen wurden verschiedene Analoga entwickelt, und zwei davon, Topotecan und Irinotecan, wurden von der FDA zugelassen und werden in der Krebschemotherapie eingesetzt. | ||
| In vivo | Camptothecin (CPT) (8 mg/kg) zeigt eine vollständige Wachstumshemmung und Regression in Maus-Xenotransplantaten verschiedener Tumoren, einschließlich Kolon-, Lungen-, Brust-, Magen- und Ovarialtumoren. Bei Mäusen induzieren Kombinationen dieser Verbindung (50 mg/kg) und TNF (5 und 7 μg/kg), aber nicht sie allein, Leberschäden. |
Protokoll (aus Referenz)
| Kinase-Assay:[2] |
|
|---|---|
| Zell-Assay:[2] |
|
| Tierstudie:[3] |
|
Referenzen
|
Kundenproduktvalidierung
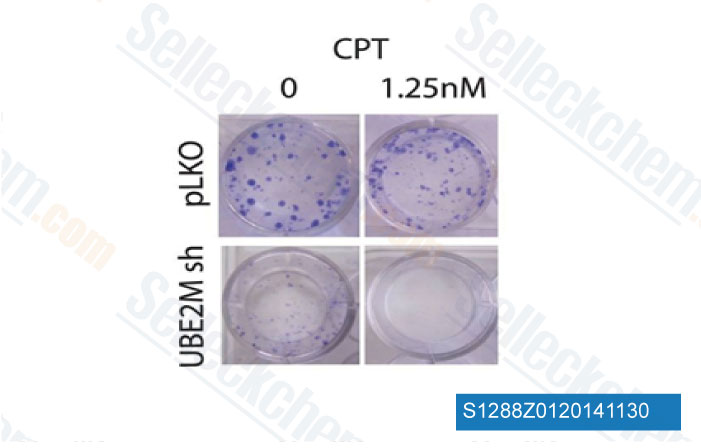
-
Daten von [ PLoS One , 2014 , 9(7), e101844 ]
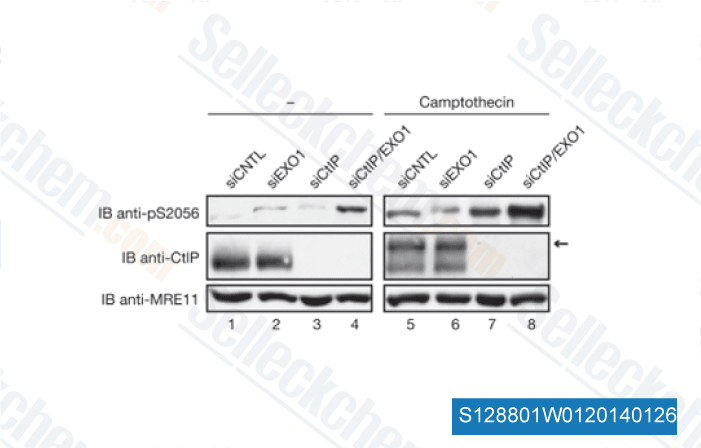
-
Daten von [ EMBO Rep , 2010 , 11(12), 962-8 ]
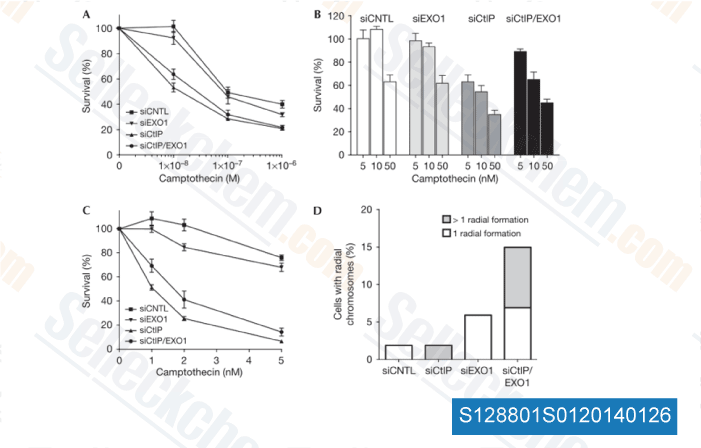
-
Daten von [ EMBO Rep , 2010 , 11(12), 962-8 ]
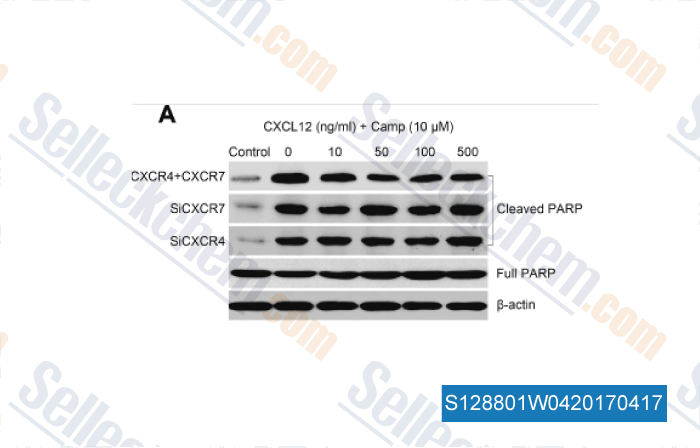
-
Daten von [ , , Tumour Biol, 2016, 37(6):8169-79 ]
Sellecks Camptothecin (CPT) Wurde zitiert von 164 Publikationen
| Non-canonical functions of DNMT3A in hematopoietic stem cells regulate telomerase activity and genome integrity [ Cell Stem Cell, 2025, S1934-5909(25)00256-5] | PubMed: 40680747 |
| Inherited deficiency of DIAPH1 identifies a DNA double strand break repair pathway regulated by γ-actin [ Nat Commun, 2025, 16(1):4491] | PubMed: 40368919 |
| A novel biosensor for the spatiotemporal analysis of STING activation during innate immune responses to dsDNA [ EMBO J, 2025, 10.1038/s44318-025-00370-y] | PubMed: 39984755 |
| DSCC1 restrains 53BP1/RIF1 signaling at DNA double-strand breaks to promote homologous recombination repair [ Cell Rep, 2025, 44(4):115452] | PubMed: 40117291 |
| Steroid-Modulated Transcription Synergistically Forms DNA Double-Strand Breaks With Topoisomerase II Inhibitor [ Cancer Sci, 2025, 10.1111/cas.70081] | PubMed: 40231641 |
| The novel role of LCK and other PcDEGs in the diagnosis and prognosis of sepsis: Insights from bioinformatic identification and experimental validation [ Int Immunopharmacol, 2025, 149:114194] | PubMed: 39904039 |
| The Kinase Inhibitor GNF-7 Is Synthetically Lethal in Topoisomerase 1-Deficient Ewing Sarcoma [ Cancers (Basel), 2025, 17(15)2475] | PubMed: 40805174 |
| Peroxiredoxin 1 inhibits tumorigenesis by activating the NLRP3/GSDMD pathway to induce pyroptosis of colorectal cancer cells [ World J Gastroenterol, 2025, 31(36):111557] | PubMed: 41025079 |
| Discovery and Characterization of Small Molecule Inhibitors Targeting Exonuclease 1 for Homologous Recombination-Deficient Cancer Therapy [ ACS Chem Biol, 2025, 10.1021/acschembio.5c00117] | PubMed: 40378357 |
| DDX18 influences chemotherapy sensitivity in colorectal cancer by regulating genomic stability [ Exp Cell Res, 2025, 444(1):114344] | PubMed: 39577603 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
