Technische Daten
| Formel | C17H14F3N3O2S |
||||||||||
| Molekulargewicht | 381.37 | CAS-Nr. | 169590-42-5 | ||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 100 mg/mL (262.21 mM) | ||||||||
| Ethanol | 76 mg/mL (199.28 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Celecoxib ist ein selektiver COX-2-Inhibitor mit einer IC50 von 40 nM in Sf9-Zellen. | ||
|---|---|---|---|
| Ziele |
|
||
| In vitro | Celecoxib zeigt eine geringe Empfindlichkeit gegenüber COX-1 mit einer IC50 von 15 μM. Diese Verbindung zeigt eine antiproliferative Wirkung auf Zelllinien des Nasopharynxkarzinoms (NPC) einschließlich HNE1 und CNE1-LMP1 mit einer IC50 von 32,86 μM bzw. 61,31 μM. |
||
| In vivo | Celecoxib zeigt eine potente, orale entzündungshemmende Aktivität. Diese Verbindung reduziert akute Entzündungen im Carrageenan-Ödem-Assay und chronische Entzündungen im Adjuvans-Arthritis-Modell mit einer ED50 von 7,1 mg/kg bzw. 0,37 mg/kg/Tag. Darüber hinaus zeigt es auch eine analgetische Aktivität im Hargreaves-Hyperalgesie-Modell mit einer ED50 von 34,5 mg/kg. Außerdem verursacht diese Chemikalie bei Ratten keine akute GI-Toxizität bei Dosen von bis zu 200 mg/kg und keine chronische GI-Toxizität bei Ratten bei Dosen von bis zu 600 mg/kg/Tag über 10 Tage. In einem C3Hf/KamLaw weiblichen Mausmodell erhöht es die mediane Überlebenszeit von 105 Tagen (Bereich, 79-145 Tage) nach 13,5 Gy lokaler thorakaler Bestrahlung (LTI) allein auf 142 Tage (Bereich, 94-155 Tage). |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
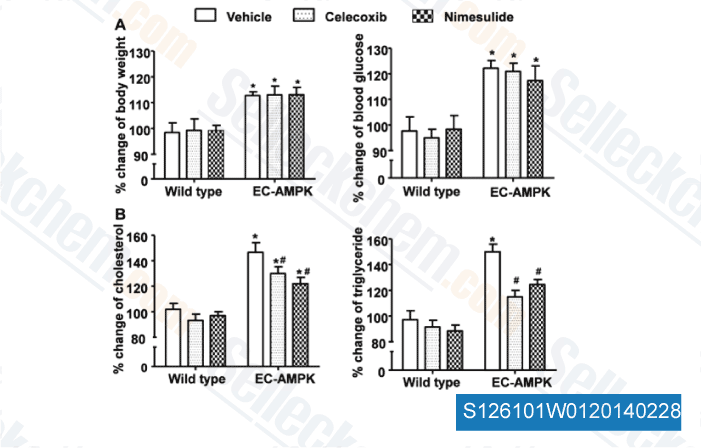
-
Daten von [ Br J Pharmacol , 2014 , 171(2), 498-508 ]
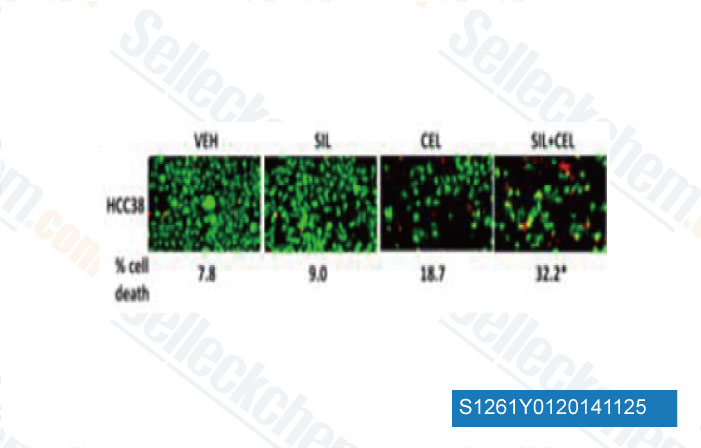
-
Daten von [ J Cell Physiol , 2014 , 10.1002/jcp.24843 ]
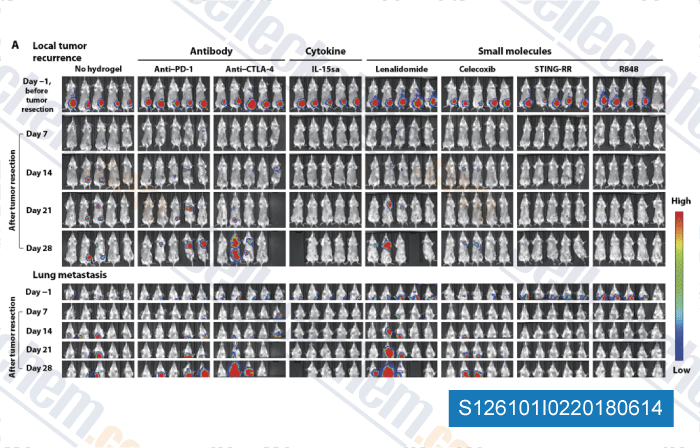
-
Daten von [ , , Science, 2018, 10(433), doi: 10.1126/scitranslmed.aar1916 ]
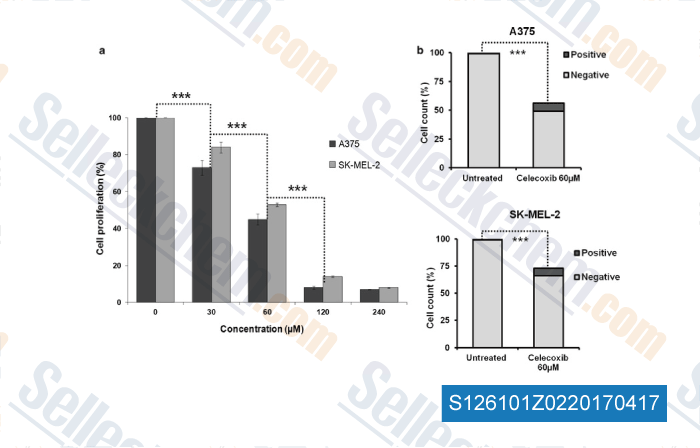
-
Daten von [ , , J Transl Med, 2017, 15(1):46 ]
Sellecks Celecoxib (SC-58635) Wurde zitiert von 115 Publikationen
| Tumor-initiating stem cells fine-tune the plasticity of neutrophils to sculpt a protective niche [ Cancer Cell, 2025, S1535-6108(25)00494-5] | PubMed: 41349542 |
| Monkeypox virus induces ferroptosis to facilitate viral replication and promotes inflammatory responses [ Emerg Microbes Infect, 2025, 14(1):2522877] | PubMed: 40536397 |
| The nonsteroidal anti-inflammatory drug sulindac reverses obesity-driven immunosuppression and triple-negative breast cancer progression [ Breast Cancer Res, 2025, 27(1):186] | PubMed: 41137072 |
| Carbonic anhydrase 2-derived drug-responsive domain regulates membrane-bound cytokine expression and function in engineered T cells [ Commun Biol, 2025, 8(1):28] | PubMed: 39789216 |
| Hyperoxia-activated Nrf2 regulates ferroptosis in intestinal epithelial cells and intervenes in inflammatory reaction through COX-2/PGE2/EP2 pathway [ Mol Med, 2025, 31(1):1] | PubMed: 39754066 |
| Protein kinase a suppresses antiproliferative effect of interferon-α in hepatocellular carcinoma by activation of protein tyrosine phosphatase SHP2 [ J Biol Chem, 2025, 301(2):108195] | PubMed: 39826687 |
| Missense Mutant p53 Transactivates Wnt/β-Catenin Signaling in Neighboring p53-Destabilized Cells through the COX-2/PGE2 Pathway [ Cancer Res Commun, 2025, 5(1):13-23] | PubMed: 39641656 |
| Leptin-mediated suppression of lipoprotein lipase cleavage enhances lipid uptake and facilitates lymph node metastasis in gastric cancer [ Cancer Commun (Lond), 2024, 10.1002/cac2.12583] | PubMed: 38958445 |
| Therapeutic Anti-Tumor Efficacy of DC-Based Vaccines Targeting TME-Associated Antigens Is Improved When Combined with a Chemokine-Modulating Regimen and/or Anti-PD-L1 [ Vaccines (Basel), 2024, 12(7)777] | PubMed: 39066414 |
| Celecoxib Combined with Tocilizumab Has Anti-Inflammatory Effects and Promotes the Recovery of Damaged Cartilage via the Nrf2/HO-1 Pathway In Vitro [ Biomolecules, 2024, 14(12)1636] | PubMed: 39766343 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
