Technische Daten
| Formel | C23H23ClFNO5 |
||||||
| Molekulargewicht | 447.88 | CAS-Nr. | 697761-98-1 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 89 mg/mL (198.71 mM) | ||||
| Ethanol | 35 mg/mL (78.14 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Elvitegravir ist ein HIV-Integrase-Inhibitor für HIV-1 IIIB, HIV-2 EHO und HIV-2 ROD mit einer IC50 von 0,7 nM, 2,8 nM bzw. 1,4 nM in zellfreien Assays. | ||||||
|---|---|---|---|---|---|---|---|
| Ziele |
|
||||||
| In vitro | Elvitegravir hemmt PBMC und PA mit einer IC50 von 0,89 bzw. 20 nM. Diese Verbindung verhindert die Integration von HIV-1-cDNA durch die Hemmung des DNA-Strangtransfers. Sie unterdrückt die Replikation von HIV-1, einschließlich verschiedener Subtypen und multiresistenter klinischer Isolate, sowie von HIV-2-Stämmen mit einer 50 %igen effektiven Konzentration im subnanomolaren bis nanomolaren Bereich. Dieser Inhibitor blockiert die Replikation von klinischen HIV-1-Isolaten, die NRTI-, NNRTI- und PI-resistenzassoziierte Genotypen tragen. Er hemmt die HIV-Replikation in einem Schritt, der nach der reversen Transkription, aber vor der proteolytischen Spaltung erfolgt, was mit dem Integrationsschritt übereinstimmt. Diese Chemikalie hemmt die Synthese von Strangtransferprodukten mit einer IC50 von 54 nM. Sie blockiert die Integration über die Hemmung des IN-vermittelten Strangtransfers. Dieses Mittel hemmt die Integration des auf HIV basierenden Vektors, der als positive Kontrolle für den Luciferase-Assay verwendet wird, mit einer EC50 von 0,8 nM, wie im MAGI-Assay mit HIV-1IIIB beobachtet. Es unterdrückt die Replikation der MLV-Infektion mit einer IC50 von 5,8 nM sowie die des Primatenretrovirus SIV (IC50 = 0,5 nM), was zeigt, dass IN-Inhibitoren eine antivirale Aktivität gegen ein breites Spektrum von Retroviren aufweisen. Diese Verbindung ist aktiv gegen HIV-1 und HIV-2 und hat eine serumfreie antivirale IC50 von 0,3-0,9 nM in peripheren Blutmononukleären Zellen. |
Protokoll (aus Referenz)
Referenzen
|
Kundenproduktvalidierung
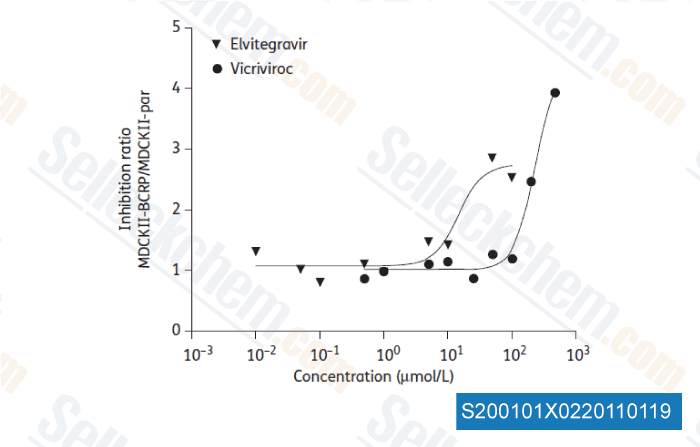
-
Daten von [ J Antimicrob Chemother , 2011 , 66, 802-812 ]
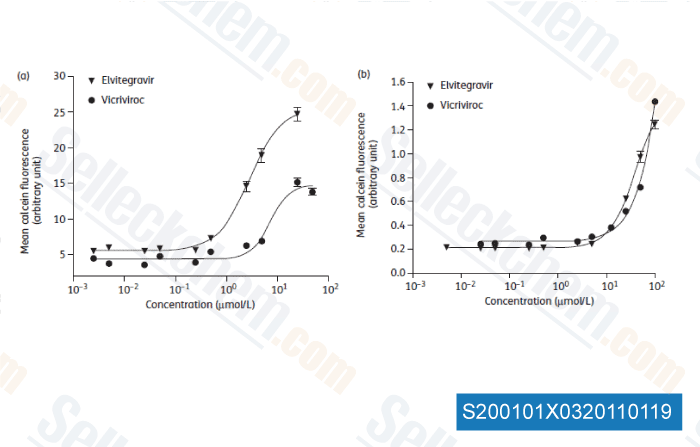
-
Daten von [ J Antimicrob Chemother , 2011 , 66, 802-812 ]
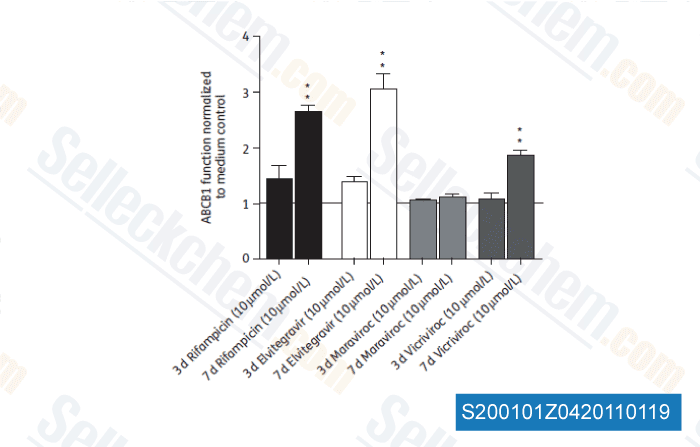
-
Daten von [ J Antimicrob Chemother , 2011 , 66, 802-812 ]
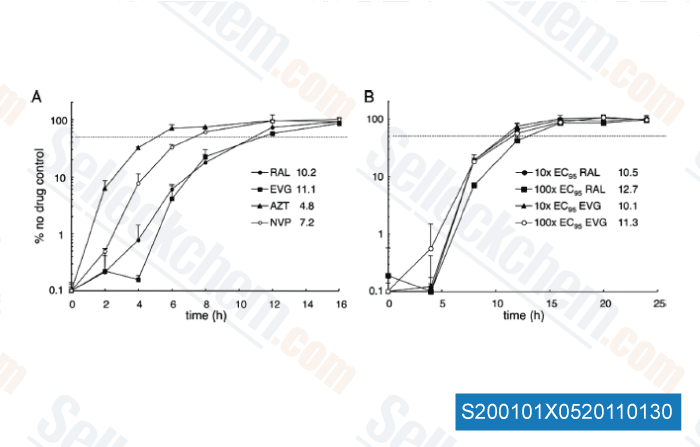
-
Daten von [ Antim Ag Ch , 2011 , 55, 42-49 ]
Sellecks Elvitegravir Wurde zitiert von 34 Publikationen
| HMGB1 Expression Levels Correlate with Response to Immunotherapy in Non-Small Cell Lung Cancer [ Lung Cancer, 2024, 15:55-67] | PubMed: 38741920 |
| Biological and Structural Analyses of New Potent Allosteric Inhibitors of HIV-1 Integrase [ Antimicrob Agents Chemother, 2023, 67(7):e0046223] | PubMed: 37310224 |
| Acute antagonism in three-drug combinations for vaginal HIV prevention in humanized mice [ Sci Rep, 2023, 13(1):4594] | PubMed: 36944714 |
| Anti-HIV drug elvitegravir suppresses cancer metastasis via increased proteasomal degradation of m6A methyltransferase METTL3 [ Cancer Res, 2022, canres.4124.2021] | PubMed: 35507004 |
| In Vitro Susceptibility of HIV Isolates with High Growth Capability to Antiretroviral Drugs [ Int J Mol Sci, 2022, 23(23)15380] | PubMed: 36499705 |
| Reduction of CD8 T cell functionality but not inhibitory capacity by integrase inhibitors [ J Virol, 2022, JVI0173021] | PubMed: 35019724 |
| Impact of combinations of clinically observed HIV integrase mutations on phenotypic resistance to integrase strand transfer inhibitors (INSTIs): a molecular study [ J Antimicrob Chemother, 2022, dkab498] | PubMed: 35061879 |
| Biochemical Activity of RAGs Is Impeded by Dolutegravir, an HIV Integrase Inhibitor [ Cell Death Discov, 2020, 6:50] | PubMed: 32566255 |
| Effect of HIV infection and antiretroviral therapy on immune cellular functions. [ JCI Insight, 2019, 4(12)] | PubMed: 31217351 |
| HIV-1 Subtype C with PYxE Insertion Has Enhanced Binding of Gag-p6 to Host Cell Protein ALIX and Increased Replication Fitness. [ J Virol, 2019, 93(9)] | PubMed: 30760577 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
