Technische Daten
| Formel | C26H27NO9.HCl |
||||||
| Molekulargewicht | 533.95 | CAS-Nr. | 57852-57-0 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 100 mg/mL (187.28 mM) | ||||
| Water | 2 mg/mL (3.74 mM) | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Idarubicin HCl (4-Demethoxydaunorubicin (NSC256439, 4-DMDR) HCl) ist eine Hydrochlorid-Salzform von Idarubicin, einem Anthracyclin-Antibioticum und einem DNA topoisomerase II (topo II)-Inhibitor für MCF-7-Zellen mit einer IC50 von 3,3 ng/mL in einem zellfreien Assay. Idarubicin induziert mTOR-abhängige zytotoxische autophagy. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | Idarubicin zeigt eine signifikante zytotoxische Aktivität gegen multizelluläre Sphäroide, vergleichbar mit den antiproliferativen Effekten auf Monolayer-Zellen. Idarubicin hemmt CYP450 2D6. Idarubicin ist etwa 57,5-fach und 25-fach aktiver als Doxorubicin bzw. Epirubicin. Idarubicin ist in der Lage, P-Glykoprotein-vermittelte Multidrug-Resistenz zu überwinden. Idarubicin hemmt die PMN-Superoxidradikalbildung. Idarubicin konnte mit monoklonalen Antikörpern (Anti-Ly-2.1, Anti-L3T4 oder Anti-Thy-1) gekoppelt werden, wobei die Proteinlöslichkeit und Antikörperaktivität erhalten blieben. Idarubicin hemmt die Proliferation von NALM-6-Zellen mit einer IC50 von 12 nM. |
||||
| In vivo | Die Reduktion von Idarubicin ist von Ketonreduktasen abhängig und verläuft stereoselektiver als die der meisten Ketone, wobei fast ausschließlich das (13S)-Epimer entsteht. Die hohe Stereospezifität bei der Idarubicin-Reduktion könnte auf chirale Induktion aufgrund des Vorhandenseins asymmetrischer Zentren nahe der Carbonylgruppe in Idarubicin zurückzuführen sein. |
||||
| Merkmale | Idarubicin ist ein Substrat für CYP450 2D6 und 2C9. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
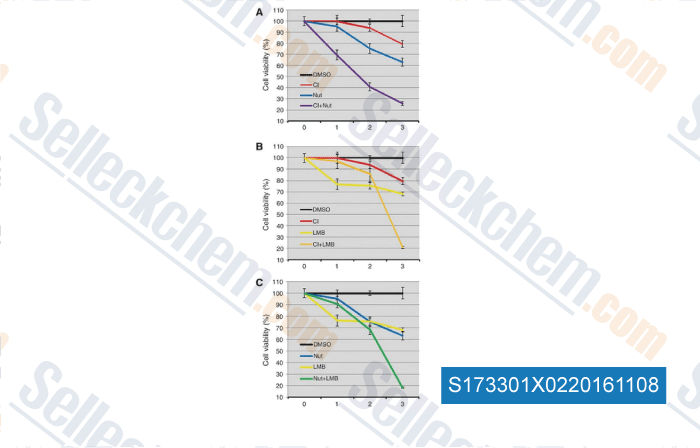
-
, , Clin Cancer Res, 2016, 22(3):746-56.
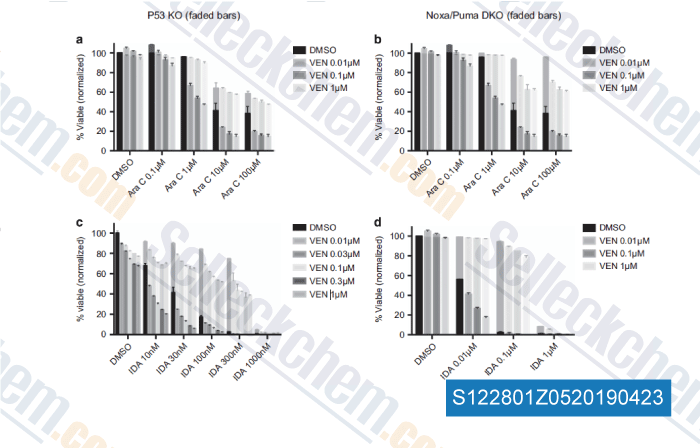
-
Daten von [ , , Leukemia, 2018, 32(2):303-312 ]
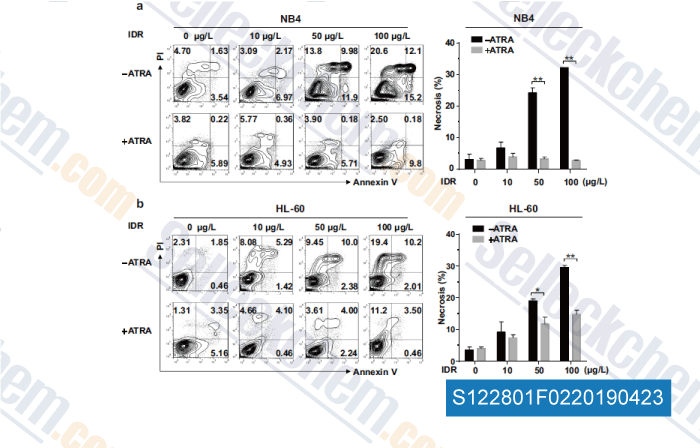
-
Daten von [ , , Mol Cell Biochem, 2018, doi:10.1007/s11010-018-3402-0 ]
Sellecks Idarubicin HCl Wurde zitiert von 58 Publikationen
| An isoform-specific RUNX1C-BTG2 axis governs AML quiescence and chemoresistance [ Blood Cancer Discov, 2025, 10.1158/2643-3230.BCD-24-0327] | PubMed: 40632085 |
| An Isoform-Specific RUNX1C-BTG2 Axis Governs AML Quiescence and Chemoresistance [ Blood Cancer Discov, 2025, 6(5):464-483] | PubMed: 40632085 |
| Relevance of transportome among the mechanisms of chemoresistance in hepatoblastoma [ Biochem Pharmacol, 2025, 237:116914] | PubMed: 40185314 |
| G2 arrest primes hematopoietic stem cells for megakaryopoiesis [ Cell Rep, 2024, 43(7):114388] | PubMed: 38935497 |
| Patient-derived rhabdomyosarcoma cells recapitulate the genetic and transcriptomic landscapes of primary tumors [ iScience, 2024, 27(10):110862] | PubMed: 39319271 |
| Immuno-oncological effects of standard anticancer agents and commonly used concomitant drugs: an in vitro assessment [ BMC Pharmacol Toxicol, 2024, 25(1):25] | PubMed: 38444002 |
| Histone H3 lysine 27 crotonylation mediates gene transcriptional repression in chromatin [ Mol Cell, 2023, 83(13):2206-2221.e11] | PubMed: 37311463 |
| Spermatogenesis associated serine rich 2 like plays a prognostic factor and therapeutic target in acute myeloid leukemia by regulating the JAK2/STAT3/STAT5 axis [ J Transl Med, 2023, 21(1):115] | PubMed: 36774517 |
| Relevance of the organic anion transporting polypeptide 1B3 (OATP1B3) in the personalized pharmacological treatment of hepatocellular carcinoma [ Biochem Pharmacol, 2023, 214:115681] | PubMed: 37429423 |
| p53 controls choice between apoptotic and non-apoptotic death following DNA damage [ bioRxiv, 2023, 2023.01.17.524444] | PubMed: 36712034 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
