Technische Daten
| Formel | C14H19BCl2N2O4 |
||||||
| Molekulargewicht | 361.03 | CAS-Nr. | 1072833-77-2 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 72 mg/mL (199.42 mM) | ||||
| Ethanol | 72 mg/mL (199.42 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Ixazomib (MLN2238) hemmt die Chymotrypsin-ähnliche proteolytische (β5) Stelle des 20S proteasome mit IC50 und Ki von 3,4 nM bzw. 0,93 nM in zellfreien Assays und hemmt auch die Caspase-ähnlichen (β1) und Trypsin-ähnlichen (β2) proteolytischen Stellen mit IC50 von 31 und 3500 nM. Ixazomib (MLN2238) induziert autophagy. Phase 3. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | Bei höheren Konzentrationen hemmt diese Verbindung auch die Caspase-ähnlichen (β1) und Trypsin-ähnlichen (β2) proteolytischen Stellen mit IC50-Werten von 31 nM bzw. 3,5 uM. Es hemmt Calu-6-Zellen mit einem IC50-Wert von 9,7 nM. MLN2238 ist ein selektiver, potenter und reversibler Inhibitor des Proteasome in Tumorzellen. Diese Verbindung zeigt eine zeitabhängige reversible Proteasome-Hemmung. Sowohl diese Verbindung als auch Bortezomib zeigen eine zeitabhängige reversible Proteasome-Hemmung; jedoch ist die Dissoziationshalbwertszeit des Proteasome für sie etwa 6-mal schneller als die von Bortezomib (18 bzw. 110 Minuten). Es dissoziiert schneller vom Proteasome als Bortezomib, was mit einer schnelleren Wiederherstellung der Proteasome-Aktivität übereinstimmt, die im Proteasome-Glo-Assay beobachtet wurde. Es hat einen größeren gesamten Tumor-pharmakodynamischen Effekt als Bortezomib, bewertet durch 20S-Hemmung. Diese Verbindung ist die biologisch aktive Form von MLN9708. | ||||
| In vivo | MLN2238 induziert eine größere pharmakodynamische Reaktion als Bortezomib in Xenograft-Tumoren. Diese Verbindung zeigt eine größere maximale und anhaltende Tumor-Proteasome-Hemmung im Vergleich zu Bortezomib in Xenograft-Modellen. Diese Ergebnisse bestätigen, dass die verbesserte Tumorexposition, die mit diesem Mittel beobachtet wird, sich in eine verbesserte tumorpharmakodynamische Reaktion sowohl auf der Ebene des Proteasome als auch nachgeschaltet vom Proteasome übersetzt. Es zeigt Antitumoraktivität im CWR22-Xenograft-Modell. Diese Chemikalie zeigt im Vergleich zu Bortezomib größere tumorpharmakodynamische Reaktionen in WSU-DLCL2-Xenografts. In ähnlicher Weise führte die Bortezomib-Behandlung nur zu einem geringfügigen Anstieg der GADD34-Spiegel in WSU-DLCL2-Xenograft-Tumoren, während sie dessen Expression stark induziert. Diese Verbindung hat ein verbessertes pharmakodynamisches Profil und eine verbesserte Antitumoraktivität im Vergleich zu Bortezomib in beiden OCI-Ly10- und PHTX22L-Modellen. | ||||
| Merkmale | Ein First-in-Class-Proteasom-Inhibitor, der in präklinischen Studien verbesserte pharmakokinetische (PK), pharmakodynamische (PD) und Antitumoraktivität aufweist. |
Protokoll (aus Referenz)
| Kinase-Assay:[1] |
|
|---|---|
| Zell-Assay:[1] |
|
| Tierstudie:[2] |
|
Referenzen
|
Kundenproduktvalidierung
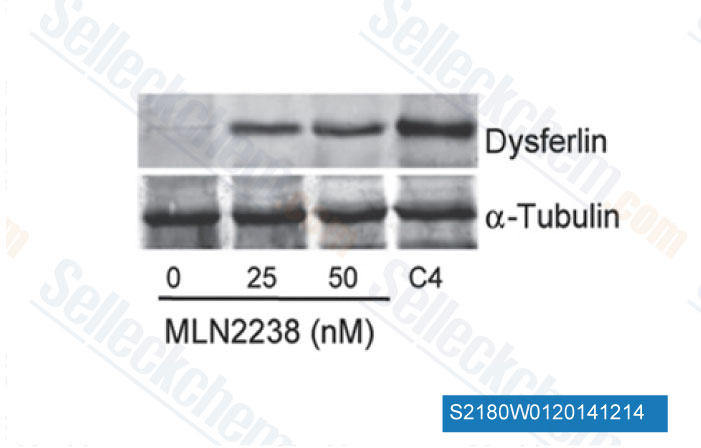
-
Daten von [ Sci Transl Med , 2014 , 6(250), 250ra112 ]
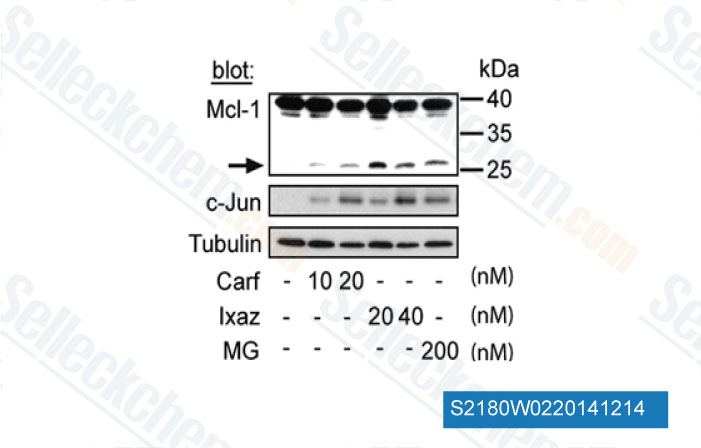
-
Daten von [ Cancer Lett , 2014 , 343(2), 286-94 ]
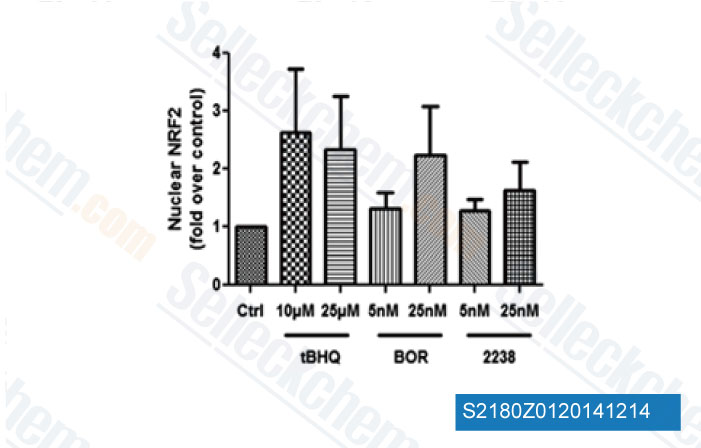
-
Daten von [ Hemoglobin , 2014 , 38(3), 188-95 ]
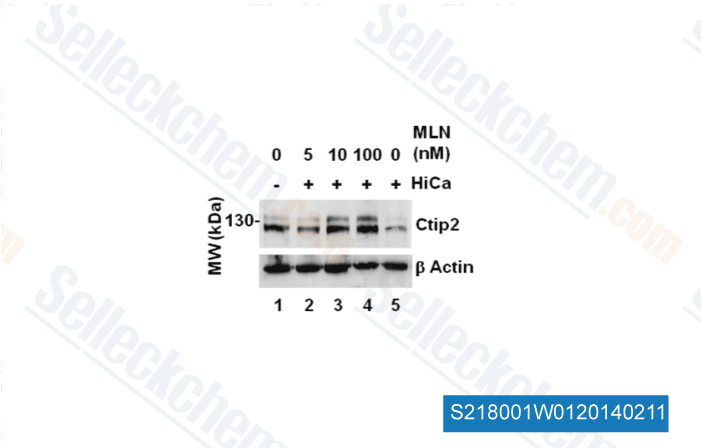
-
Daten von [ J Cell Sci , 2012 , 125(Pt 23), 5733-44 ]
Sellecks MLN2238 (Ixazomib) Wurde zitiert von 71 Publikationen
| Structural basis for allosteric modulation of M. tuberculosis proteasome core particle [ Nat Commun, 2025, 16(1):3138] | PubMed: 40169579 |
| A patient-derived T cell lymphoma biorepository uncovers pathogenetic mechanisms and host-related therapeutic vulnerabilities [ Cell Rep Med, 2025, S2666-3791(25)00102-8] | PubMed: 40147445 |
| Enhancing T cell cytotoxicity in multiple myeloma with bispecific αPD-L1 × αCD3 T cell engager-armed T cells and low-dose bortezomib therapy [ Biomed Pharmacother, 2025, 184:117878] | PubMed: 39891948 |
| High-Throughput Drug Screening of Clear Cell Ovarian Cancer Organoids Reveals Vulnerability to Proteasome Inhibitors and Dinaciclib and Identifies AGR2 as a Therapeutic Target [ Cancer Res Commun, 2025, 5(6):1018-1033] | PubMed: 40459063 |
| Integrated transcriptomics- and structure-based drug repositioning identifies drugs with proteasome inhibitor properties [ Sci Rep, 2024, 14(1):18772] | PubMed: 39138277 |
| A combinatorial therapeutic approach to enhance FLT3-ITD AML treatment [ Cell Rep Med, 2023, 10.1016/j.xcrm.2023.101286] | PubMed: 37951217 |
| Targeting ITGB4/SOX2-driven lung cancer stem cells using proteasome inhibitors [ iScience, 2023, 26(8):107302] | PubMed: 37554452 |
| Dual inhibition of HSF1 and DYRK2 impedes cancer progression [ Biosci Rep, 2023, 43(1)BSR20222102] | PubMed: 36622366 |
| Proteasome inhibition as a therapeutic target for the fungal pathogen Cryptococcus neoformans [ Microbiol Spectr, 2023, 11(5):e0190423] | PubMed: 37750732 |
| Proteasome inhibition as a therapeutic target for the fungal pathogen Cryptococcus neoformans [ Microbiol Spectr, 2023, 10.1128/spectrum.01904-23] | PubMed: 37750732 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
