Technische Daten
| Formel | C27H29N5O |
||||||
| Molekulargewicht | 439.55 | CAS-Nr. | 475489-16-8 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 88 mg/mL (200.2 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | NVP-AEW541 ist ein potenter Inhibitor von IGF-1R/InsR mit einer IC50 von 150 nM/140 nM in zellfreien Assays, mit größerer Potenz und Selektivität für IGF-1R in einem zellbasierten Assay. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ziele |
|
|||||||||||
| In vitro | NVP-AEW541 hemmt auch InsR, Tek, Flt1 und Flt3 mit einer IC50 von 140 nM, 530 nM, 600 nM und 420 nM in Assays mit gereinigten Kinasen/rekombinanten Kinasedomänen. Diese Verbindung ist selektiver und zeigt auf zellulärer Ebene eine 27-fach höhere Wirksamkeit als InsR. Sie unterdrückt das IGF-I-vermittelte Überleben, das Weichagar-Wachstum und die Proliferation von MCF-7-Zellen mit einer IC50 von 0,162 μM, 0,105 μM bzw. 1,64 μM. Diese Chemikalie reduziert auch den Spiegel von Phospho-IGF-1R und Phospho-PKB in NWT-21-Zellen. Sie zeigt eine wachstumshemmende Wirkung auf TC-71-Muskuloskelettalsarkomzellen in serumarmem Medium sowie in 10 % FBS-haltigem Medium. Diese Verbindung hemmt den Zellzyklus und induziert einen spezifischen G1-Arrest in Sarkomzelllinien (TC-71, SK-N-MC, SaoS-2, RD/18 und RH4). Sie könnte das Wachstum menschlicher Neuroblastomzellen mit einer IC50 von 0,4-6,8 μM hemmen. Eine Zunahme der hypodiploiden Fraktion und die Depletion der S- und G2-M-Kompartimente konnten in diesen Zelllinien nachgewiesen werden. Diese Verbindung-getriebene Hemmung von IGF-1R führt zu einer Reduktion der Phosphorylierung von Akt, aber nicht von Erk1 und Erk2 in Neuroblastomzellen. Sie hemmt das Gliomzellwachstum und stört die autokrine Schleife, die durch HIF1α-Stabilisierung initiiert wird. Eine aktuelle Studie zeigt, dass diese Chemikalie die Proliferation und Viabilität von PC3-, DU145- und 22Rv1-Prostatakrebszellen unterdrückt, ohne dass ein assoziierter Zelltod erforderlich ist. Sie senkt die Phospho-Akt-Spiegel in 22Rv1- und DU415-Zellen, nicht aber in PC3-Zellen, ohne die Gesamt-Akt-Spiegel zu beeinflussen, was zeigt, dass der PTEN-Status die Wirksamkeit dieser Verbindung mit essentiellem Akt bestimmen könnte. Die durch diese Verbindung induzierte Radiosensibilisierung ist vom Akt-Aktivierungsstatus abhängig. Sie könnte die H2AX-Phosphorylierung (ein Maß für DSBs) in PC3-, DU145- und 22Rv1-Zellen erhöhen. | |||||||||||
| In vivo | NVP-AEW541 (50 mg/kg, p.o.) führt zur Aufhebung der basalen und IGF-I-induzierten Rezeptor-, sowie PKB- und MAPK-Phosphorylierung, mit einem T/C-Wert von 14 % im NWT-21-Tumorxenograft. Diese Verbindung (50 mg/kg) verursacht eine Tumorschrumpfung sowohl in HTLA-230- als auch in SK-N-BE2c-Xenografts, ohne Anzeichen systemischer Toxizität. Sie könnte die Tumorinvasion sowohl in Matrigel-beschichteten Kammern als auch in HTLA-230-Xenografts hemmen. |
Protokoll (aus Referenz)
| Kinase-Assay:[1] |
|
|---|---|
| Zell-Assay:[1] |
|
| Tierstudie:[1] |
|
Referenzen
|
Kundenproduktvalidierung
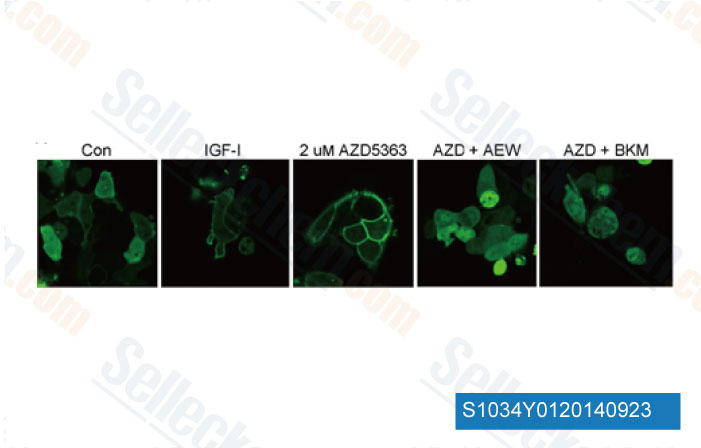
-
Daten von [ Breast Cancer Res , 2013 , 15, R55 ]
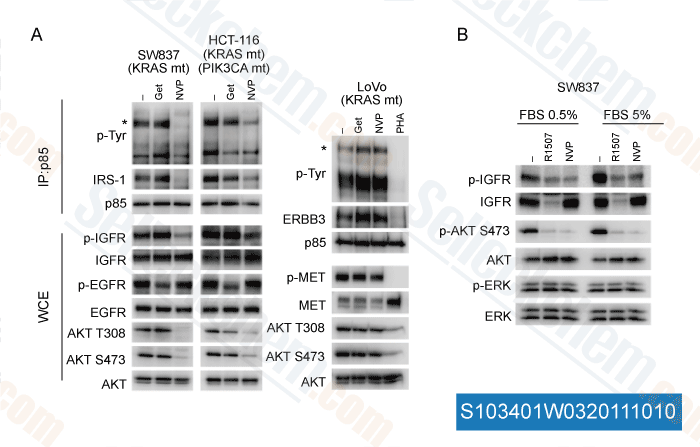
-
Daten von [ J Clin Invest , 2011 , 121, 4311-21 ]
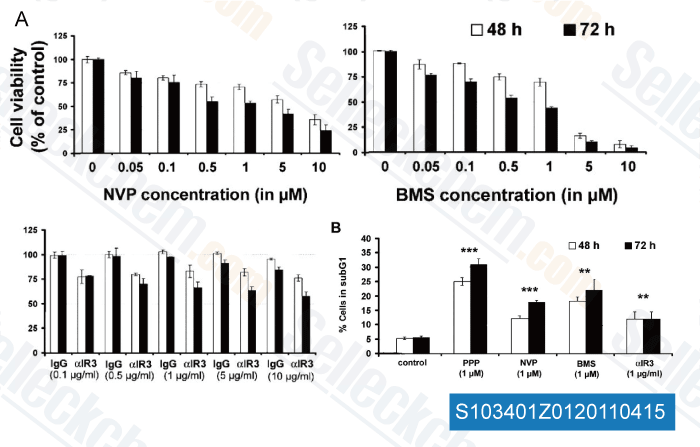
-
Daten von [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
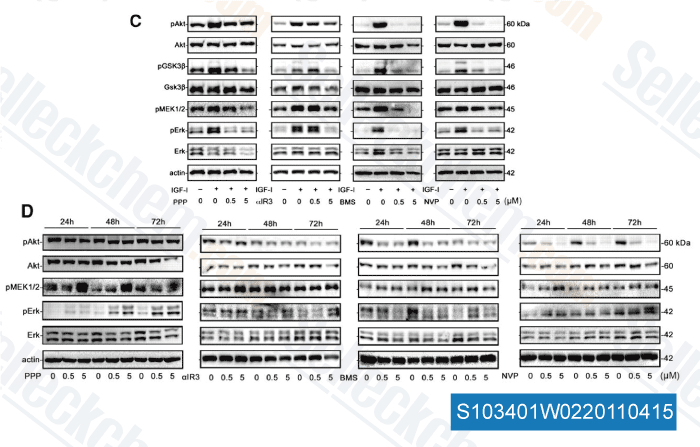
-
Daten von [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
Sellecks NVP-AEW541 Wurde zitiert von 67 Publikationen
| Translocation of IGF-1R in endoplasmic reticulum enhances SERCA2 activity to trigger Ca2+ER perturbation in hepatocellular carcinoma [ Acta Pharm Sin B, 2023, 13(9):3744-3755] | PubMed: 37719369 |
| Anatomic position determines oncogenic specificity in melanoma [ Nature, 2022, 604(7905):354-361] | PubMed: 35355015 |
| Integrative analysis of drug response and clinical outcome in acute myeloid leukemia [ Cancer Cell, 2022, S1535-6108(22)00312-9] | PubMed: 35868306 |
| SFRP4+ stromal cell subpopulation with IGF1 signaling in human endometrial regeneration [ Cell Discov, 2022, 8(1):95] | PubMed: 36163341 |
| Comprehensive drug response profiling and pan-omic analysis identified therapeutic candidates and prognostic biomarkers for Asian cholangiocarcinoma [ iScience, 2022, 25(10):105182] | PubMed: 36248745 |
| Strong Synergic Growth Inhibition and Death Induction of Cancer Cells by Astragalus membranaceus and Vaccaria hispanica Extract [ Cancers (Basel), 2022, 14(23)5833] | PubMed: 36497315 |
| Differential cytotoxic activity of pharmacological inhibitors of IGF1R-related pathways in JAK2V617F driven cells [ Toxicol In Vitro, 2022, 83:105384] | PubMed: 35568132 |
| Targeting Aurora B kinase prevents and overcomes resistance to EGFR inhibitors in lung cancer by enhancing BIM- and PUMA-mediated apoptosis [ Cancer Cell, 2021, S1535-6108(21)00383-4] | PubMed: 34388376 |
| Three subtypes of lung cancer fibroblasts define distinct therapeutic paradigms [ Cancer Cell, 2021, S1535-6108(21)00492-X] | PubMed: 34624218 |
| Aerobic exercise and resistance exercise alleviate skeletal muscle atrophy through IGF-1/IGF-1R-PI3K/Akt pathway in mice with myocardial infarction [ Am J Physiol Cell Physiol, 2021, 10.1152/ajpcell.00344.2021] | PubMed: 34852207 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
