Technische Daten
| Formel | C26H19F3N4O |
||||||||||
| Molekulargewicht | 460.45 | CAS-Nr. | 742112-33-0 | ||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 11 mg/mL (23.88 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | OSU-03012 (AR-12) ist ein potenter Inhibitor der rekombinanten PDK-1 (Phosphoinositid-abhängige Kinase 1) mit einer IC50 von 5 μM in einem zellfreien Assay, der eine 2-fache Potenzsteigerung gegenüber OSU-02067 aufweist. | ||
|---|---|---|---|
| Ziele |
|
||
| In vitro | OSU-03012 (AR-12) induziert den apoptotischen Zelltod in PC-3-Zellen mit einer IC50 von 5 µM und reduziert die Aktivität der immunpräzipitierten p70S6K. Es unterdrückt das Zellwachstum in einer Vielzahl von Tumorzelllinien bei Konzentrationen von 3–5 μm vollständig, verglichen mit einer Konzentration von mindestens 50 μm. Diese Verbindung fördert das Abtöten von Gliazellen in größerem Maße als in nicht transformierten Astrozyten. Sie verursacht eine dosisabhängige Induktion des Zelltods, der durch p53-Mutation, Expression von ERBB1 VIII oder den Verlust der Phosphatase- und Tensin-Funktion aufgrund einer homologen Deletion auf Chromosom 10 nicht verändert wird. OSU-03012 und ionisierende Strahlung verursachen eine additive, Caspase-unabhängige Erhöhung des Zelltods. Ihre Letalität als Einzelwirkstoff oder in Kombination mit Signalmodulatoren wird in Zellen, denen die Expression von BIM oder von BAX/BAK fehlt, nicht modifiziert. Sie fördert die Freisetzung von Cathepsin B aus dem lysosomalen Kompartiment und von AIF aus den Mitochondrien. Die Letalität dieser Verbindung ist in Protein-Kinase-R-ähnlichen Endoplasmatisches-Retikulum-Kinase-/-Zellen abgeschwächt, was mit der reduzierten Spaltung von BID und der Unterdrückung der Freisetzung von Cathepsin B und AIF in das Zytosol korrelierte. Es hemmt die Proliferation und Migration von Schilddrüsenkrebszellen (NPA-, WRO- und ARO-Zellen) und induziert Apoptose, was zu einer Zunahme der Zellen in der S-Phase ohne Zunahme der Zellen in G2 führt. OSU-03012 ist ein ATP-kompetitiver Inhibitor der PAK-Aktivität und unterdrückt die Phosphorylierung von AKT in Schilddrüsenkrebszellen. Es hemmt das Zellwachstum von hepatozellulären Karzinomzelllinien, einschließlich Huh7-, Hep3B- und HepG2-Zellen, mit IC50-Werten unter 1 μM. Diese Verbindung unterdrückt weder die PDK1- oder AKT-Aktivität noch induziert sie die zelluläre Apoptose, sondern induziert Autophagie in Huh7-Zellen. Darüber hinaus wird nach ihrer Behandlung eine Akkumulation reaktiver Sauerstoffspezies (ROS) nachgewiesen. Eine aktuelle Studie zeigt, dass sie die Anfälligkeit von (Bcr)-Abl-mutierten Zelllinien für Apoptose verstärken könnte. |
||
| In vivo | OSU-03012 (AR-12) unterdrückt das Tumorwachstum um 57,59% und erhöht gespaltenes LC3 in Huh7-Tumor-Xenografts bei 200 mg/kg. Diese Verbindung verringert die Expression des EGFR-Proteins in den Tumoren um 48% im Vergleich zu Vehikelkontrollen und verhindert auch, dass YB-1 an den EGFR-Promotor in MDA-MB-435/LCC6-Xenografts bindet. Es wird gut vertragen und hemmt das Wachstum von HMS-97-Schwannom-Xenografts um 55% nach oraler Verabreichung. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
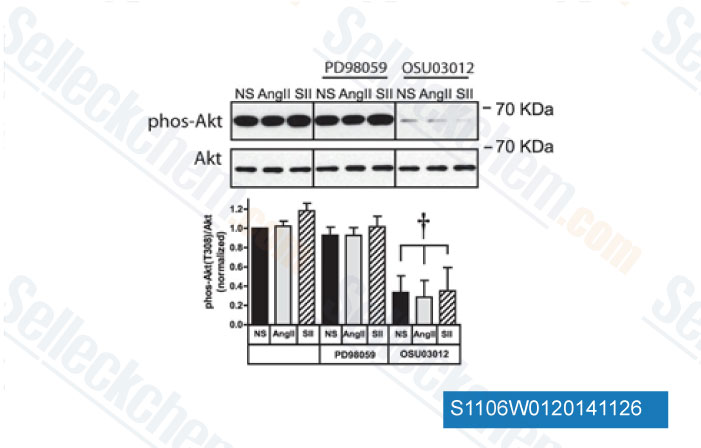
-
Daten von [ J Biol Chem , 2014 , 289(38), 26155-66 ]
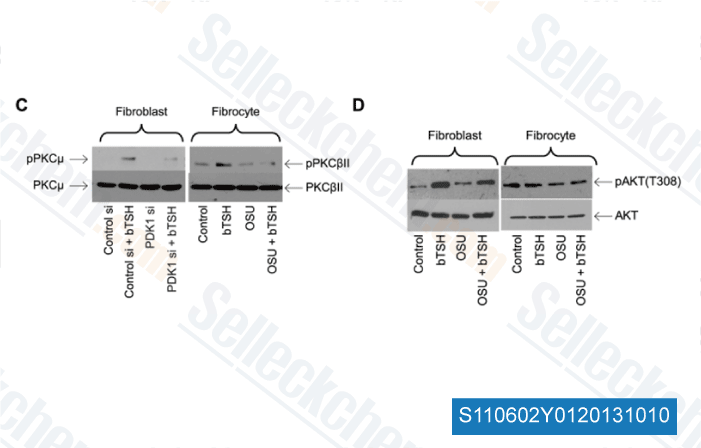
-
Daten von [ PLoS One , 2013 , 8, e75100 ]
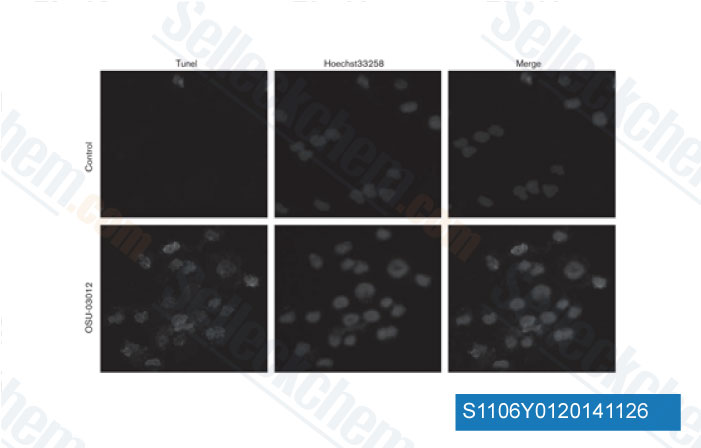
-
Daten von [ Anticancer Drugs , 2013 , 24(7), 690-8 ]
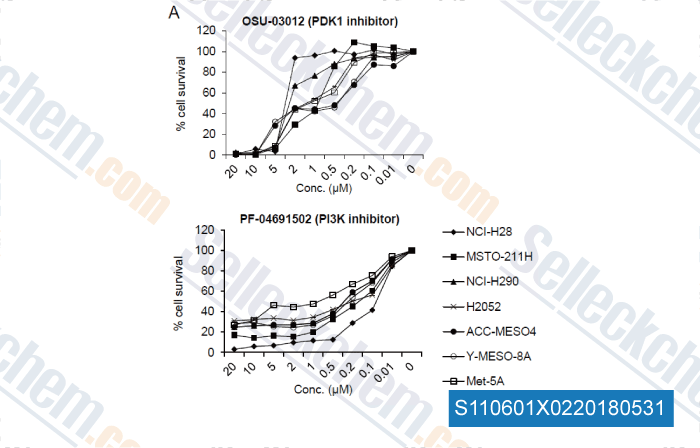
-
Daten von [ , , Cancer Medicine, 2017, 6(11):2646-2659 ]
Sellecks OSU-03012 (AR-12) Wurde zitiert von 51 Publikationen
| R406 and its structural analogs reduce SNCA/α-synuclein levels via autophagic degradation [ Autophagy, 2025, 1-17.] | PubMed: 40143425 |
| NAC1 confines virus-specific memory formation of CD4+ T cells through the ROCK1-mediated pathway [ J Med Virol, 2023, 95(7):e28957] | PubMed: 37465969 |
| Salmonella effector SopF regulates PANoptosis of intestinal epithelial cells to aggravate systemic infection [ Gut Microbes, 2023, 15(1):2180315] | PubMed: 36803521 |
| AR12 increases BAG3 expression which is essential for Tau and APP degradation via LC3-associated phagocytosis and macroautophagy [ Aging (Albany NY), 2022, 14(20):8221-8242] | PubMed: 36227739 |
| Pulmonary fibrosis distal airway epithelia are dynamically and structurally dysfunctional [ Nat Commun, 2021, 12(1):4566] | PubMed: 34315881 |
| Development of potent dual PDK1/AurA kinase inhibitors for cancer therapy: Lead-optimization, structural insights, and ADME-Tox profile [ Eur J Med Chem, 2021, 226:113895] | PubMed: 34624821 |
| Decanoic Acid Stimulates Autophagy in D. discoideum [ Cells, 2021, 10(11)2946] | PubMed: 34831171 |
| Inhibition of heat shock proteins increases autophagosome formation, and reduces the expression of APP, Tau, SOD1 G93A and TDP-43 [ Aging (Albany NY), 2021, 13(13):17097-17117] | PubMed: 34252884 |
| OSU-03012 Disrupts Akt Signaling and Prevents Endometrial Carcinoma Progression in vitro and in vivo [ Drug Des Devel Ther, 2021, 15:1797-1810] | PubMed: 33958857 |
| Metabolic Modifier Screen Reveals Secondary Targets of Protein Kinase Inhibitors Within Nucleotide Metabolism [ Cell Chem Biol, 2020, 20;27(2):197-205.e6] | PubMed: 31734178 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
