Technische Daten
| Formel | C28H41N7O3 |
||||||
| Molekulargewicht | 523.67 | CAS-Nr. | 219580-11-7 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 105 mg/mL (200.5 mM) | ||||
| Ethanol | 105 mg/mL (200.5 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | PD173074 ist ein potenter FGFR1-Inhibitor mit einer IC50 von ~25 nM und hemmt auch VEGFR2 mit einer IC50 von 100-200 nM in zellfreien Assays, ~1000-fach selektiver für FGFR1 als PDGFR und c-Src. PD173074 reduziert die Proliferation und fördert die Apoptose in Magenkrebszellen. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | PD173074 ist ein ATP-kompetitiver Inhibitor von FGFR1 mit einem Ki von ~40 nM. Diese Verbindung ist auch ein wirksamer Inhibitor von VEGFR2. Im Vergleich zu FGFR1 hemmt sie die Aktivitäten von Src, InsR, EGFR, PDGFR, MEK und PKC schwach mit 1000-fach oder höheren IC50-Werten. Dieser Inhibitor hemmt die Autophosphorylierung von FGFR1 und VEGFR2 dosisabhängig mit einer IC50 von 1-5 nM bzw. 100-200 nM. Er hemmt die FGF-2-Förderung des Überlebens von Granula-Neuronen dosisabhängig mit einer IC50 von 12 nM, wobei er eine 1.000-fach höhere Wirksamkeit als SU 5402 aufweist. Diese Chemikalie hemmt spezifisch FGF-2-vermittelte Effekte auf Proliferation, Differenzierung und MAPK-Aktivierung in Oligodendrozyten (OL)-Linienzellen. Sie ist aktiv gegen den WT-Rezeptor und FGFR3-Mutationen in Multiples Myelom (MM)-Zelllinien. Diese Verbindung hemmt auch potent die Autophosphorylierung von FGFR3 dosisabhängig mit einer IC50 von ~5 nM. Ihre Behandlung reduziert potent die Lebensfähigkeit von FGFR3-exprimierenden KMS11- und KMS18-Zellen mit einer IC50 von <20 nM. Die Hemmung des aFGF-stimulierten MM-Zellwachstums durch dieses Mittel korreliert stark mit der Expression von FGFR3. Ihre Behandlung hebt die NIH 3T3-Transformation, die durch Y373C FGFR3, aber nicht durch Ras V12 vermittelt wird, vollständig auf, was zeigt, dass sie spezifisch auf die FGFR3-vermittelte Zelltransformation abzielt und keine unspezifische zytotoxische Wirkung hat. Diese Chemikalie induziert auch die funktionelle Reifung von KMS11- und KMS18-Zellen. | ||||
| In vivo | Die Verabreichung von PD173074 in Dosen von 1 mg/kg/Tag oder 2 mg/kg/Tag an Mäuse kann die durch FGF oder VEGF induzierte Angiogenese dosisabhängig und ohne offensichtliche Toxizität wirksam blockieren. Diese Verbindung hemmt das In-vivo-Wachstum von mutant FGFR3-transfiziert NIH 3T3-Zellen in Nacktmäusen. Die Hemmung von FGFR3 durch diese Chemikalie verzögert das Tumorwachstum und erhöht das Überleben von Mäusen in einem KMS11-Xenograft-Myelommodell. Im H-510-Xenograft blockiert die orale Verabreichung dieser Verbindung das Tumorwachstum ähnlich wie bei einer Cisplatin-Einzeltherapie, wodurch das mittlere Überleben im Vergleich zu Kontrolltieren mit Scheineingriff verlängert wird. In H-69-Xenografts induziert diese Chemikalie bei 50 % der Mäuse vollständige Remissionen, die >6 Monate andauern. Diese Effekte korrelieren mit einer erhöhten Apoptose in exzidierten Tumoren, sind aber keine Folge einer gestörten Tumorgefäßversorgung. |
Protokoll (aus Referenz)
| Kinase-Assay:[1] |
|
|---|---|
| Zell-Assay:[4] |
|
| Tierstudie:[1] |
|
Referenzen
|
Kundenproduktvalidierung
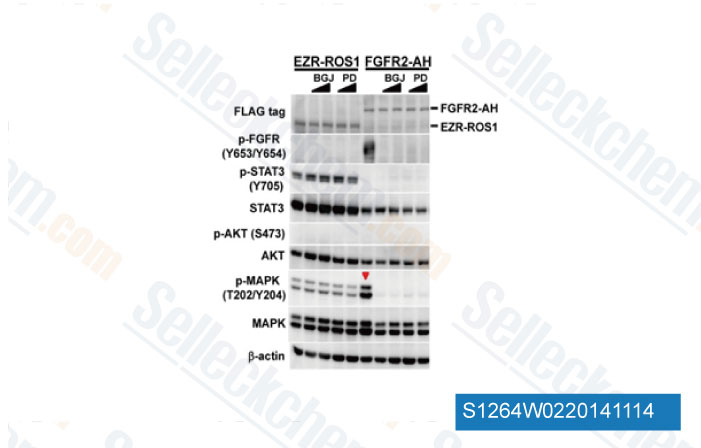
-
Daten von [ Hepatology , 2014 , 59(4) ,1427-34 ]
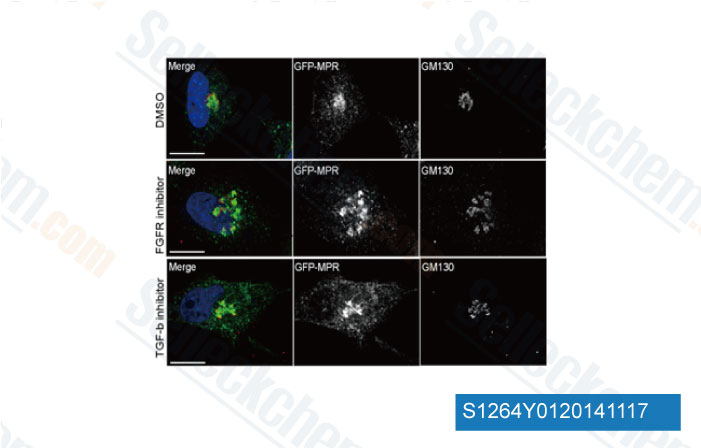
-
Daten von [ J Cell Sci , 2014 , 10.1242/jcs.159608 ]
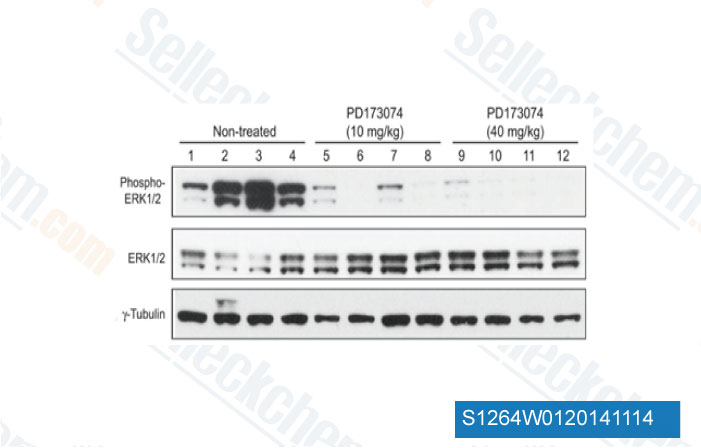
-
Daten von [ Cancer Discov , 2013 , 3(6), 636-47 ]

-
Daten von [ PLoS Genet , 2012 , 8(2), e1002500 ]
Sellecks PD173074 Wurde zitiert von 127 Publikationen
| Signaling pathway-based culture condition improves differentiation potential of canine induced pluripotent stem cells [ Stem Cell Reports, 2025, 20(10):102640] | PubMed: 40972586 |
| NLRP7 maintains the genomic stability during early human embryogenesis via mediating alternative splicing [ Commun Biol, 2025, 8(1):125] | PubMed: 39865169 |
| Modeling the atrioventricular conduction axis using human pluripotent stem cell-derived cardiac assembloids [ Cell Stem Cell, 2024, S1934-5909(24)00294-7] | PubMed: 39260368 |
| Chimerization of human ESC-derived extraembryonic cells with the mouse blastocyst [ Int J Biol Sci, 2024, 20(13):5056-5069] | PubMed: 39430245 |
| FGF receptors mediate cellular senescence in the cystic fibrosis airway epithelium [ JCI Insight, 2024, 9(15)e174888] | PubMed: 38916962 |
| PP2 suppresses proliferation and migration of C6 Glioma and MDA-MB-231 cells by targeting both fibroblast growth factor receptor 1 and Src [ Chem Biol Interact, 2024, 403:111252] | PubMed: 39341487 |
| Smad4 is essential for epiblast scaling and morphogenesis after implantation, but nonessential before implantation [ Development, 2024, 151(11)dev202377] | PubMed: 38752427 |
| Smad4 is essential for epiblast scaling and morphogenesis after implantation, but nonessential prior to implantation in the mouse [ bioRxiv, 2024, 2024.01.23.576717] | PubMed: 38328075 |
| FGF21 increases the sensitivity of sorafenib to hepatocellular carcinoma under hypoxia [ Malignancy Spectrum, 2024, 10.1002/msp2.20] | PubMed: none |
| Dietary phosphorus consumption alters T cell populations, cytokine production, and bone volume in mice [ JCI Insight, 2023, 8(10)e154729] | PubMed: 37079375 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
