Technische Daten
| Formel | C17H14ClF2N3O3S |
||||||
| Molekulargewicht | 413.83 | CAS-Nr. | 918505-84-7 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 83 mg/mL (200.56 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | PLX4720 ist ein potenter und selektiver Inhibitor von B-RafV600E mit einer IC50 von 13 nM in einem zellfreien Assay, ebenso potent wie c-Raf-1 (Y340D- und Y341D-Mutationen), 10-fache Selektivität für B-RafV600E gegenüber Wildtyp-B-Raf. | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Ziele |
|
||||||||
| In vitro | PLX-4720 zeigt eine über 10-mal höhere Selektivität gegenüber Wildtyp-B-Raf und eine über 100-mal höhere Selektivität gegenüber anderen Kinasen wie Frk, Src, Fak, FGFR und Aurora A mit einer IC50 von 1,3–3,4 μM. Diese Verbindung hemmt signifikant die ERK-Phosphorylierung in Zelllinien mit B-RafV600E mit einer IC50 von 14–46 nM, jedoch nicht in Zellen mit Wildtyp-B-Raf. Sie hemmt signifikant das Wachstum von Tumorzelllinien, die das B-RafV600E-Onkogen tragen, wie COLO205, A375, WM2664 und COLO829 mit einer GI50 von 0,31 μM, 0,50 μM, 1,5 μM bzw. 1,7 μM. Darüber hinaus induziert diese chemische Behandlung bei 1 μM einen Zellzyklusarrest und Apoptose ausschließlich in den B-RafV600E-positiven 1205Lu-Zellen, nicht aber in den B-Raf-Wildtyp-C8161-Zellen. Diese Verbindung (10 μM) induziert signifikant eine >14-fache Expression von BIM in den PTEN+-Zellen im Vergleich zu den PTEN--Zelllinien (4-fach), was eine Erklärung für die Resistenz von PTEN--Zellen gegenüber dieser chemisch induzierten Apoptose liefert. | ||||||||
| In vivo | Die orale Verabreichung von PLX-4720 in einer Dosis von 20 mg/kg/Tag führt zu signifikanten Tumorwachstumsverzögerungen und -regressionen in B-RafV600E-abhängigen COLO205-Tumorxenograften, ohne offensichtliche Nebenwirkungen bei Mäusen, selbst bei einer Dosis von 1 g/kg. Diese Verbindung in einer Dosis von 100 mg/kg zweimal täglich eliminiert fast vollständig die 1205Lu-Xenografts mit B-RafV600E, während sie keine Aktivität gegen C8161-Xenografts mit Wildtyp-B-Raf aufweist. Die Antitumorwirkungen dieser Verbindung korrelieren mit der Blockade des MAPK-Signalwegs in jenen Zellen, die die V600E-Mutation aufweisen. Diese chemische Behandlung in einer Dosis von 30 mg/kg/Tag hemmt signifikant das Tumorwachstum von 8505c-Xenografts um >90 % und verringert dramatisch die Fernmetastasen in der Lunge. |
Protokoll (aus Referenz)
| Kinase-Assay:[1] |
|
|---|---|
| Zell-Assay:[1] |
|
| Tierstudie:[1] |
|
Referenzen
|
Kundenproduktvalidierung
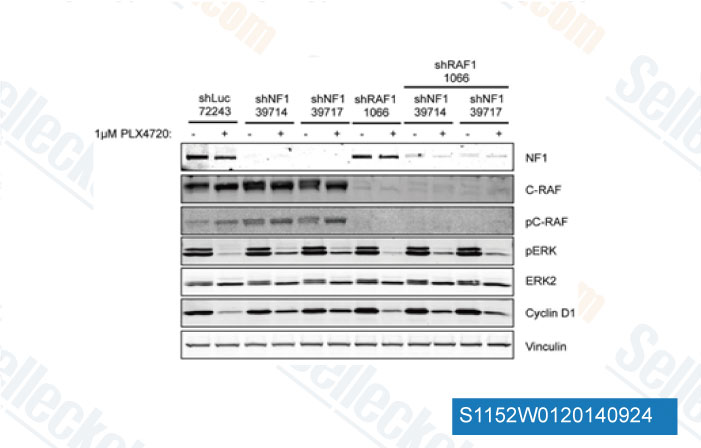
-
Daten von [ Cancer Discov , 2013 , 3, 350-62 ]
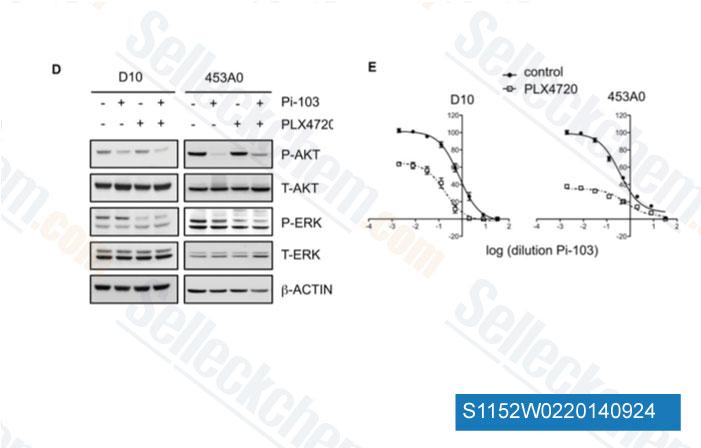
-
Daten von [ Genes Dev , 2012 , 26, 1055-69 ]
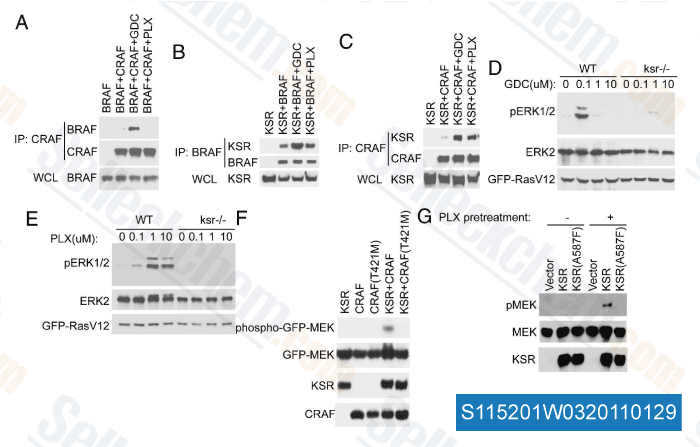
-
Daten von [ Proc Natl Acad Sci USA , 2011 , 108, 6067-6072 ]
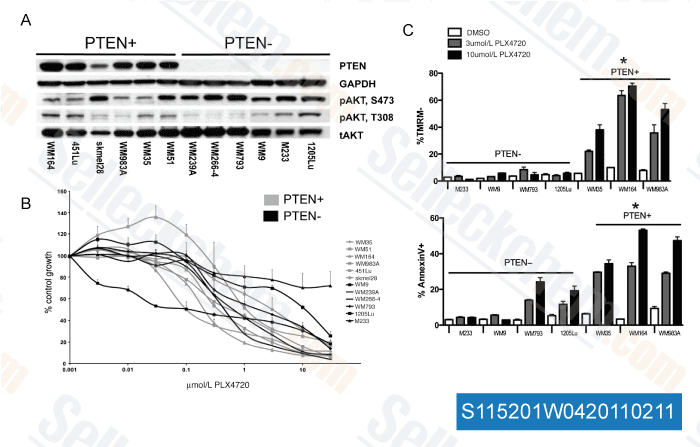
-
Daten von [ Cancer Res , 2011 , 71, 2750-2760 ]
Sellecks PLX-4720 Wurde zitiert von 206 Publikationen
| Elevated NR2F1 underlies the persistence of invasive disease after treatment of BRAF-mutant melanoma [ J Clin Invest, 2025, 135(18)e178446] | PubMed: 40955663 |
| Elevated Transglutaminase-2 in SOX10-Deficient Melanoma Promotes Tumor Onset and Decreases Intratumoral CD4+ T Cells [ Cancer Res, 2025, 10.1158/0008-5472.CAN-24-3267] | PubMed: 40742313 |
| PTRF Confers Melanoma-Acquired Drug Resistance Through the Upregulation of EGFR [ Cell Prolif, 2025, e70086.] | PubMed: 40745979 |
| A functional comparison of two transplantable syngeneic mouse models of melanoma: B16F0 and YUMM1.7 [ Biol Open, 2025, 14(9)bio062175] | PubMed: 40878826 |
| Noncanonical role of Golgi-associated macrophage TAZ in chronic inflammation and tumorigenesis [ Sci Adv, 2025, 11(4):eadq2395] | PubMed: 39841821 |
| The ribotoxic stress response drives UV-mediated cell death [ Cell, 2024, 187(14):3652-3670.e40] | PubMed: 38843833 |
| Tracking the EMT-like phenotype switching during targeted therapy in melanoma by analyzing extracellular vesicle phenotypes [ Biosens Bioelectron, 2024, 10.1016/j.bios.2023.115819] | PubMed: 37952322 |
| Mcl-1 mediates intrinsic resistance to RAF inhibitors in mutant BRAF papillary thyroid carcinoma [ Cell Death Discov, 2024, 10(1):175] | PubMed: 38622136 |
| The ERK5 pathway in BRAFV600E melanoma cells plays a role in development of acquired resistance to dabrafenib but not vemurafenib [ FEBS Lett, 2024, 10.1002/1873-3468.14960] | PubMed: 38977937 |
| Executioner caspases restrict mitochondrial RNA-driven Type I IFN induction during chemotherapy-induced apoptosis [ Nat Commun, 2023, 14(1):1399] | PubMed: 36918588 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
