Technische Daten
| Formel | C24H22O6 |
||||||
| Molekulargewicht | 406.43 | CAS-Nr. | 914913-88-5 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 81 mg/mL (199.29 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Palomid 529 (P529, SG 00529) hemmt sowohl die mTORC1- als auch die mTORC2-Komplexe und reduziert die Phosphorylierung von pAktS473, pGSK3βS9 und pS6. Diese Verbindung befindet sich in Phase 1. | ||
|---|---|---|---|
| Ziele |
|
||
| In vitro | Palomid 529 (P529) hemmt die Proliferation und erhöht die Apoptose von Endothelzellen, wobei sowohl die VEGF-getriebene als auch die bFGF-getriebene Endothelzellproliferation mit einer IC50 von 20 nM bzw. 30 nM gehemmt wird. Es behält die Fähigkeit bei, die Apoptose von Endothelzellen zu induzieren und die VEGF-A-getriebene Phosphorylierung von pAktS473, pGSK3βS9 und pS6 zu verringern. Dieses Compound verhindert jedoch weder die phosphorylierte Mitogen-aktivierte Proteinkinase (pMAPK) noch pAktT308 so potent wie pAktS473. Es reduziert nicht nur die proliferative Reaktion in der ischämischen Netzhaut, sondern verbessert auch die Organisation und Struktur der sich bildenden Gefäße. P529 zeigt eine potente antiproliferative Aktivität im NCI-60-Zelllinien-Panel, mit einer wachstumshemmenden 50 (GI50) <35 μM. Darüber hinaus verstärkt es signifikant die antiproliferative Wirkung der Strahlung in Prostatakrebszellen (PC-3), was zu einer konzentrationsabhängigen Wachstumshemmung der PC-3-Zellen führt. Dosen von 2 und 7 μM führten zu einer Wachstumshemmung von 30 bzw. 60 %. Es hemmt die strahleninduzierte p-Akt-Aktivierung und verringert das Bcl-2/Bax-Verhältnis in PC-3. Dieses Compound hemmt nicht nur die strahleninduzierte Überexpression von Id-1 und VEGF, sondern reguliert auch die strahleninduzierte MMP-2 und MMP-9 herunter. |
||
| In vivo | Palomid 529 (P529) zeigt nach seiner Behandlung eine dosisabhängige Hemmung der Ad-VEGF-A-getriebenen Angiogenese. Es hemmt das Wachstum von C6V10-Gliom-Tumoren in Nacktmäusen nach i.p.-Gabe und verringert die AktS473-, aber nicht die AktT308-Signalübertragung. Diese Verbindung hemmt auch das Tumorwachstum, die Angiogenese und die vaskuläre Permeabilität. Die Behandlung von PC-3-Tumor tragenden Mäusen damit reduzierte das Tumorwachstum im Vergleich zu Kontrollen um 57,1 %. Es ist ein wirksamer Suppressor der Müller-Zellproliferation, der Glianarbenbildung und des Photorezeptorzelltods in einem Kaninchenmodell der Netzhautablösung (RD). Palomid 529 unterdrückt signifikant das Wachstum Brca1-defizienter Tumoren in Mäusen durch Hemmung sowohl der Akt- als auch der mTOR-Signalübertragung. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
Referenzen
|
Kundenproduktvalidierung
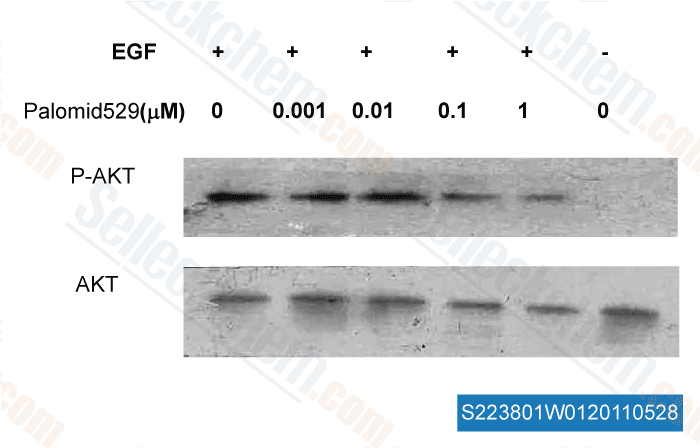
-
, , Dr. Zhang of Tianjin Medical University
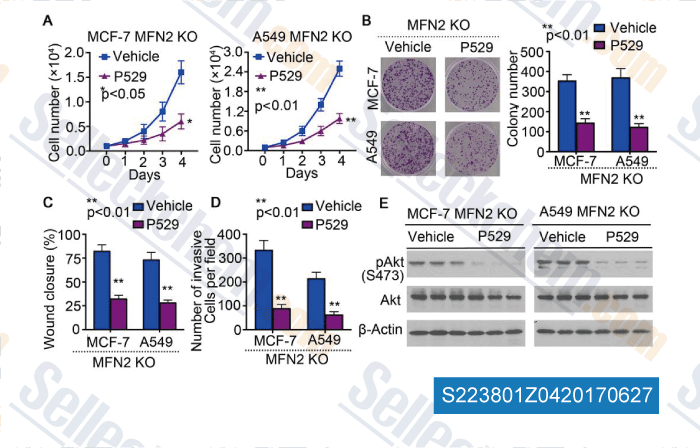
-
Daten von [ , , Sci Rep, 2017, 7:41718 ]
Sellecks Palomid 529 (P529) Wurde zitiert von 8 Publikationen
| Neuroimmune Microenvironment Reprogramming via Immuno-piezoelectric Transducers for Synergistic Stem Cell Therapy in Traumatic Brain Injury [ Adv Mater, 2025, e12810.] | PubMed: 41030193 |
| γ-catenin alleviates cardiac fibrosis through inhibiting phosphorylation of GSK-3β. [ J Biomed Res, 2020, 0(0):1-9] | PubMed: 31741464 |
| MFN2 suppresses cancer progression through inhibition of mTORC2/Akt signaling. [Xu K, et al. Sci Rep, 2017, 7:41718] | PubMed: 28176801 |
| A Mechanism for Asymmetric Cell Division Resulting in Proliferative Asynchronicity. [Dey-Guha I, et al. Mol Cancer Res, 2015, 13(2):223-30] | |
| A mechanism for asymmetric cell division resulting in proliferative asynchronicity. [ Mol Cancer Res, 2015, 13(2):223-30] | PubMed: 25582703 |
| Deciphering Combinations of PI3K/AKT/mTOR Pathway Drugs Augmenting Anti-Angiogenic Efficacy In Vivo [Sasore T, et al PLoS One, 2014, 9(8):e105280] | PubMed: 25144531 |
| LKB1 Loss at Transcriptional Level Promotes Tumor Malignancy and Poor Patient Outcomes in Colorectal Cancer. [He TY, et al. Ann Surg Oncol, 2014, 10.1245/s10434-014-3824-1] | PubMed: 24879590 |
| Pharmacological profiling of phosphoinositide-3-kinase inhibitors as mitigators of ionizing radiation-induced cell death. [Lazo JS, et al. J Pharmacol Exp Ther, 2013, 347(3):669-80] | PubMed: 24068833 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
