Technische Daten
| Formel | C20H21FN6O5 |
||||||
| Molekulargewicht | 444.42 | CAS-Nr. | 518048-05-0 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 89 mg/mL (200.26 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Raltegravir ist ein potenter Integrase (IN)-Inhibitor für WT und S217Q PFV IN mit einer IC50 von 90 nM bzw. 40 nM in zellfreien Assays. Es zeigt eine mehr als 1000-fache Selektivität für HIV-1 IN gegenüber mehreren verwandten Mg2+-abhängigen Enzymen wie HCV-Polymerase, HIV-Reverse-Transkriptase, HIV RNaseH und menschlichen α-, β-, γ-Polymerasen. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | PFV IN, das die S217H-Substitution trägt, ist 10-fach weniger empfindlich gegenüber Raltegravir mit einer IC50 von 900 nM. PFV IN zeigt 10 % der WT-Aktivität und wird durch diese Verbindung mit einer IC50 von 200 nM gehemmt, was eine etwa zweifache Abnahme der Empfindlichkeit gegenüber dem IN strand transfer inhibitor (INSTI) im Vergleich zu WT IN anzeigt. S217Q PFV IN ist gegenüber dieser Verbindung genauso empfindlich wie das WT-Enzym. Es wird durch Glucuronidierung metabolisiert, nicht hepatisch. Diese Verbindung hat eine potente In-vitro-Aktivität gegen HIV-1 mit einer 95%igen Hemmkonzentration von 31?0 nM in humanen T-Lymphoidzellkulturen. Sie ist auch gegen HIV-2 aktiv, wenn sie in CEMx174-Zellen getestet wird, mit einer IC95 von 6 nM. Ihr Metabolismus erfolgt hauptsächlich durch Glucuronidierung. Arzneimittel, die starke Induktoren des Glucuronidierungsenzyms UGT1A1 sind, reduzieren ihre Konzentrationen erheblich und sollten nicht verwendet werden. Es zeigt schwache hemmende Wirkungen auf die hepatische Cytochrom-P450-Aktivität. Es induziert weder die CYP3A4-RNA-Expression noch die CYP3A4-abhängige Testosteron-6-β-Hydroxylase-Aktivität. Seine zelluläre Permeabilität ist in Gegenwart von Magnesium und Kalzium reduziert. Diese Verbindung und verwandte HIV-1 Integrase (IN) strand transfer inhibitors (INSTIs) blockieren effizient die virale Replikation. In akut infizierten humanen lymphatischen CD4+-T-Zelllinien MT-4 und CEMx174 wird die SIVmac251-Replikation durch diese Verbindung effizient gehemmt, die eine EC90 im niedrigen nanomolaren Bereich zeigt. | ||||
| In vivo | Raltegravir induziert eine viro-immunologische Verbesserung bei nicht-humanen Primaten mit fortschreitender SIVmac251-Infektion. Ein nicht-humaner Primat zeigt eine nicht nachweisbare Viruslast nach dieser Verbindung als Monotherapie. | ||||
| Merkmale | Der erste zugelassene human immunodeficiency virus type 1 (HIV-1) Integrase Inhibitor. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
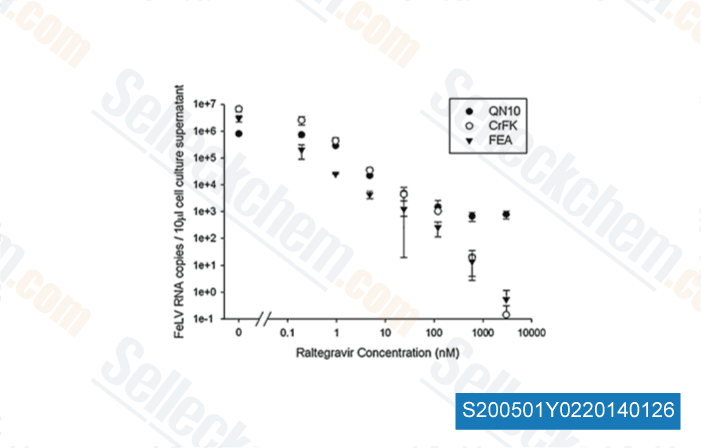
-
Daten von [ Vet Microbiol , 2011 , 152(1-2), 165-8 ]
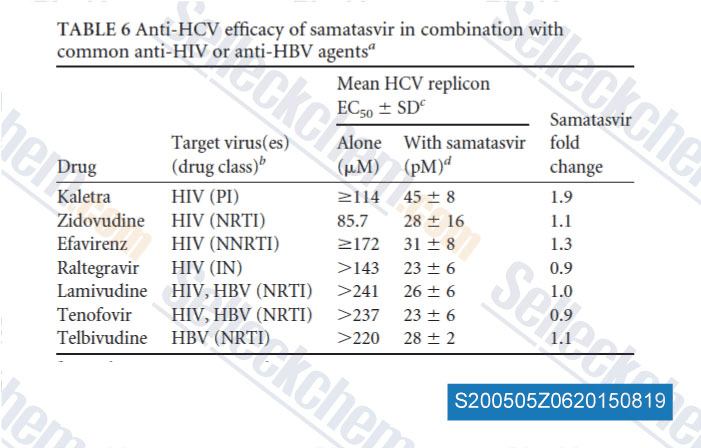
-
Daten von [ , , Antimicrob Agents Chemother, 2014, 58(8): 4431-42 ]
Sellecks Raltegravir Wurde zitiert von 76 Publikationen
| The macrophage-intrinsic MDA5/IRF5 axis drives HIV-1 intron-containing RNA-induced inflammatory responses [ J Clin Invest, 2025, 135(16)e187663] | PubMed: 40493408 |
| Pomalidomide enhances CD8+ T and NK cell mediated killing of HIV-infected cells [ EBioMedicine, 2025, 122:106004] | PubMed: 41232235 |
| Combined dendritic cell and anti-TIGIT immunotherapy potentiates adaptive NK cells against HIV-1 [ EMBO Mol Med, 2025, 10.1038/s44321-025-00255-x] | PubMed: 40473838 |
| Targeting Ikaros and Aiolos with pomalidomide fails to reactivate or induce apoptosis of the latent HIV reservoir [ J Virol, 2025, e0167624.] | PubMed: 39902962 |
| Limitations and use of the Morpheus-V5 dual reporter virus in assessing interventions that target HIV latency [ J Virol Methods, 2025, 338:115236] | PubMed: 40754007 |
| 5' cap sequestration is required for sensing of unspliced HIV-1 RNA by MDA5 [ bioRxiv, 2025, 2025.08.20.671346] | PubMed: 40909469 |
| IKAROS expression drives the aberrant metabolic phenotype of macrophages in chronic HIV infection [ Clin Immunol, 2024, 260:109915] | PubMed: 38286172 |
| Broad synergistic antiviral efficacy between a novel elite controller-derived dipeptide and antiretrovirals against drug-resistant HIV-1 [ Front Cell Infect Microbiol, 2024, 14:1334126] | PubMed: 38915925 |
| HMGB1 Expression Levels Correlate with Response to Immunotherapy in Non-Small Cell Lung Cancer [ Lung Cancer, 2024, 15:55-67] | PubMed: 38741920 |
| Conversion of raltegravir carrying a 1,3,4-oxadiazole ring to a hydrolysis product upon pH changes decreases its antiviral activity [ PNAS Nexus, 2024, 3(1):pgad446] | PubMed: 38170115 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
