Technische Daten
| Formel | C13H16N6O4 |
||||||||||
| Molekulargewicht | 320.3 | CAS-Nr. | 35943-35-2 | ||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 64 mg/mL (199.81 mM) | ||||||||
| Ethanol | 16 mg/mL (49.95 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Triciribine (API-2) ist ein DNA synthesis Inhibitor, der auch Akt in der PC3-Zelllinie und HIV-1 in CEM-SS-, H9-, H9IIIB-, U1-Zellen mit einer IC50 von 130 nM bzw. 20 nM hemmt; es hemmt nicht PI3K/PDK1 und ist 5000-fach weniger aktiv in Zellen, denen die Adenosin-Kinase fehlt. Phase 1/2. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | Triciribine (API-2) zeigt eine maximale Wachstumshemmung bei etwa 1-10 μM und hemmt die Phosphorylierung von Akt sowie von nachgeschaltetem p70S6K bis auf Basalniveaus bei 100μM (IC50 = 130 nM). Es zeigt besonderes Potenzial zur Hemmung des Wachstums in Nf1- und Trp53-mutanten Astrozytomzellen in einer gradabhängigen Weise. Die WHO II K1861-10 Linie wird unvollständig (69% maximale Hemmung) mit einem GI50-Wert von 1,7 μM für diese Verbindung gehemmt, während höhergradige Tumorlinien (KR158, KR130 und SF295) in größerem Maße (>80% maximale Hemmung) bei niedrigeren GI50-Werten (0,4–1,1 mM) gehemmt werden. Wichtig ist, dass es viel weniger wirksam bei der Hemmung primärer Astrozyten ist (GI5013,6 mM), was darauf hindeutet, dass dieser Inhibitor Spezifität für Tumorzellen zeigen könnte. Es hemmt HIV-1 mit einer IC50 von 20 nM. Eine Hemmung von mehr als 90% wird bei 0,1μM erreicht, und eine vollständige Hemmung der Synzytienbildung wird bei 5μM erreicht. Die assoziierte Zelltoxizität in derselben Zelllinie für Triciribine beträgt 46 μM, was zu Selektivitätsindizes von 2250 führt. Es hemmt deutlich die HIV-1-induzierte p24-Core-Antigenproduktion, Reverse Transkriptase und infektiöse Virusproduktion in einer dosisabhängigen Weise unter Verwendung von HIV-1-akut infizierten CEM-SS-, H9- und persistent infizierten H9IIIB- und U1-Zellen. Diese Verbindung hemmt die Akt-Phosphorylierung an Thr308 und Ser473 und die Akt-Aktivität in der menschlichen Prostatakrebs-Zelllinie PC-3. Sie sensibilisiert PC-3-Zellen für TRAIL- und Anti-CD95-induzierte Apoptose, während die Zellen gegenüber DNA-schädigenden Chemotherapeutika resistent bleiben. Es ist hochselektiv für Akt und hemmt nicht die Aktivierung von Phosphatidylinositol-3-Kinase, Phosphoinositid-abhängiger Kinase-1, Proteinkinase C, Serum- und Glukokortikoid-induzierbarer Kinase, Proteinkinase A, Signaltransduktor und Aktivatoren von Transkription 3, extrazellulär signalregulierter Kinase-1/2 oder c-Jun NH2-terminaler Kinase. | ||||
| In vivo | Triciribine (API-2), verabreicht bei 1 mg/kg/Tag i.p., hemmt das Tumorwachstum um 90%, 88% und 80% in Nacktmäusen mit OVCAR3-, OVCAR8- und PANC1-Tumoren, die Akt überexprimieren. Diese Verbindung hat jedoch wenig Einfluss auf das Wachstum von OVCAR5- und COLO357-Zellen. |
Protokoll (aus Referenz)
| Kinase-Assay:[1] |
|
|---|---|
| Zell-Assay:[2] |
|
| Tierstudie:[4] |
|
Referenzen
|
Kundenproduktvalidierung
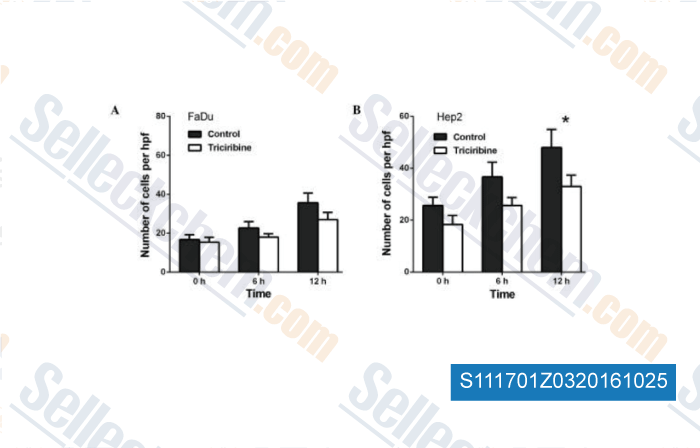
-
, , Oncol Lett, 2016, 11(3):1889-1894.
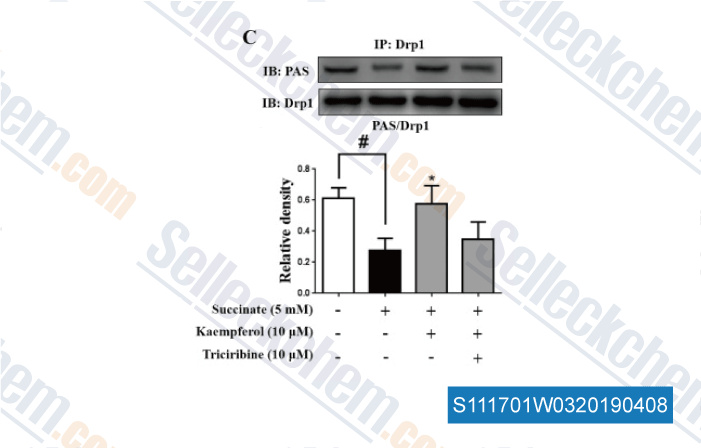
-
Daten von [ , , Biochim Biophys Acta Mol Basis Dis, 2017, 1863(9):2307-2318 ]
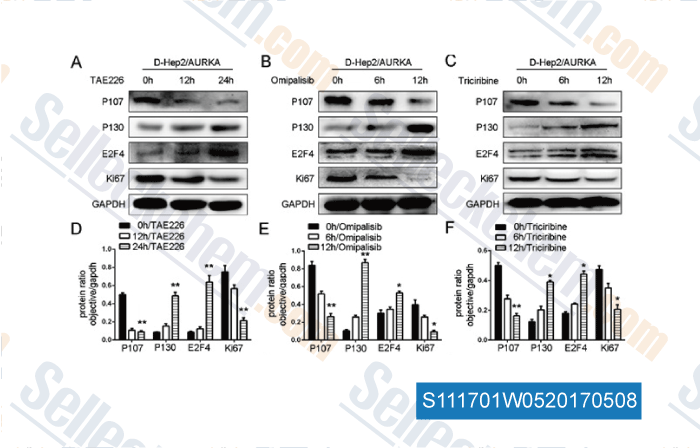
-
Daten von [ , , Oncotarget, 2016, 7(30):48346-48359 ]
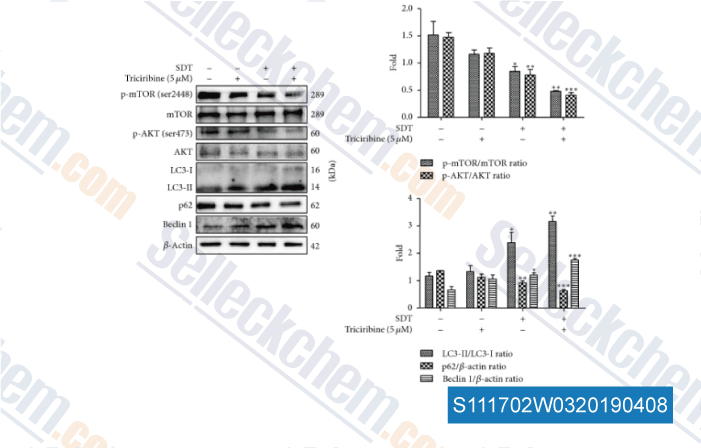
-
Daten von [ , , Oxid Med Cell Longev, 2017, 2017:8519169 ]
Sellecks Triciribine (API-2) Wurde zitiert von 94 Publikationen
| βIV spectrin abundancy, cellular distribution and sensitivity to AKT/GSK3 regulation in schizophrenia [ Mol Psychiatry, 2025, 10.1038/s41380-025-02917-1] | PubMed: 39920295 |
| Dual inhibition of AKT and autophagy sensitizes triple negative breast cancer cells to carboplatin [ Transl Oncol, 2025, 58:102434] | PubMed: 40450899 |
| Lamin A/C phosphorylation at serine 22 is a conserved heat shock response to regulate nuclear adaptation during stress [ J Cell Sci, 2023, 136(4)jcs259788] | PubMed: 36695453 |
| Functional restoration of lysosomes and mitochondria through modulation of AKT activity ameliorates senescence [ Exp Gerontol, 2023, 173:112091] | PubMed: 36657533 |
| Regulation of miRNA expression by α4β1 integrin-dependent multiple myeloma cell adhesion [ EJHaem, 2023, 4(3):631-638] | PubMed: 37601846 |
| CREB3L1 promotes tumor growth and metastasis of anaplastic thyroid carcinoma by remodeling the tumor microenvironment [ Mol Cancer, 2022, 21(1):190] | PubMed: 36192735 |
| Disruption of the IL-33-ST2-AKT signaling axis impairs neurodevelopment by inhibiting microglial metabolic adaptation and phagocytic function [ Immunity, 2022, 55(1):159-173.e9] | PubMed: 34982959 |
| Anionic nanoplastic exposure induces endothelial leakiness [ Nat Commun, 2022, 13(1):4757] | PubMed: 35963861 |
| DENR controls JAK2 translation to induce PD-L1 expression for tumor immune evasion [ Nat Commun, 2022, 13(1):2059] | PubMed: 35440133 |
| CRISPR/Cas9 Screens Reveal that Hexokinase 2 Enhances Cancer Stemness and Tumorigenicity by Activating the ACSL4-Fatty Acid β-Oxidation Pathway [ Adv Sci (Weinh), 2022, 9(21):e2105126] | PubMed: 35603967 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
