Technische Daten
| Formel | C24H25FO5S |
||||||
| Molekulargewicht | 444.52 | CAS-Nr. | 842133-18-0 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 89 mg/mL (200.21 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Canagliflozin (TA 7284, JNJ 28431754) ist ein hochwirksamer und selektiver SGLT2-Inhibitor für hSGLT2 mit einer IC50 von 2,2 nM in einem zellfreien Assay und weist eine 413-fache Selektivität gegenüber hSGLT1 auf. | ||||||
|---|---|---|---|---|---|---|---|
| Ziele |
|
||||||
| In vitro | Canagliflozin (JNJ 28431754) ist ein neuartiges C-Glucosid mit Thiophenring. Es hemmt die Na+-abhängige 14C-AMG-Aufnahme konzentrationsabhängig. Diese Verbindung hemmt die 14C-AMG-Aufnahme in CHO-hSGLT1- und mSGLT1-Zellen mit einer IC50 von 0,7 μM bzw. >1 μM. Es hemmt die erleichterte (nicht-Na+-gebundene) GLUT-vermittelte 2H-2-DG-Aufnahme in L6-Myoblasten um weniger als 50%. In schein-injizierten Oozyten beeinflusst Canagliflozin (10 μM) oder Phlorizin (3 mM) allein in Gegenwart von 50 μM DNJ keine Ströme. In SGLT3-injizierten Oozyten hemmen DMSO und Canagliflozin 10 μM die DNJ-induzierten Ströme um 15,6% bzw. 23,4%. | ||||||
| In vivo | Canagliflozin (JNJ 28431754) zeigt ausgeprägte anti-hyperglykämische Effekte bei KK-Mäusen (HF-KK), die mit einer fettreichen Diät gefüttert wurden. Die orale Verabreichung dieser Verbindung in einer Dosis von 30 mg/kg an männliche SD-Ratten führt zu einer Glukoseausscheidung über 24 Stunden von 3.696 mg pro 200 g Körpergewicht. Pharmakokinetische Studien zeigen eine wesentlich höhere Exposition nach oraler Verabreichung. Nach intravenöser und oraler Dosen von 3 bzw. 10 mg/kg an männliche SD-Ratten wurden AUC0−inf, po, t1/2 und die orale Bioverfügbarkeit auf 35.980 ng·h/mL, 5,2 Stunden bzw. 85% bestimmt. Somit dürfte die Hemmung von SGLT2 in den Nierentubuli nach oraler Gabe die Rückresorption von Glukose kontinuierlich unterdrücken. Die umfangreiche UGE würde ausgezeichnete pharmakokinetische Eigenschaften in vivo sowie eine hohe Potenz der SGLT2-Hemmung widerspiegeln. Da der größte Teil der filtrierten Glukose durch SGLT2 in den Nierentubuli rückresorbiert wird, wäre die neuartige Verbindung als Antidiabetikum nützlich. Eine einmalige orale Verabreichung von 3 mg/kg reduzierte die Blutzuckerwerte bei hyperglykämischen KK-Mäusen (HF-KK), die mit einer fettreichen Diät gefüttert wurden, signifikant, ohne die Nahrungsaufnahme zu beeinflussen. Es gab eine 48%ige Reduktion des Blutzuckerspiegels im Vergleich zum Vehikel nach 6 Stunden. Im Gegensatz dazu beeinflusst es die Blutzuckerwerte bei normoglykämischen Mäusen nur geringfügig. Daher würde Canagliflozin die Hyperglykämie bei der Therapie von T2DM mit geringem Hypoglykämie-Risiko kontrollieren. |
Protokoll (aus Referenz)
| Zell-Assay:[1] |
|
|---|---|
| Tierstudie:[2] |
|
Referenzen
|
Kundenproduktvalidierung

-
Daten von [ , , Mol Metab, 2016, 5(10):1048-56 ]
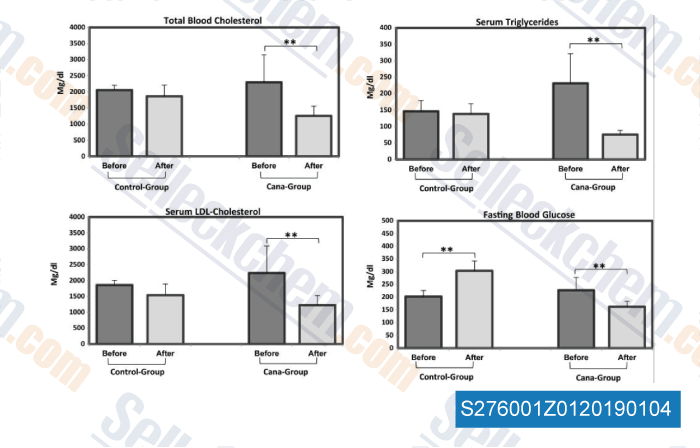
-
Daten von [ , , Cardiovasc Diabetol, 2018, 17(1):106 ]
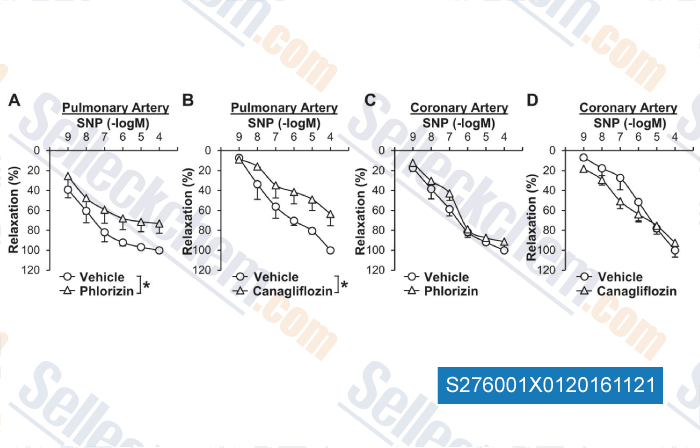
-
Daten von [ , , Am J Physiol Lung Cell Mol Physiol, 2015, 309(9):L1027-36. ]
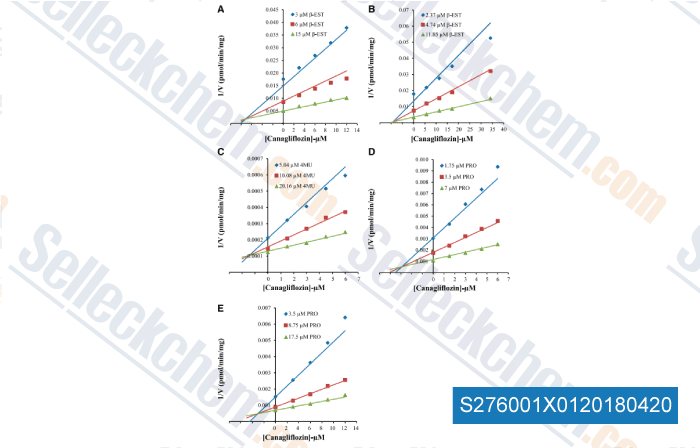
-
Daten von [ , , Drug Metab Dispos, 2015, 43(10):1468-76. ]
Sellecks Canagliflozin (JNJ-28431754) Wurde zitiert von 34 Publikationen
| Nuclear translocation of metabolic enzyme PKM2 participates in high glucose-promoted HCC metastasis by strengthening immunosuppressive environment [ Redox Biol, 2024, 71:103103] | PubMed: 38471282 |
| Canagliflozin reverses doxorubicin-induced cardiotoxicity via restoration of autophagic homeostasis [ Toxicol Appl Pharmacol, 2024, 495:117183] | PubMed: 39631538 |
| Canagliflozin primes antitumor immunity by triggering PD-L1 degradation in endocytic recycling [ J Clin Invest, 2023, 133(1)e154754] | PubMed: 36594471 |
| Canagliflozin ameliorates hypobaric hypoxia-induced pulmonary arterial hypertension by inhibiting pulmonary arterial smooth muscle cell proliferation [ Clin Exp Hypertens, 2023, 10.1080/10641963.2023.2278205] | PubMed: 37970663 |
| The impact of SGLT2 inhibitors on αKlotho in renal MDCK and HK-2 cells [ Front Endocrinol (Lausanne), 2023, 14:1069715] | PubMed: 36967770 |
| Study on the pharmacological mechanisms of sodium-glucose co-transporter 2 inhibitors in obesity-related atrial fibrillation based on network pharmacology and experimental verification [ Ann Transl Med, 2023, 11(8):300] | PubMed: 37181345 |
| Systematic identification of biomarker-driven drug combinations to overcome resistance [ Nat Chem Biol, 2022, 10.1038/s41589-022-00996-7] | PubMed: 35332332 |
| SGLT2 inhibitor activates the STING/IRF3/IFN-β pathway and induces immune infiltration in osteosarcoma [ Cell Death Dis, 2022, 13(6):523] | PubMed: 35662245 |
| Multi-site desmoplastic small round cell tumors are genetically related and immune-cold [ Cell Mol Life Sci, 2022, 79(5):273] | PubMed: 35503137 |
| Anti-inflammatory effect of SGLT-2 inhibitors viauric acidand insulin [ Cellular and Molecular Life Sciences, 2022, 273] | PubMed: None |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
