Technische Daten
| Formel | C21H28BN3O5 |
||||||||||||||
| Molekulargewicht | 413.28 | CAS-Nr. | 847499-27-8 | ||||||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 83 mg/mL (200.83 mM) | ||||||||||||
| Ethanol | 83 mg/mL (200.83 mM) | ||||||||||||||
| Water | Insoluble | ||||||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Delanzomib ist ein oral aktiver Inhibitor der Chymotrypsin-ähnlichen Aktivität des Proteasome mit einer IC50 von 3,8 nM, mit nur geringer Hemmung der tryptischen und Peptidylglutamyl-Aktivitäten des Proteasome. Phase 1/2. | ||
|---|---|---|---|
| Ziele |
|
||
| In vitro | CEP-18770 zeigt eine geringfügige Prävention der tryptischen und peptidyl-glutamylen Aktivitäten des Proteasome. CEP-18770 hemmt A2780-Ovarialkarzinomzellen, PC3-Prostatakrebs, H460, LoVo-Darmkrebs, RPMI8226-multiples Myelom und HS-Sultan-anaplastisches Non-Hodgkin-Lymphom mit IC50-Werten von 13,7, 22,2, 34,2, 11,3, 5,6 und 8,2 nM. CEP-18770 blockiert den Ubiquitin-Proteasome-Weg in mehreren MM und in der chronisch myeloischen Leukämiezelllinie K562. CEP-18770 führt zu einer Akkumulation von ubiquitinierten Proteinen über 4 bis 8 Stunden. Die IκBα-Degradation wird durch Vorbehandlung mit CEP-18770 vollständig blockiert. CEP-18770 hemmt signifikant hohe NF-κB-Aktivitätswerte sowohl in RPMI-8226- als auch in U266-Zellen. Die zeit- und konzentrationsabhängige Suppression der NF-kB-DNA-Bindungsaktivität in MM-Zelllinien durch CEP-18770 führt zu einer Abnahme der Expression mehrerer NF-κB-modulierter Gene, die das Wachstum und Überleben von Tumorzellen vermitteln, einschließlich IkBα selbst, des X-chromosomal-gebundenen Inhibitor-of-Apoptosis-Proteins (XIAP), der proinflammatorischen Zytokine TNF-α und Interleukin-1β (IL-1β), des intrazellulären Adhäsionsmoleküls (ICAM1) und des pro-angiogenen Faktors vaskulärer endothelialer Wachstumsfaktor. Die Expression dieser NF-κB-vermittelten Gene ist mit einer günstigeren klinischen Reaktion auf dieses Mittel verbunden, was ihren potenziellen prognostischen Wert bei der Reaktion auf CEP-18770-Exposition unterstreicht. Die proapoptotische Aktivität von CEP-18770 gegen MM ist nicht allein auf Tumorzelllinien des MM beschränkt, sondern erstreckt sich auch auf primäre MM-Explante von Patienten mit Rezidiven oder refraktären Erkrankungen. Darüber hinaus führt CEP-18770 in Kombination zu einer synergistischen Hemmung der MM-Zellviabilität in vitro. |
||
| In vivo | CEP-18770 zeigt eine anhaltende dosisabhängige relative Tumorgewichtsinhibition. CEP-18770 führt zu dosisabhängigen vollständigen Tumorregressionen, was zu einer 50%igen Inzidenz von CR bei seiner maximal verträglichen Dosis (MTD) von 1,2 mg/kg intravenös führt. CEP-18770 zeigt eine dosisabhängige Zunahme der Inzidenz von tumorfreien Mäusen bis zum Abschluss dieser Studien (120 Tage nach Tumortransplantation). Die orale Verabreichung von CEP-18770 führt zu einer deutlichen Abnahme des Tumorgewichts und einer bemerkenswerten dosisabhängigen Inzidenz vollständiger Tumorregression mit minimalen Änderungen des Tierkörpergewichts im Verlauf der 120-Tage-Studien. Equiactive Dosen von CEP-18770 zeigen eine größere und anhaltendere dosisabhängige Hemmung der Tumor-Proteasome-Aktivität, die zeitlich mit der maximalen Induktion der Caspase-3- und 7-Aktivität korrespondiert. Das maximale apoptotische Signal ist für CEP-18770 2,5-fach größer. Im Gegensatz dazu sind die Proteasome-Inhibitionsprofile von CEP-18870 in den untersuchten normalen peripheren Mausgeweben (Leber, Lunge, Vollblut und Gehirn [keine Aktivität]) sowohl in ihrer Größe als auch in ihrer Dauer vergleichbar. Zu keinem Zeitpunkt wurde in Gehirngewebe eine Proteasome-Inhibition für CEP-18770 oder festgestellt. Einzelwirkstoff CEP-18770 PO zeigt auch deutliche Anti-MM-Effekte in diesen Xenograft-Modellen |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
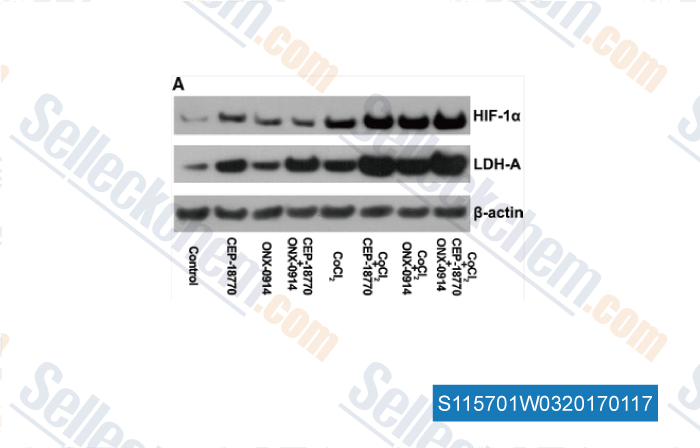
-
Daten von [ , , Int Urol Nephrol, 2016, 48(6):907-15. ]
Sellecks Delanzomib Wurde zitiert von 18 Publikationen
| A patient-derived T cell lymphoma biorepository uncovers pathogenetic mechanisms and host-related therapeutic vulnerabilities [ Cell Rep Med, 2025, S2666-3791(25)00102-8] | PubMed: 40147445 |
| Inhibitors of the ubiquitin‑proteasome system rescue cellular levels and ion transport function of pathogenic pendrin (SLC26A4) protein variants [ Int J Mol Med, 2025, 55(5)69] | PubMed: 40052591 |
| Slt2 Is Required to Activate ER-Stress-Protective Mechanisms through TORC1 Inhibition and Hexosamine Pathway Activation [ J Fungi (Basel), 2022, 8(2)92] | PubMed: 35205847 |
| Oral Proteasomal Inhibitors Ixazomib, Oprozomib, and Delanzomib Upregulate the Function of Organic Anion Transporter 3 (OAT3): Implications in OAT3-Mediated Drug-Drug Interactions [ Pharmaceutics, 2021, 13(3)314] | PubMed: 33670955 |
| Crosstalk between HSPA5 arginylation and sequential ubiquitination leads to AKT degradation through autophagy flux. [ Autophagy, 2020, 10.1080/15548627.2020.1740529] | PubMed: 32164484 |
| Crosstalk between cardiomyocytes and noncardiomyocytes is essential to prevent cardiomyocyte apoptosis induced by proteasome inhibition [ Cell Death Dis, 2020, 11(9):783] | PubMed: 32951004 |
| A Patient-Derived Cell Atlas Informs Precision Targeting of Glioblastoma [ Cell Rep, 2020, 32(2):107897] | PubMed: 32668248 |
| Differential antitumor activity of compounds targeting the ubiquitin-proteasome machinery in gastrointestinal stromal tumor (GIST) cells. [ Sci Rep, 2020, 10(1):5178] | PubMed: 32198455 |
| Charge transfer reaction mechanisms of epoxyketone and boronated peptides at glassy carbon and boron doped diamond electrodes [ J Electroanal Chem (Lausanne), 2020, 878:114733] | PubMed: 33020701 |
| Proteasome Inhibition in Multiple Myeloma: Head-to-Head Comparison of Currently Available Proteasome Inhibitors. [ Cell Chem Biol, 2019, 26(3):340-351] | PubMed: 30612952 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
