Technische Daten
| Formel | C19H12ClN3O2 |
||||||
| Molekulargewicht | 349.77 | CAS-Nr. | 1009820-21-6 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 70 mg/mL (200.13 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Silmitasertib (CX-4945) ist ein potenter und selektiver Inhibitor von CK2 (Casein Kinase 2) mit einem IC50 von 1 nM in einem zellfreien Assay, obwohl es weniger potent gegen Flt3, Pim1 und CDK1 ist (in zellbasiertem Assay inaktiv). Diese Verbindung induziert Autophagy und fördert apoptosis. Phase 1/2. | ||
|---|---|---|---|
| Ziele |
|
||
| In vitro | Silmitasertib (CX-4945) ist selektiv für CK2, da es bei einer Konzentration von 0,5 M, die 500-fach höher ist als die IC50 von CK2, nur 7 der 238 Kinasen um mehr als 90 % hemmt. Obwohl diese Verbindung in zellfreien Systemen FLT3, PIM1 und CDK1 mit IC50-Werten von 35 nM, 46 nM bzw. 56 nM hemmt, ist eine Behandlung bei 10 M in zellbasierten funktionellen Assays gegen FLT3, PIM1 und CDK1 inaktiv. Es zeigt ein breites Spektrum an antiproliferativer Aktivität, und die Brustkrebszelllinien zeigen die größte Empfindlichkeit gegenüber Silmitasertib (CX-4945) mit EC50-Werten von 1,71-20,01 M. Die antiproliferative Aktivität von CX-4945 korreliert mit den CK2α mRNA- und Proteinspiegeln, aber nicht mit der katalytischen CK2α'-Untereinheit, der regulatorischen CK2β-Untereinheit und dem PI3K/Akt- oder PTEN-Mutationsstatus. Es hemmt die PI3K/Akt-Signalübertragung, indem es die Phosphorylierung von Akt an Serin 129 durch CK2 direkt blockiert und nicht durch Aktivierung von PTEN. Die Behandlung mit dieser Verbindung führt zu einer reduzierten Phosphorylierung von p21 (T145), erhöhten Spiegeln von Gesamt-p21 und p27 sowie zur Induktion der Caspase-3/7-Aktivität. Es induziert einen G2/M-Zellzyklus-Arrest in BT-474-Zellen und einen G1-Arrest in BxPC-3-Zellen. Diese Verbindung hemmt die HUVEC-Proliferation, -Migration und -Röhrchenbildung mit IC50-Werten von 5,5 M, 2 M bzw. 4 M. Unter hypoxischen Bedingungen in BT-474- und BxPC-3-Zellen verhindert es die Herunterregulierung von p53 und pVHL und reduziert die Aktivierung der HIF-1α-Transkription. Es hemmt die endogene intrazelluläre CK2-Aktivität mit einer IC50 von 0,1 M in Jurkat-Zellen. |
||
| In vivo | Die orale Verabreichung von Silmitasertib (CX-4945) in Dosen von 25 mg/kg oder 75 mg/kg zweimal täglich zeigt eine potente Antitumoraktivität im BT-474-Modell mit TGI von 88 % bzw. 97 %, wobei 2 von 9 Tieren in jeder Gruppe eine Reduktion der Tumorgröße um mehr als 50 % im Vergleich zum anfänglichen Tumorvolumen aufweisen. Im BxPC-3-Modell zeigt die Behandlung mit dieser Verbindung bei 75 mg/kg zweimal täglich eine 93 %ige TGI, wobei 3 Tiere am Ende der Behandlungsperiode keine Tumorreste aufweisen. Im PC3-Xenograft-Modell führt die Verabreichung von 25 mg/kg, 50 mg/kg oder 75 mg/kg zu einer Tumorwachstumsinhibition mit TGI von 19 %, 40 % bzw. 86 %. |
||
| Merkmale | Erster klinischer Inhibitor von CK2. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
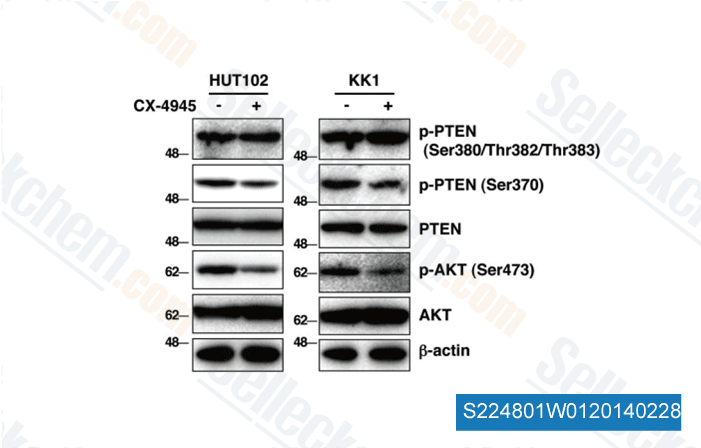
-
Daten von [ Nat Commun , 2014 , 5, 3393 ]
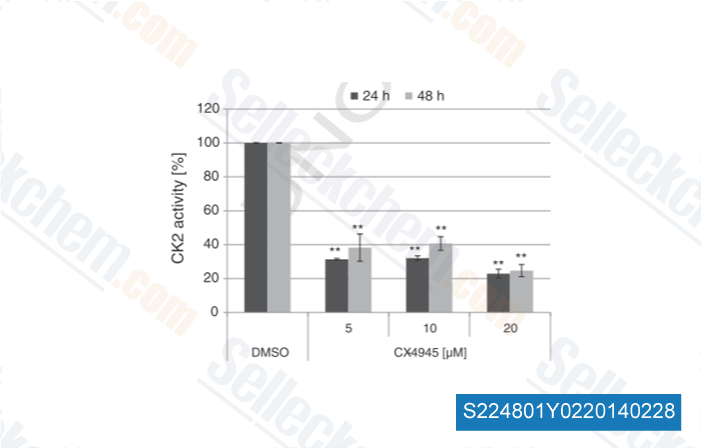
-
Daten von [ Cell Signal , 2014 , 26(7), 1567-75 ]
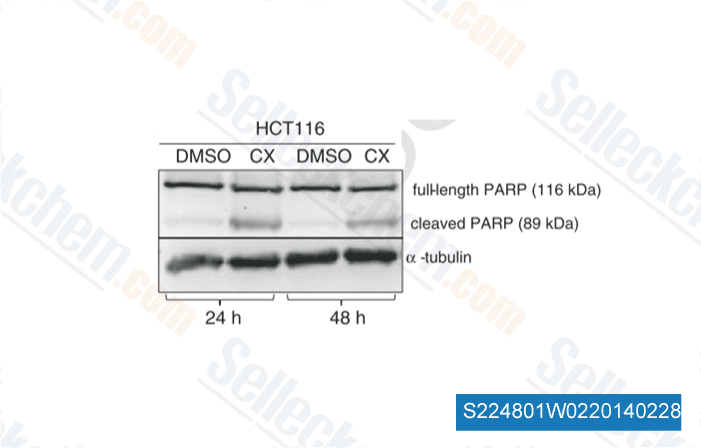
-
Daten von [ Cell Signal , 2014 , 26(7), 1567-75 ]
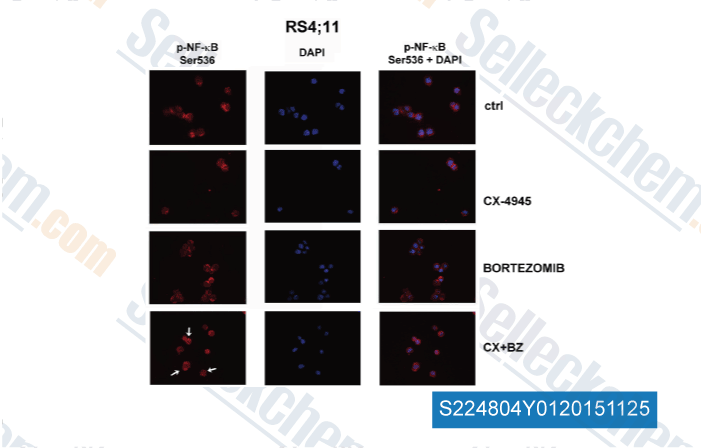
-
, , Oncotarget, 2015, 51: S659-S660
Sellecks Silmitasertib (CX-4945) Wurde zitiert von 153 Publikationen
| Reconstitution of BNIP3/NIX-mitophagy initiation reveals hierarchical flexibility of the autophagy machinery [ Nat Cell Biol, 2025, 27(8):1272-1287] | PubMed: 40715440 |
| Phosphorylation-dependent WRN-RPA interaction promotes recovery of stalled forks at secondary DNA structure [ Nat Commun, 2025, 16(1):997] | PubMed: 39870632 |
| Body weight control via protein kinase CK2: diet-induced obesity counteracted by pharmacological targeting [ Metabolism, 2025, 162:156060] | PubMed: 39521118 |
| CK2 regulates somatostatin expression in pancreatic delta cells [ Islets, 2025, 17(1):2515332] | PubMed: 40474387 |
| CK2 activity is crucial for proper glucagon expression [ Diabetologia, 2024, 10.1007/s00125-024-06128-1] | PubMed: 38503901 |
| Rutaecarpine alleviates inflammation and fibrosis by targeting CK2α in diabetic nephropathy [ Biomed Pharmacother, 2024, 180:117499] | PubMed: 39353318 |
| Protein kinase CK2α is overexpressed in classical hodgkin lymphoma, regulates key signaling pathways, PD-L1 and may represent a new target for therapy [ Front Immunol, 2024, 15:1393485] | PubMed: 38807597 |
| Mcam stabilizes a luminal progenitor-like breast cancer cell state via Ck2 control and Src/Akt/Stat3 attenuation [ NPJ Breast Cancer, 2024, 10(1):80] | PubMed: 39277578 |
| Protein kinase CK2 sustains de novo fatty acid synthesis by regulating the expression of SCD-1 in human renal cancer cells [ Cancer Cell Int, 2024, 24(1):432] | PubMed: 39726006 |
| Casein Kinase 2 Inhibitor, CX-4945, Induces Apoptosis and Restores Blood-Brain Barrier Homeostasis in In Vitro and In Vivo Models of Glioblastoma [ Cancers (Basel), 2024, 16(23)3936] | PubMed: 39682125 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
