Technische Daten
| Formel | C24H29FN6O5 |
||||||
| Molekulargewicht | 500.52 | CAS-Nr. | 915769-50-5 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 100 mg/mL (199.79 mM) | ||||
| Water | 66 mg/mL (131.86 mM) | ||||||
| Ethanol | 1 mg/mL (1.99 mM) | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Dovitinib (TKI258) Lactate monohydrate ist das Laktat von Dovitinib, einem Multitarget-RTK-Inhibitor, hauptsächlich für Klasse III (FLT3/c-Kit) mit IC50 von 1 nM/2 nM, auch wirksam gegen Klasse IV (FGFR1/3) und Klasse V (VEGFR1-4) RTKs mit IC50 von 8-13 nM, weniger wirksam gegen InsR, EGFR, c-Met, EphA2, Tie2, IGFR1 und HER2. Phase 4. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ziele |
|
|||||||||||
| In vitro | Dovitinib hemmt stark das FGF-stimulierte Wachstum von WT- und F384L-FGFR3-exprimierenden B9-Zellen mit einem IC50 von 25 nM. Darüber hinaus hemmt Dovitinib die Proliferation von B9-Zellen, die jede der verschiedenen aktivierten Mutanten von FGFR3 exprimieren. Interessanterweise gibt es minimale Unterschiede in der Empfindlichkeit der verschiedenen FGFR3-Mutationen gegenüber Dovitinib, wobei der IC50 für jede der verschiedenen Mutationen zwischen 70 und 90 nM liegt. IL-6-abhängige B9-Zellen, die nur Vektor enthalten (B9-MINV-Zellen), sind resistent gegen die hemmende Aktivität von Dovitinib bei Konzentrationen bis zu 1 μM. Dovitinib hemmt die Zellproliferation von KMS11 (FGFR3-Y373C), OPM2 (FGFR3-K650E) und KMS18 (FGFR3-G384D) Zellen mit einem IC50 von 90 nM (KMS11 und OPM2) bzw. 550 nM. Dovitinib hemmt die FGF-vermittelte ERK1/2-Phosphorylierung und induziert Zytotoxizität in FGFR3-exprimierenden primären MM-Zellen. BMSCs verleihen einen moderaten Grad an Resistenz mit 44,6 % Wachstumshemmung für Zellen, die mit 500 nM Dovitinib behandelt und auf Stroma kultiviert wurden, verglichen mit 71,6 % Wachstumshemmung für Zellen, die ohne BMSCs kultiviert wurden. Dovitinib hemmt die Proliferation von M-NFS-60, einer M-CSF-Wachstums-getriebenen Maus-myeloblastischen Zelllinie mit einer medianen effektiven Konzentration (EC50) von 220 nM. Die Behandlung von SK-HEP1-Zellen mit Dovitinib führt zu einer dosisabhängigen Reduktion der Zellzahl und einem G2/M-Phasenarrest mit Reduktion der G0/G1- und S-Phasen, Hemmung des Verankerungs-unabhängigen Wachstums und Blockierung der bFGF-induzierten Zellmotilität. Der IC50 für Dovitinib in SK-HEP1-Zellen beträgt ungefähr 1,7 μM. Dovitinib reduziert auch signifikant die basalen Phosphorylierungsspiegel von FGFR-1, FGFR-Substrat 2α (FRS2-α) und ERK1/2, aber nicht Akt in sowohl SK-HEP1- als auch 21-0208-Zellen. In 21-0208 HCC-Zellen hemmt Dovitinib signifikant die bFGF-induzierte Phosphorylierung von FGFR-1, FRS2-α, ERK1/2, aber nicht Akt. |
|||||||||||
| In vivo | Dovitinib induziert in vivo sowohl zytostatische als auch zytotoxische Reaktionen, die zu einer Regression von FGFR3-exprimierenden Tumoren führen. Dovitinib zeigt eine dosis- und expositionsabhängige Hemmung von Ziel-Rezeptor-Tyrosinkinasen (RTKs), die in Tumorzell-Xenografts exprimiert werden. Dovitinib hemmt stark das Tumorwachstum von sechs HCC-Linien. Die Hemmung der Angiogenese korrelierte mit der Inaktivierung der FGFR/PDGFRβ/VEGFR2-Signalwege. In einem orthotopen Modell hemmt Dovitinib stark das primäre Tumorwachstum und die Lungenmetastasierung und verlängerte signifikant das Überleben der Mäuse. Die Verabreichung von Dovitinib führt zu einer signifikanten Hemmung des Tumorwachstums und zu Tumorregressionen, einschließlich großer, etablierter Tumoren (500-1.000 mm3). |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung

-
, , Genome Biol, 2014, 15(8):428.

-
Daten von [ , , Neoplasia, 2013, 15(8):975-88 ]
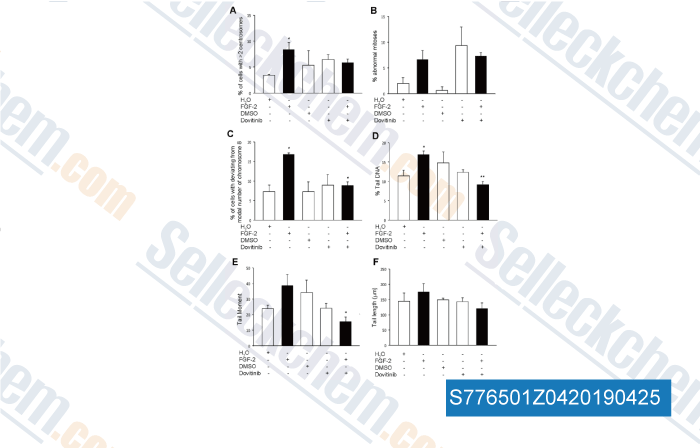
-
Daten von [ , , Urol Oncol, 2018, 36(8):365 ]
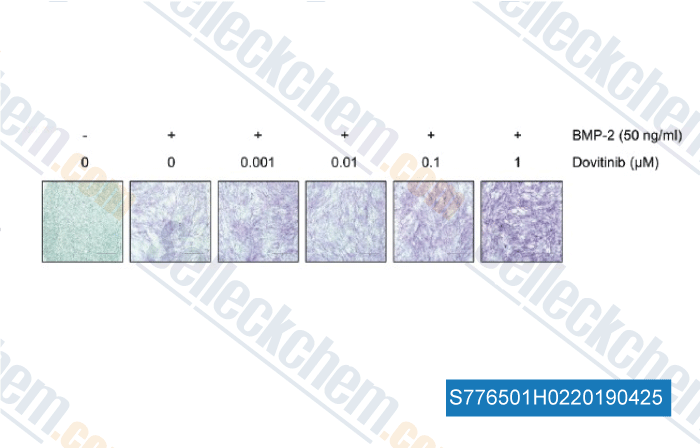
-
Daten von [ , , Mol Cells, 2016, 39(5):389-94 ]
Sellecks Dovitinib (TKI258) Lactate monohydrate Wurde zitiert von 31 Publikationen
| Lysine acetylation restricts mutant IDH2 activity to optimize transformation in AML cells [ Mol Cell, 2021, S1097-2765(21)00507-4] | PubMed: 34289383 |
| Targeting fibroblast growth factor receptors to combat aggressive ependymoma [ Acta Neuropathol, 2021, 10.1007/s00401-021-02327-x] | PubMed: 34046693 |
| Newly identified members of fibroblast growth factor receptor 1 splice variants engage in crosstalk with the AXL/AKT axis in salivary adenoid cystic carcinoma [ Cancer Res, 2021, canres.1780.2020] | PubMed: 33408119 |
| Effects of FGFR Tyrosine Kinase Inhibition in OLN-93 Oligodendrocytes [ Cells, 2021, 10(6)1318] | PubMed: 34070622 |
| Entrectinib Induces Apoptosis and Inhibits the Epithelial-Mesenchymal Transition in Gastric Cancer with NTRK Overexpression [ Int J Mol Sci, 2021, 23(1)395] | PubMed: 35008821 |
| TRK inhibitors block NFKB and induce NRF2 in TRK fusion-positive colon cancer [ J Cancer, 2021, 12(21):6356-6362] | PubMed: 34659525 |
| TRK inhibitors block NFKB and induce NRF2 in TRK fusion-positive colon cancer [ Journal of Cancer, 2021, 12(21): 6356-6362] | PubMed: None |
| Comprehensive pharmacogenomic characterization of gastric cancer. [ Genome Med, 2020, 18;12(1):17] | PubMed: 32070411 |
| Effects of FGFR inhibitors TKI258, BGJ398 and AZD4547 on breast cancer cells in 2D, 3D and tissue explant cultures [ Cell Oncol (Dordr), 2020, 10.1007/s13402-020-00562-0] | PubMed: 33119860 |
| Anti-Proliferative Effect of Allium senescens L. Extract in Human T-Cell Acute Lymphocytic Leukemia Cells [ Molecules, 2020, 26(1)E35] | PubMed: 33374788 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
