Technische Daten
| Formel | C22H23N3O4 |
||||||
| Molekulargewicht | 393.44 | CAS-Nr. | 183321-74-6 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 78 mg/mL (198.25 mM) | ||||
| Ethanol | 78 mg/mL (198.25 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Erlotinib ist ein EGFR-Inhibitor mit einer IC50 von 2 nM, der ">1000-fach empfindlicher für EGFR ist als menschliches c-Src oder v-Abl. Erlotinib induziert Autophagy. | ||
|---|---|---|---|
| Ziele |
|
||
| In vitro | Erlotinib HCl hemmt die EGFR-Aktivierung in intakten Zellen, einschließlich menschlicher HNS-Kopf- und Hals-Tumorzellen (IC50 20nM), DiFi-Darmkrebszellen und MDA MB-468-Brustkrebszellen. Diese Verbindung (1 μM) induziert Apoptose in menschlichen DiFi-Darmkrebszellen. Sie hemmt das Wachstum einer Reihe von NSCLC-Zelllinien, einschließlich A549, H322, H3255, H358 H661, H1650, H1975, H1299, H596 mit IC50-Werten von 29 nM bis >20 μM. Diese Chemikalie (2 μM) hemmt signifikant das Wachstum von AsPC-1- und BxPC-3-Pankreaszellen. Die Wirkungen dieser Verbindung in Kombination mit Gemcitabin werden bei KRAS-mutierten Pankreaskrebszellen als additiv betrachtet. Zehn Mikromolar dieser Chemikalie hemmt die EGFR-Phosphorylierung an den Stellen Y845 (Src-abhängige Phosphorylierung) und Y1068 (Autophosphorylierung). Die Kombination mit dieser Verbindung könnte die Rapamycin-stimulierte Akt-Aktivität herabregulieren und einen synergistischen Effekt auf die Zellwachstumshemmung erzielen. |
||
| In vivo | Bei Dosen von 100 mg/kg verhindert Erlotinib HCl die EGF-induzierte Autophosphorylierung von EGFR in menschlichen HN5-Tumoren, die als Xenotransplantate in athymischen Mäusen wachsen, und des hepatischen EGFR der behandelten Mäuse vollständig. Diese Verbindung (100 mg/Kg) hemmt die Tumormodelle H460a und A549 mit einer Hemmrate von 71 bzw. 93 %. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung

-
Daten von [ Cancer Res , 2014 , 4(1):253-62 ]
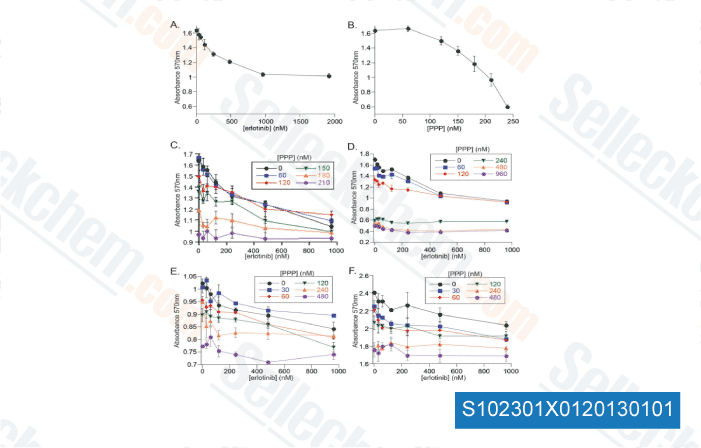
-
Daten von [ Head Neck , 2013 , 35, 86-93 ]
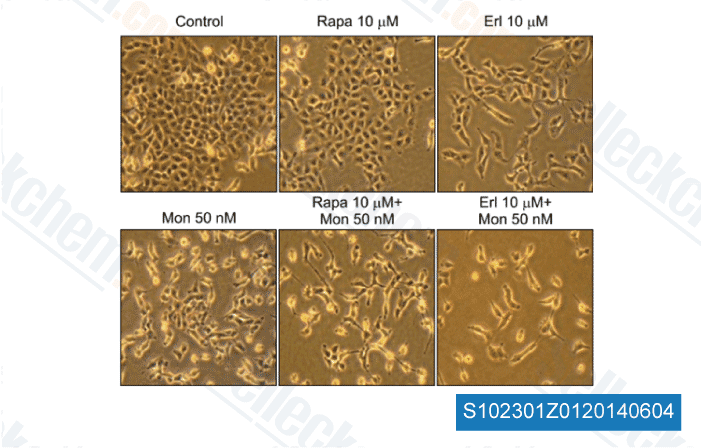
-
Daten von [ Tuberc Respir Dis , 2013 , 75(1), 9-17 ]
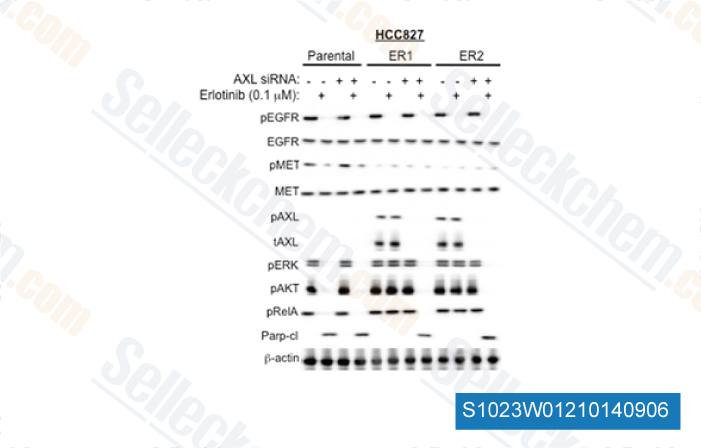
-
Daten von [ Nat Genet , 2012 , 44(8):852-60 ]
Sellecks Erlotinib (CP-358774) Wurde zitiert von 650 Publikationen
| Non-canonical dihydrolipoyl transacetylase promotes chemotherapy resistance via mitochondrial tetrahydrofolate signaling [ Nat Commun, 2025, 16(1):8932] | PubMed: 41062483 |
| EGFR TKIs suppress MUC1 glycosylation through the PI3K/AKT/SP1/C1GALT1 pathway to enhance TnMUC1 CAR-T efficacy in EGFR-mutant NSCLC [ Cell Rep Med, 2025, S2666-3791(25)00272-1] | PubMed: 40562040 |
| Multi-layer stratified oncology platform utilizing transcriptomics, prostate cancer organoids, and modeling of drug response [ J Exp Clin Cancer Res, 2025, 44(1):290] | PubMed: 41094672 |
| AP1-mediated reprogramming of EGFR expression triggers resistance to BLU-667 and LOXO-292 in RET-rearranged tumors [ J Exp Clin Cancer Res, 2025, 44(1):154] | PubMed: 40405293 |
| Targeting CDK12/13 Drives Mitotic Arrest to Overcome Resistance to KRASG12C Inhibitors [ Cancer Res, 2025, 10.1158/0008-5472.CAN-25-0450] | PubMed: 41165466 |
| Anti-galectin-9 therapy synergizes with EGFR inhibition to reprogram the tumor microenvironment and overcome immune evasion [ J Immunother Cancer, 2025, 13(7)e010926] | PubMed: 40664443 |
| Oncogenic RARγ isoforms promote head and neck cancer proliferation through vinexin-β-mediated cell cycle acceleration and autocrine activation of EGFR signal [ Int J Biol Sci, 2025, 21(1):1-16] | PubMed: 39744424 |
| The AURKA inhibitor alters the immune microenvironment and enhances targeting B7-H3 immunotherapy in glioblastoma [ JCI Insight, 2025, e173700] | PubMed: 39928563 |
| Rare mutations at EGFR L747 position: molecular characteristics and superior response to afatinib in NSCLC patients [ ESMO Open, 2025, 10(9):105558] | PubMed: 40834500 |
| Targeting both wild-type EGFR and its drug-resistant mutants with erlotinib-aptamer conjugates [ Eur J Med Chem, 2025, 296:117871] | PubMed: 40554308 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
