Technische Daten
| Formel | C15H18ClO4.Na |
||||||
| Molekulargewicht | 320.74 | CAS-Nr. | 828934-41-4 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 64 mg/mL (199.53 mM) | ||||
| Water | 64 mg/mL (199.53 mM) | ||||||
| Ethanol | 64 mg/mL (199.53 mM) | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Etomoxir sodium salt ((R)-(+)-Etomoxir sodium salt) ist ein irreversibler Inhibitor der Carnitin-Palmitoyltransferase-1 (CPT-1) auf der Außenseite der inneren Mitochondrienmembran. Etomoxir verstärkt die Palmitat-induzierte Zellapoptose. | ||
|---|---|---|---|
| Ziele |
|
||
| In vitro | Etomoxir sodium salt wurde auch als direkter Agonist von PPARα identifiziert. Diese Verbindung bindet irreversibel an die katalytische Stelle von CPT-1, hemmt deren Aktivität, reguliert aber auch Enzyme der Fettsäureoxidation hoch. Transkriptionelle Effekte von Etomoxir könnten auf 1. eine Verschiebung im Energiemetabolismus mit erhöhter Glukoseverwertung und 2. PPARalpha-Aktivierung zurückzuführen sein. Es reduziert die Produktion proinflammatorischer Zytokine und erhöht die Apoptose von MOG-spezifischen T-Zellen. Etomoxir wurde gezeigt, dass es die Sauerstoffverbrauchsraten (OCRs) verringert und die ATP- und NADPH-Produktion in der pädiatrischen Glioblastom-Zelllinie SF188 beeinträchtigt. | ||
| In vivo | Etomoxir sodium salt hat eine schützende Wirkung auf die Ischämie/Reperfusionsschädigung der Niere, ähnlich einem etablierten PPARalpha-Agonisten. Es wurde zur Behandlung von nicht-insulinabhängigem Diabetes Mellitus entwickelt. Diese Verbindung erhöht die funktionelle Erholung von mit Fettsäuren perfundierten ischämischen Rattenherzen, was nicht mit Veränderungen der Langketten-Acylcarnitinspiegel zusammenhängt und einem erhöhten Glukoseverbrauch zugeschrieben wird. Eine chronische Behandlung von Ratten mit dieser Chemikalie erhöht die SR-Ca2+-ATPase-Aktivität, die Ca2+-Aufnahmerate, die Anzahl der aktiven Ca2+-Pumpen E~P, das SERCA2-Protein und die SERCA2-mRNA-Abundanz des Herzens. Bei niedriger Dosierung hat es einen selektiven Einfluss auf die Kontraktions- und Entspannungsrate überlasteter Herzen. Diese Verbindung kann in der Leber als peroxisomaler Proliferator wirken, wodurch die DNA-Synthese und das Leberwachstum erhöht werden. Mit Etomoxir behandelte Mäuse zeigen eine reduzierte Immunzellinfiltration im ZNS mit wenigen Makrophagen, aktivierten Mikroglia oder T-Zellen. Es reduziert Entzündungen und Demyelinisierung im ZNS behandelter Mäuse. Die Hemmung der Fettsäureoxidation durch diese Chemikalie verlängert die Überlebenszeit in einem syngenen Mausmodell des malignen Glioms und verlangsamt das Tumorwachstum. Das Auftreten und Fortschreiten des Glioms werden bei Behandlung mit dem Prüfmedikament Etomoxir verzögert. Es wurde bereits in klinischen Studien der Phase I/II zur Behandlung von mittelschwerer kongestiver Herzinsuffizienz getestet; diese Studie wurde abgebrochen, da 4 Patienten (von 226, die das Medikament einnahmen) bei der Behandlung unzulässig hohe Lebertransaminasewerte entwickelten und das Risiko solch drastischer Nebenwirkungen als ausreichend angesehen wird, um den potenziellen Nutzen dieses Medikaments für diese Patienten zu negieren. |
Protokoll (aus Referenz)
| Zell-Assay: |
|
|---|---|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
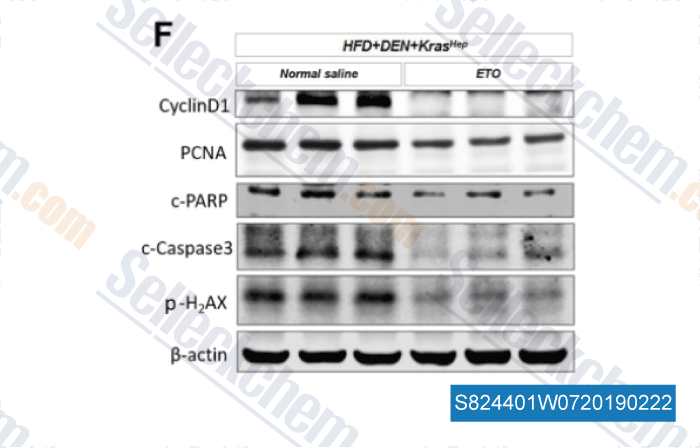
-
Daten von [ , , Cancer Lett, 2018, 442:40-52 ]
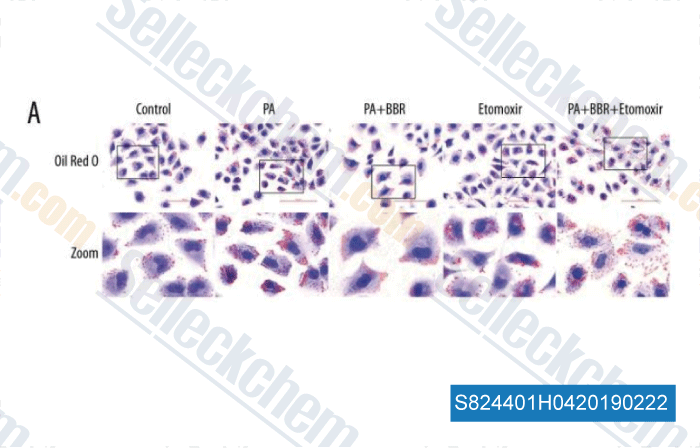
-
Daten von [ , , Med Sci Monit, 2018, 24:1484-1492 ]
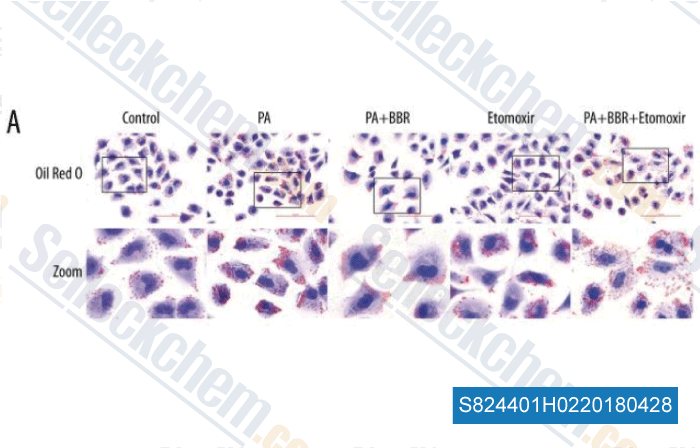
-
Daten von [ , , Med Sci Monit, 2018, 24: 1484-1492 ]
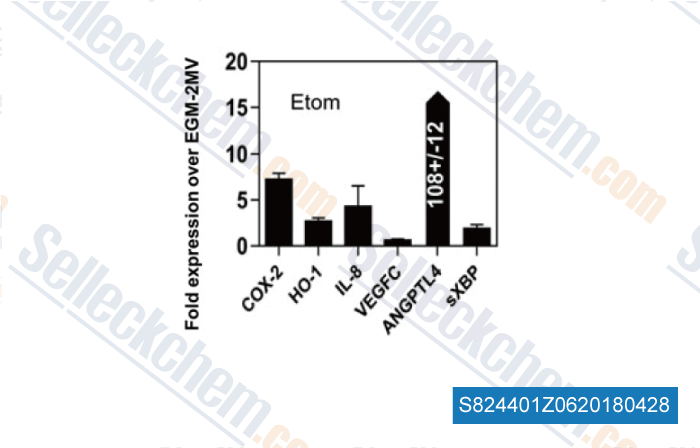
-
Daten von [ , , Lymphatic Research and BiologyVol, 2018, 16(1). https://doi.org/10.1089/lrb.2017.0033 ]
Sellecks Etomoxir sodium salt Wurde zitiert von 52 Publikationen
| Coenzyme A protects against ferroptosis via CoAlation of mitochondrial thioredoxin reductase [ J Clin Invest, 2025, e190215] | PubMed: 40694424 |
| Inhibition of adenosine/A2A receptor signaling suppresses dermal fibrosis by enhancing fatty acid oxidation [ Cell Commun Signal, 2025, 23(1):206] | PubMed: 40301970 |
| Autophagic flux-lipid droplet biogenesis cascade sustains mitochondrial fitness in colorectal cancer cells adapted to acidosis [ Cell Death Discov, 2025, 11(1):21] | PubMed: 39856069 |
| Comprehensive characterization of fatty acid oxidation in triple-negative breast cancer: Focus on biological roles and drug modulation [ Eur J Pharmacol, 2025, 991:177343] | PubMed: 39900330 |
| Metabolic imprinting drives epithelial memory during mucosal fungal infection [ bioRxiv, 2025, 2025.07.11.664387] | PubMed: 40791350 |
| Extracellular matrix stiffness as an energy metabolism regulator drives osteogenic differentiation in mesenchymal stem cells [ Bioact Mater, 2024, 35:549-563] | PubMed: 38434800 |
| NINJ1 regulates ferroptosis via xCT antiporter interaction and CoA modulation [ Cell Death Dis, 2024, 15(10):755] | PubMed: 39424803 |
| Small molecules targeting selective PCK1 and PGC-1α lysine acetylation cause anti-diabetic action through increased lactate oxidation [ Cell Chem Biol, 2024, 31(10):1772-1786.e5] | PubMed: 39341205 |
| PIM1 drives lipid droplet accumulation to promote proliferation and survival in prostate cancer [ Oncogene, 2024, 43(6):406-419] | PubMed: 38097734 |
| Monocyte and macrophage profiles in patients with inherited long-chain fatty acid oxidation disorders [ Biochim Biophys Acta Mol Basis Dis, 2024, 1871(1):167524] | PubMed: 39307292 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
