Technische Daten
| Formel | C33H37F2N7O4 |
||||||||||
| Molekulargewicht | 633.69 | CAS-Nr. | 928037-13-2 | ||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 20 mg/mL (31.56 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Golvatinib (E7050) ist ein dualer c-Met- und VEGFR-2-Inhibitor mit einer IC50 von 14 nM bzw. 16 nM. Diese Verbindung hemmt nicht das bFGF-stimulierte HUVEC-Wachstum (bis zu 1000 nM) und befindet sich derzeit in Phase-1/2-Studien. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | In-vitro-Studien zeigen, dass Golvatinib (E7050) die Phosphorylierung von sowohl c-Met als auch VEGFR-2 stark hemmt. Es unterdrückt auch stark das Wachstum von c-Met-amplifizierten Tumorzellen und Endothelzellen, die entweder mit HGF oder VEGF stimuliert wurden. Diese Verbindung umgeht die Resistenz gegen alle reversiblen, irreversiblen und mutationsselektiven EGFR-TKIs, die durch exogenes und/oder endogenes HGF in EGFR-mutierten Lungenkrebszelllinien induziert werden, indem sie den Met/Gab1/PI3K/Akt-Signalweg in vitro blockiert. Es verhindert auch das Auftreten von Gefitinib-resistenten HCC827-Zellen, die durch kontinuierliche Exposition gegenüber HGF induziert werden. | ||||
| In vivo | Golvatinib (E7050) zeigt in vivo eine Hemmung der Phosphorylierung von c-Met und VEGFR-2 in Tumoren, mit einer starken Unterdrückung des Tumorwachstums und der Angiogenese in Xenograft-Modellen. Die Behandlung einiger Tumorlinien mit c-Met-Amplifikationen mit hohen Dosen dieser Verbindung (50–200 mg/kg) induziert Tumorrückbildung und -verschwinden. In einem Modell der peritonealen Dissemination zeigt es eine Antitumorwirkung gegen peritoneale Tumoren sowie eine signifikante Verlängerung der Lebensdauer bei behandelten Mäusen. In einer weiteren Xenograft-Studie sind Tumoren, die durch HGF-transfizierte Ma-1 (Ma-1/HGF)-Zellen erzeugt wurden, angiogener als Vektor-Kontrolltumoren und zeigen eine Resistenz gegen ZD1839. E7050 allein hemmt die Angiogenese und verzögert das Wachstum von Ma-1/HGF-Tumoren, und in Kombination mit ZD1839 induziert es eine ausgeprägte Regression des Tumorwachstums. |
Protokoll (aus Referenz)
| Kinase-Assay:[1] |
|
|---|---|
| Zell-Assay:[1] |
|
| Tierstudie:[1] |
|
Referenzen
|
Kundenproduktvalidierung
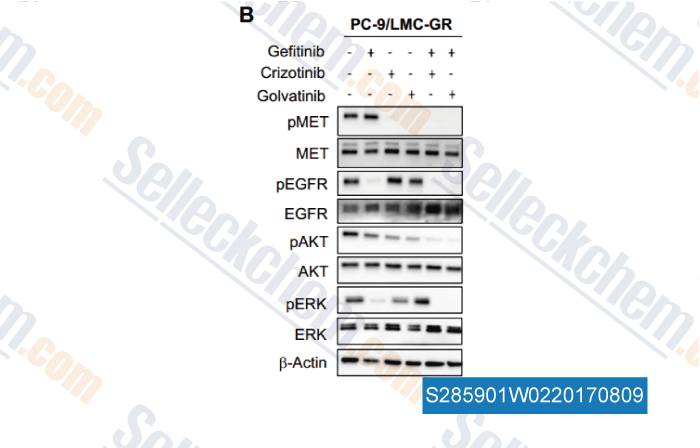
-
Daten von [ , , Mol Cancer Ther, 2017, 16(3):506-515 ]
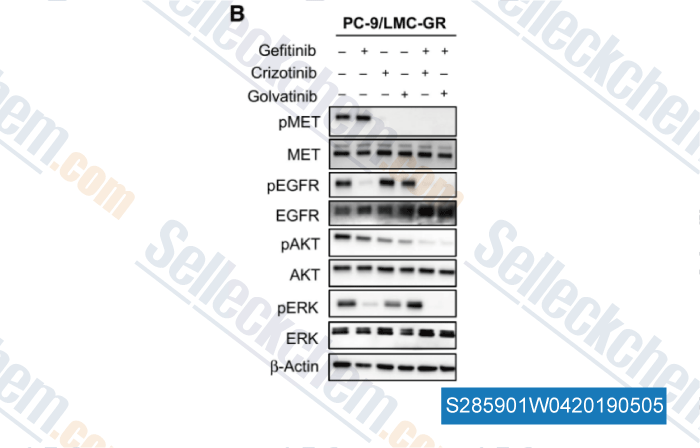
-
Daten von [ , , Mol Cancer Ther, 2017, 16(3):506-515 ]
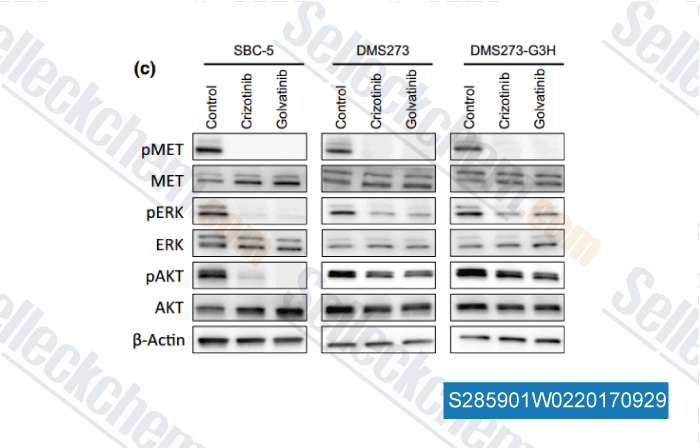
-
Daten von [ , , Cancer Sci, 2017, 108(7):1378-1385 ]
Sellecks Golvatinib (E7050) Wurde zitiert von 8 Publikationen
| E7050 Suppresses the Growth of Multidrug-Resistant Human Uterine Sarcoma by Inhibiting Angiogenesis via Targeting of VEGFR2-Mediated Signaling Pathways [ Int J Mol Sci, 2023, 24(11)9606] | PubMed: 37298555 |
| Blockade of c-Met-Mediated Signaling Pathways by E7050 Suppresses Growth and Promotes Apoptosis in Multidrug-Resistant Human Uterine Sarcoma Cells [ Int J Mol Sci, 2022, 23(23)14884] | PubMed: 36499211 |
| MET amplification results in heterogeneous responses to osimertinib in EGFR-mutant lung cancer treated with erlotinib [ Cancer Sci, 2020, 111(10):3813-3823] | PubMed: 32735723 |
| Diverse Receptor Tyrosine Kinase Phosphorylation in Urine-Derived Tubular Epithelial Cells from Autosomal Dominant Polycystic Kidney Disease Patients [ Nephron, 2020, 1-12] | PubMed: 32799196 |
| LECT2, a Ligand for Tie1, Plays a Crucial Role in Liver Fibrogenesis [ Cell, 2019, 178(6):1478-1492] | PubMed: 31474362 |
| MET Copy Number Gain Is Associated with Gefitinib Resistance in Leptomeningeal Carcinomatosis of EGFR-mutant Lung Cancer [Nanjo S Mol Cancer Ther, 2017, 16(3):506-515] | PubMed: 28138027 |
| Impact of MET inhibition on small-cell lung cancer cells showing aberrant activation of the hepatocyte growth factor/MET pathway. [Taniguchi H, et al. Cancer Sci, 2017, 108(7):1378-1385] | PubMed: 28474864 |
| In vivo imaging xenograft models for the evaluation of anti-brain tumor efficacy of targeted drugs [Kita K Cancer Med, 2017, 6(12):2972-2983] | PubMed: 29125233 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
