Technische Daten
| Formel | C35H30N4O4 |
||||||||||
| Molekulargewicht | 570.64 | CAS-Nr. | 120685-11-2 | ||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 100 mg/mL (175.24 mM) | ||||||||
| Ethanol | 2 mg/mL (3.5 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Midostaurin ist ein Multi-Target-Kinaseinhibitor, einschließlich PKCα/β/γ, Syk, Flk-1, Akt, PKA, c-Kit, c-Fgr, c-Src, FLT3, PDFRβ und VEGFR1/2 mit einer IC50 von 80-500 nM. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ziele |
|
|||||||||||
| In vitro | Midostaurin (PKC412) ist ein Breitspektrum-Proteinkinase-Inhibitor. Diese Verbindung interagiert stark mit den ATP-Bindungsstellen der konventionellen PKC-α, -β und -γ, PDGFRβ, VEGF-R2, VEGF-R1 und dem Cyclin-abhängigen Kinase-1-Cyclin-B-Komplex. Es hemmt das Wachstum verschiedener menschlicher und tierischer Zelllinien in vitro bei ähnlichen submikromolaren Konzentrationen. Diese Chemikalie hemmt auch wirksam die In-vitro-Proliferation von Glioblastomen und induzierte die Akkumulation von Zellen in G2/M und die Bildung von Riesenkernen mit ausgedehnter Fragmentierung und apoptotischen Körpern. Es ist in der Lage, die p-Glykoprotein-vermittelte Multidrug-Resistenz von Tumorzellen in vitro umzukehren. | |||||||||||
| In vivo | Midostaurin (PKC412) kann das Tumorwachstum unterdrücken, indem es die Tumorangiogenese (über seine Auswirkungen auf die VEGF-Rezeptor-Tyrosinkinasen) hemmt und zusätzlich direkt die Proliferation von Tumorzellen (über seine Auswirkungen auf PKCs) hemmt. Diese antiangiogene Wirkung kann zu der antimetastatischen und breiten Antitumoraktivität dieser Verbindung sowie zur Synergie mit zytotoxischen Mitteln, einschließlich Doxorubicin, Cyclophosphamid, Cisplatin und Gemcitabin, beitragen. Oral verabreicht beträgt die maximal tolerierte Dosis für diese Chemikalie >300 mg/kg. |
Protokoll (aus Referenz)
| Zell-Assay:[2] |
|
|---|---|
| Tierstudie:[1] |
|
Referenzen
|
Kundenproduktvalidierung
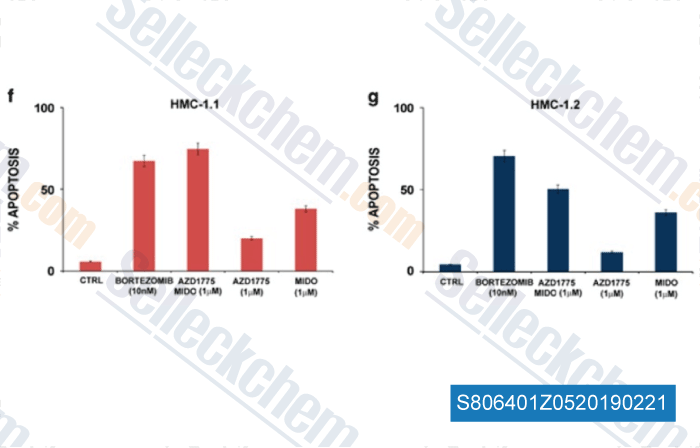
-
Daten von [ , , Leukemia, 2018, 32(1):139-148 ]
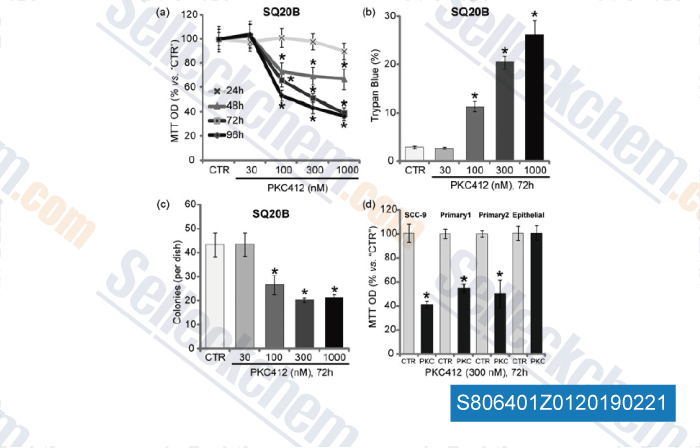
-
Daten von [ , , J Cell Physiol, 2018, 233(12):9437-9446 ]
Sellecks Midostaurin (PKC412) Wurde zitiert von 56 Publikationen
| The lncRNA ELDR suppresses tumorigenicity of AML by interfering with DNA replication and chromatin accessibility [ Blood Adv, 2025, bloodadvances.2024015427] | PubMed: 40921006 |
| Anti-Tumor Effects of Gilteritinib on FLT3 Mutations: Insights into Resistance Mechanisms in Ba/F3 Cell Models [ Onco Targets Ther, 2025, 18:489-501] | PubMed: 40196870 |
| RSK1 dependency in FLT3-ITD acute myeloid leukemia [ Blood Cancer J, 2024, 14(1):207] | PubMed: 39592591 |
| Unveiling the signaling network of FLT3-ITD AML improves drug sensitivity prediction [ Elife, 2024, 12RP90532] | PubMed: 38564252 |
| Patient-derived rhabdomyosarcoma cells recapitulate the genetic and transcriptomic landscapes of primary tumors [ iScience, 2024, 27(10):110862] | PubMed: 39319271 |
| The Immunomodulatory Effect of Different FLT3 Inhibitors on Dendritic Cells [ Cancers (Basel), 2024, 16(21)3719] | PubMed: 39518156 |
| Activation of the receptor KIT induces the secretion of exosome-like small extracellular vesicles [ J Extracell Biol, 2024, 3(1):e139] | PubMed: 38938682 |
| Targeting FLT3 with a new-generation antibody-drug conjugate in combination with kinase inhibitors for treatment of AML [ Blood, 2023, 141(9):1023-1035] | PubMed: 35981498 |
| A combinatorial therapeutic approach to enhance FLT3-ITD AML treatment [ Cell Rep Med, 2023, 10.1016/j.xcrm.2023.101286] | PubMed: 37951217 |
| ABCC1 and glutathione metabolism limit the efficacy of BCL-2 inhibitors in acute myeloid leukemia [ Nat Commun, 2023, 14(1):5709] | PubMed: 37726279 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
