Technische Daten
| Formel | C23H20N6O |
||||||
| Molekulargewicht | 396.44 | CAS-Nr. | 726169-73-9 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 13 mg/mL (32.79 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Mocetinostat (MGCD0103, MG0103) ist ein potenter HDAC-Inhibitor mit der höchsten Potenz für HDAC1 mit einem IC50-Wert von 0,15 μM in einem zellfreien Assay, einer 2- bis 10-fachen Selektivität gegenüber HDAC2, 3 und 11 und keiner Aktivität gegenüber HDAC4, 5, 6, 7 und 8. Mocetinostat (MGCD0103) induziert Apoptosis und Autophagy. Phase 2. | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Ziele |
|
||||||||
| In vitro | Mocetinostat (MGCD0103) hemmt nur eine Untergruppe der neun humanen rekombinanten HDACs, einschließlich HDAC1, HDAC2, HDAC3 und HDAC11, in nanomolaren oder niedrigen mikromolaren Konzentrationen und auf dosisabhängige Weise. Es zeigt in vitro die potenteste hemmende Aktivität gegen humane HDAC1- und HDAC2-Enzyme und hemmt keine Klasse-II-HDACs. Die exozyklische Aminogruppe in dieser Verbindung ist für die Enzym-hemmende Aktivität notwendig, da die HDAC-hemmende Aktivität gegen HDAC1 und HDAC2 mit dem Desamino-Analogon vollständig aufgehoben wird. Seine hemmende Aktivität erreicht bei 6 μM ein maximales Plateau, und der maximale hemmbare Enzympool, der von MGCD0103 beeinflusst wird, beträgt 75 % der gesamten Enzymaktivität in HCT116-Zellen, während NVP-LAQ824 fast 100 % davon in diesen Zellen hemmt. In A549-Zellen zeigt es auch eine dosisabhängige Hemmung der HDAC-Aktivität in ganzen Zellen. |
||||||||
| In vivo | Mocetinostat (MGCD0103) hemmt signifikant das Wachstum menschlicher Tumor-Xenografts in Nacktmäusen, und die Antitumoraktivität korrelierte mit der Induktion der Histonacetylierung in Tumoren. Die p.o.-Verabreichung dieser Verbindung (2HBr-Salz) verringert signifikant das Wachstum von implantierten fortgeschrittenen A549-Tumoren in Nacktmäusen dosisabhängig nach 13-tägiger täglicher Verabreichung. Es (170 mg/kg für 2HBr-Salz, entsprechend 120 mg/kg freie Base) blockiert signifikant das Wachstum von Tumoren im Vergleich zur alleinigen Fahrzeugbehandlung ohne Veränderung des Körpergewichts. Darüber hinaus reduziert es nicht die WBC-Zahlen und wird gut vertragen. Die Verbindung ist auch oral aktiv in vielen anderen humanen Tumor-Xenograft-Modellen, einschließlich NSCLC H1437. Bei 80 mg/kg (freie Base) blockiert es fast vollständig das Wachstum von H1437-Tumoren nach 13-tägiger täglicher p.o.-Verabreichung ohne Reduzierung des Körpergewichts bei Tieren. Es reduziert den pulmonalen arteriellen Druck dramatischer. Darüber hinaus verbessert diese Verbindung die pulmonale Arterienbeschleunigungszeit und reduziert die systolische Einkerbung der pulmonalen Arterienflusskurve, was auf einen positiven Einfluss des HDAC inhibitor auf die pulmonale Gefäßumgestaltung und -versteifung hindeutet. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
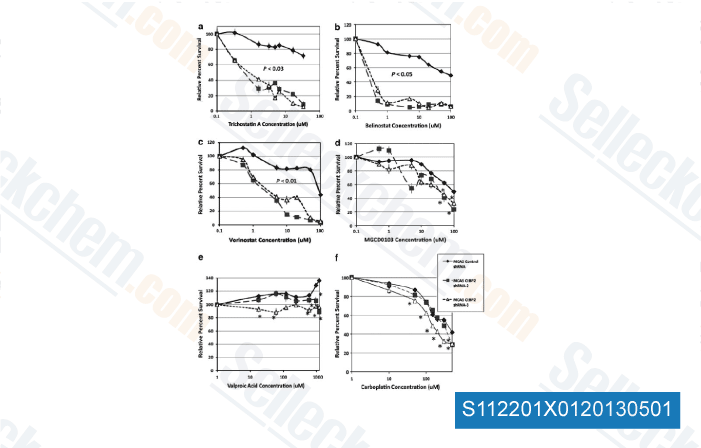
-
Daten von [ Oncogene , 2012 , 32, 3896-903 ]
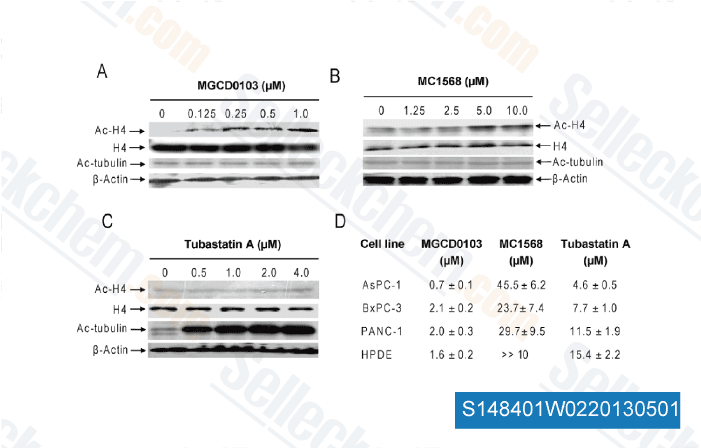
-
Daten von [ PLoS One , 2012 , 7, e52095 ]
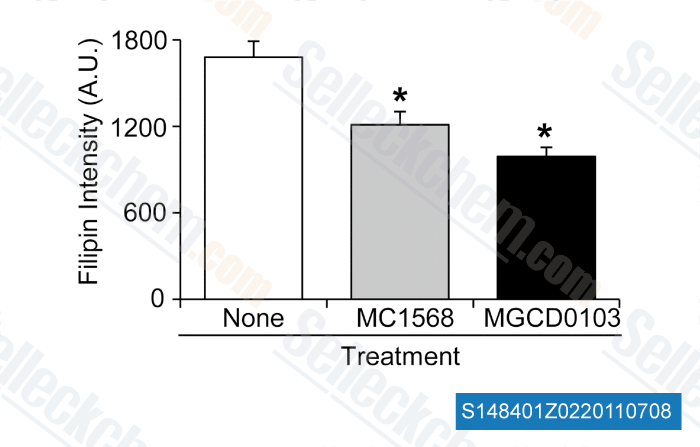
-
Daten von [ J Biol Chem , 2011 , 286, 23842–23851 ]
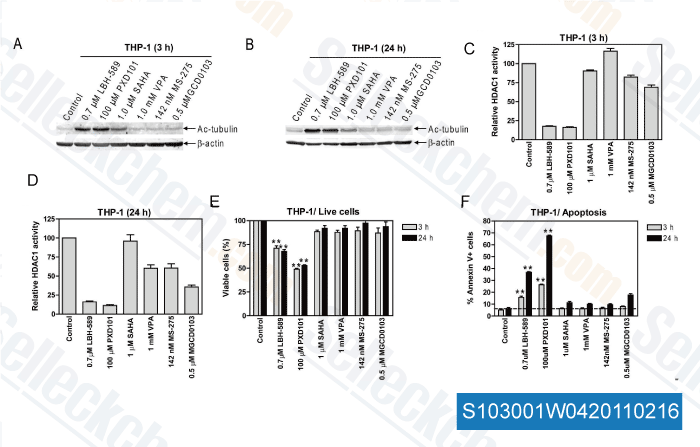
-
Daten von [ PLoS One , 2011 , 6, e17138 ]
Sellecks Mocetinostat (MGCD0103) Wurde zitiert von 119 Publikationen
| Identifying Age-Modulating Compounds Using a Novel Computational Framework for Evaluating Transcriptional Age [ Aging Cell, 2025, e70075] | PubMed: 40307992 |
| Signal transduction pathways controlling Ins2 gene activity and beta cell state transitions [ iScience, 2025, 28(3):112015] | PubMed: 40144638 |
| Inhibition of HDAC6 elicits anticancer effects on head and neck cancer cells through Sp1/SOD3/MKP1 signaling axis to downregulate ERK phosphorylation [ Cell Signal, 2025, 127:111587] | PubMed: 39755348 |
| The microbial metabolite butyrate enhances the effector and memory functions of murine CD8+ T cells and improves anti-tumor activity [ Front Med (Lausanne), 2025, 12:1577906] | PubMed: 40630475 |
| HIV-1 Vpr drives epigenetic remodeling to enhance virus transcription and latency reactivation [ bioRxiv, 2025, 2025.01.31.635859] | PubMed: 39975144 |
| Role of the NuRD complex and altered proteostasis in cancer cell quiescence [ bioRxiv, 2025, 2025.02.10.637435] | PubMed: 39990343 |
| Inhibition of HDAC activity directly reprograms murine embryonic stem cells to trophoblast stem cells [ Dev Cell, 2024, S1534-5807(24)00326-5] | PubMed: 38823394 |
| Inhibition of Selenoprotein I promotes ferroptosis and reverses resistance to platinum chemotherapy by impairing Akt phosphorylation in ovarian cancer [ MedComm (2020), 2024, 5(12):e70033] | PubMed: 39669976 |
| Romidepsin and afatinib abrogate JAK-STAT signaling and elicit synergistic antitumor effects in cutaneous T-cell lymphoma [ J Invest Dermatol, 2024, S0022-202X(23)03210-4] | PubMed: 38219917 |
| Pancreatic cancer acquires resistance to MAPK pathway inhibition by clonal expansion and adaptive DNA hypermethylation [ Clin Epigenetics, 2024, 16(1):13] | PubMed: 38229153 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
