Technische Daten
| Formel | C30H29ClN6O3 |
||||||
| Molekulargewicht | 557.04 | CAS-Nr. | 698387-09-6 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO (mit 50 °C warmem Wasserbad erwärmt) | 7 mg/mL (12.56 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Neratinib ist ein hochselektiver HER2- und EGFR-Inhibitor mit IC50-Werten von 59 nM und 92 nM in zellfreien Assays; er hemmt KDR und Src schwach, ohne signifikante Hemmung von Akt, CDK1/2/4, IKK-2, MK-2, PDK1, c-Raf und c-Met. Phase 3. | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Ziele |
|
||||||||
| In vitro | Neratinib hemmt die Tyrosinkinasen KDR und Src schwach mit IC50-Werten von 0,8 μM bzw. 1,4 μM, was einer 14- bzw. 24-fach geringeren Aktivität im Vergleich zu HER2 entspricht. Diese Verbindung zeigt keine Aktivität gegen andere Serin-Threonin-Kinasen wie Akt, Cyclin D1/cdk4, Cyclin E/cdk2, Cyclin B1/cdk1, IKK-2, MK-2, PDK1, c-Raf und Tpl-2, sowie die Tyrosinkinase c-Met. Es hemmt selektiv die Proliferation von 3T3-Zellen, die mit dem HER2 (3T3/neu) transfiziert sind, sowie von zwei anderen HER-2-überexprimierenden SK-Br-3- und BT474-Zellen mit IC50-Werten von 2-3 nM, was eine >230-fache Potenz im Vergleich zu nicht-transfizierten 3T3-Zellen sowie MDA-MB-435 und SW620, die EGFR- und HER2-negativ sind, zeigt. Diese Chemikalie hemmt auch die Proliferation von EGFR-abhängigen A431-Zellen mit einem IC50 von 81 nM. Sie reduziert die HER2-Rezeptor-Autophosphorylierung in BT474-Zellen mit einem IC50 von 5 nM und die EGF-abhängige Phosphorylierung von EGFR in A431-Zellen mit einem IC50 von 3 nM. Die Blockierung von HER-2 durch diese Verbindung führt zur Hemmung der nachgeschalteten MAPK- und Akt-Signalwege mit einem IC50 von 2 nM, was potenter ist als Trastuzumab. Es hemmt die Cyclin-D1-Expression und die Phosphorylierung des Rb-Suszeptibilitätsgenprodukts in BT474-Zellen mit einem IC50 von 9 nM, was zu einem G1-S-Arrest und letztendlich einer verminderten Zellproliferation führt. | ||||||||
| In vivo | Die orale Verabreichung von Neratinib hemmt signifikant das Wachstum von 3T3/neu-Xenografts, mit einer Hemmung von 34 %, 53 %, 98 % und 98 % bei Dosen von 10, 20, 40 und 80 mg/kg/Tag. In Übereinstimmung mit der Hemmung der HER-2-Phosphorylierung um 84 % innerhalb von 1 Stunde nach Verabreichung von 40 mg/kg/Tag hemmt diese Verbindung das Wachstum von BT474-Xenografts um 70-82 %, 67 % und 93 % bei Dosen von 5, 10 und 40 mg/kg/Tag. Es ist auch wirksam gegen SK-OV-3-Xenografts mit einer Hemmung von 31 % und 85 % bei 5 bzw. 60 mg/kg/Tag. Diese Chemikalie ist weniger potent gegen EGFR-abhängige A431-Xenografts als gegen HER-2-abhängige Tumoren, mit 32 % und 44 % Hemmung bei 5 bzw. 20 mg/kg/Tag. Sie zeigt wenig Aktivität gegen MCF-7- und MX-1-Xenografts, die niedrige Mengen an HER-2 und EGFR exprimieren, mit nur 28 % Hemmung bei 80 mg/kg/Tag, was darauf hindeutet, dass sie eine selektive Aktivität für Zellen aufweist, die HER-2 oder EGFR exprimieren. |
Protokoll (aus Referenz)
| Kinase-Assay:[1] |
|
|---|---|
| Zell-Assay:[1] |
|
| Tierstudie:[1] |
|
Referenzen
|
Kundenproduktvalidierung

-
Daten von [ Cancer Discov , 2013 , 3, 224-37 ]

-
Daten von [ Cancer Discov , 2012 , 2, 458-471 ]

-
Daten von [ Cancer Discov , 2012 , 2, 458-471 ]
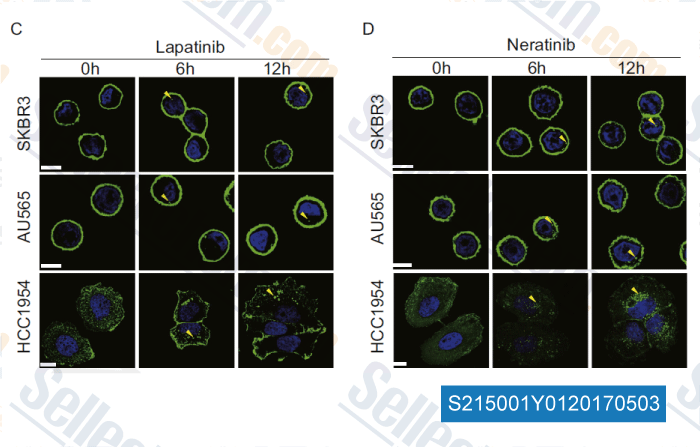
-
Daten von [ , , Cancer Lett, 2016, 382(2):176-185 ]
Sellecks Neratinib (HKI-272) Wurde zitiert von 116 Publikationen
| APOBEC3 mutagenesis drives therapy resistance in breast cancer [ Nat Genet, 2025, 57(6):1452-1462] | PubMed: 40379787 |
| Sevabertinib, a Reversible HER2 Inhibitor with Activity in Lung Cancer [ Cancer Discov, 2025, 10.1158/2159-8290.CD-25-0605] | PubMed: 41090369 |
| Small molecule kinase inhibitor altiratinib inhibits brain cyst forming bradyzoites of Toxoplasma gondii [ J Microbiol, 2025, 63(2):e2409001] | PubMed: 40044130 |
| KinoViz: A User-Friendly Web Application for High-Throughput Kinome Profiling Analysis and Visualization in Cancer Research [ Res Sq, 2025, rs.3.rs-6431257] | PubMed: 40630533 |
| Hotspot mutations in HER2 interfaces destabilize structure, causing breast cancer treatment failure [ Res Sq, 2025, rs.3.rs-5931887] | PubMed: 40166021 |
| Proteogenomic analysis dissects early-onset breast cancer patients with prognostic relevance [ Exp Mol Med, 2024, 56(11):2382-2394] | PubMed: 39482530 |
| Peptidylarginine deiminase 3 modulates response to neratinib in HER2 positive breast cancer [ Oncogenesis, 2024, 13(1):30] | PubMed: 39097594 |
| Patient-derived rhabdomyosarcoma cells recapitulate the genetic and transcriptomic landscapes of primary tumors [ iScience, 2024, 27(10):110862] | PubMed: 39319271 |
| Synergistic Effects of Neratinib in Combination With Palbociclib or Miransertib in Brain Cancer Cells [ World J Oncol, 2024, 15(3):492-505] | PubMed: 38751701 |
| The Combination of Afatinib With Dasatinib or Miransertib Results in Synergistic Growth Inhibition of Stomach Cancer Cells [ World J Oncol, 2024, 15(2):192-208] | PubMed: 38545471 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
