Technische Daten
| Formel | C17H15NO3 |
||||||
| Molekulargewicht | 281.31 | CAS-Nr. | 154447-35-5 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 1 mg/mL (3.55 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | NU7026 (LY293646) ist ein potenter DNA-PK-Inhibitor mit einer IC50 von 0,23 μM in zellfreien Assays, 60-fach selektiver für DNA-PK als PI3K und inaktiv gegen sowohl ATM als auch ATR. Diese Verbindung verstärkt den G2/M-Zellzyklusarrest und die Apoptose. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | NU7026 verstärkt die durch ionisierende Strahlung induzierte Zytotoxizität in einer konzentrationsabhängigen Weise in V3YAC- und PARP-1+/+-Zellen. Diese Verbindung hebt die Erholung von potenziell letalen Schäden in wachstumsgehemmten Zellen vollständig auf. Sie hemmt die DNA-DSB-Reparatur um 56 % in der V3YAC-Zelllinie. Diese Chemikalie (10 μM) verstärkt die wachstumshemmenden Wirkungen von Doxorubicin, mAMSA mit PF50-Werten von ungefähr 19 für mAMSA bis ungefähr 2 in K562-Zellen. Sie (10 μM) verstärkt auch die wachstumshemmende Wirkung in dieser Leukämiezelllinie mit einem PF50-Wert von 10,53. Diese Verbindung (10 μM) verstärkt die induzierte G2-Blockade des Zellzyklus in K562-Zellen. Sie verstärkt Topo-II-Gifte, die eine Hemmung der nicht-homologen Endverbindung und einen G2/M-Checkpoint-Arrest beinhalten. Diese Verbindung (10 μM) Exposition von 4 h in Kombination mit 3 Gy Strahlung ist für einen signifikanten radiosensibilisierenden Effekt in CH1 menschlichen Ovarialkarzinomzellen erforderlich. Es (< 10 μM) hat synergistische zytotoxische Aktivität bei nicht-toxischen Dosen dieser Chemikalie in einer CLL-Zelllinie (I83) und in primären CLL-Lymphozyten. Diese Verbindung (10 μM) erhöht den induzierten G(2)/M-Arrest in I83-Zellen. Es (10 μM) verstärkt das induzierte γH2AX während des gesamten Zellzyklus in der I83-Zelllinie. Diese Chemikalie (10 μM) erhöht die induzierte Apoptose in der I83-Zelllinie. Es (55 μM) führt zu einer dramatischen Induktion der Telomerfusion in p53-null MEFs und zu signifikant weniger Telomerfusionen in p53- und Ligase-IV-Doppel-null MEFs. |
||||
| In vivo | NU7026 (20 mg/kg, i.v.) wird bei Mäusen schnell aus dem Plasma eliminiert (0,108/Stunde), was größtenteils auf einen umfangreichen Metabolismus zurückzuführen ist. Die Bioverfügbarkeit nach interperitonealer (i.p.) und p.o. Verabreichung dieser Verbindung in einer Dosis von 20 mg/kg beträgt 20 bzw. 15 %. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
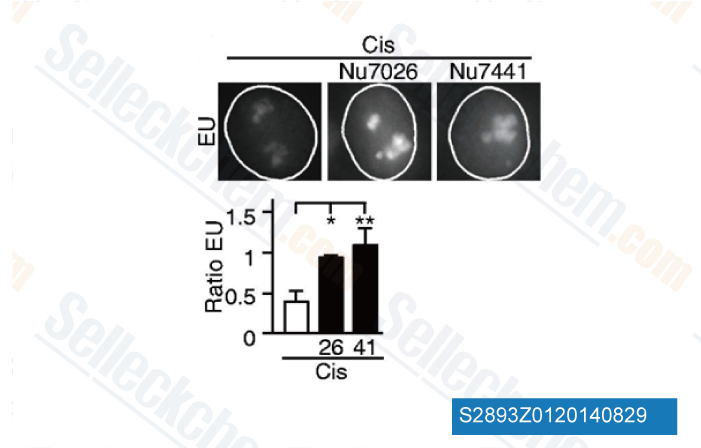
-
Daten von [ Nucleic Acids Res , 2013 , 41(15), 7378-86 ]
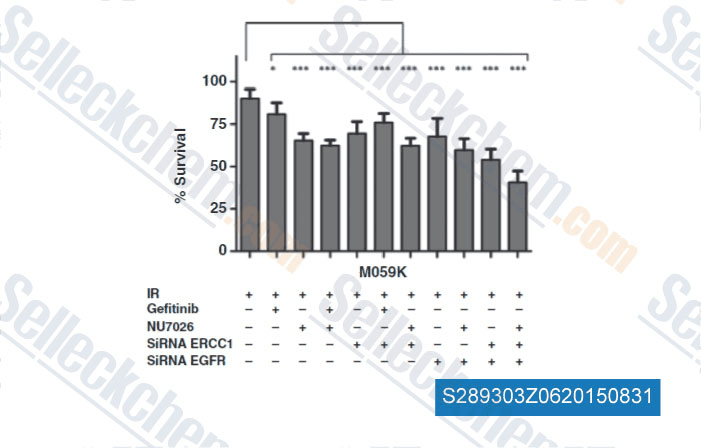
-
Daten von [ , , Clin Cancer Res, 2014, 20(13): 3496-50 ]

-
Daten von [ , , Nucleic Acids Res, 2016, 44(21):10259-10276 ]
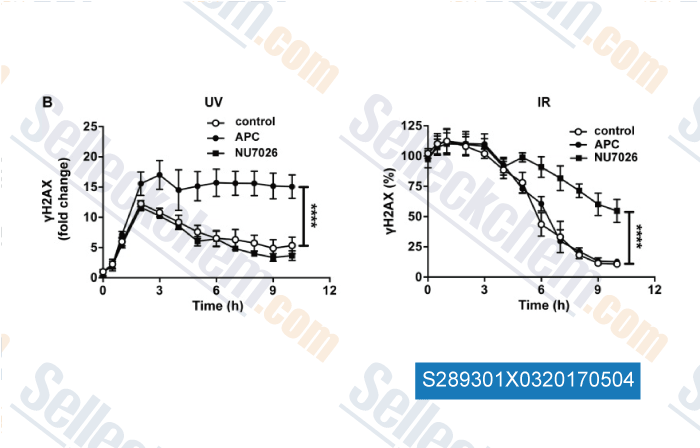
-
Daten von [ , , Oncotarget, 2016, 7(25):38367-38379 ]
Sellecks NU7026 Wurde zitiert von 71 Publikationen
| High-efficiency homology-directed insertion into the genome using the engineered homing endonuclease ARCUS [ Nucleic Acids Res, 2025, 53(18)gkaf961] | PubMed: 41047139 |
| Genome rearrangements induced by the stimulation of end-joining of DNA double strand breaks through multiple phosphorylation of MRE11 by the kinase PKB/AKT1 [ Nucleic Acids Res, 2025, 53(11)gkaf468] | PubMed: 40479710 |
| Noncanonical inhibition of topoisomerase II alpha by oxidative stress metabolites [ Redox Biol, 2025, 80:103504] | PubMed: 39879737 |
| TOX High-Mobility Group Box Family Member 4 promotes DNA double-strand break repair via nonhomologous end joining [ J Biol Chem, 2025, 301(6):110174] | PubMed: 40328361 |
| An open-source pipeline for calcium imaging and all-optical physiology in human stem cell-derived neurons [ bioRxiv, 2025, 2025.07.21.664988] | PubMed: 40777501 |
| Topoisomerase I is an evolutionarily conserved key regulator for satellite DNA transcription [ Nat Commun, 2024, 15(1):5151] | PubMed: 38886382 |
| LC3B drives transcription-associated homologous recombination via direct interaction with R-loops [ Nucleic Acids Res, 2024, gkae156] | PubMed: 38412240 |
| Generation and characterization of six human induced pluripotent stem cell lines (hiPSCs) from three individuals with SSADH Deficiency and CRISPR-corrected isogenic controls [ Stem Cell Res, 2024, 77:103424] | PubMed: 38677032 |
| Topoisomerase I is an Evolutionarily Conserved Key Regulator for Satellite DNA Transcription [ bioRxiv, 2024, 2024.05.03.592391] | PubMed: 38746280 |
| Blocking Genomic Instability Prevents Acquired Resistance to MAPK Inhibitor Therapy in Melanoma [ Cancer Discov, 2023, 13(4):880-909] | PubMed: 36700848 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
