Technische Daten
| Formel | C23H25ClN6O3 |
||||||||||
| Molekulargewicht | 468.94 | CAS-Nr. | 761437-28-9 | ||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 47 mg/mL (100.22 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | TAE226 (NVP-TAE226) ist ein potenter FAK-Inhibitor mit einer IC50 von 5,5 nM und mäßig potent gegenüber Pyk2, ~10- bis 100-fach weniger potent gegen InsR, IGF-1R, ALK und c-Met. Diese Verbindung induziert Apoptose. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ziele |
|
|||||||||||
| In vitro | TAE226 (NVP-TAE226) (< 1 μM) hemmt die extrazelluläre Matrix-induzierte Autophosphorylierung von FAK (Tyr397) in serumstarvierten U87-Zellen. Diese Verbindung (< 1 μM) hemmt auch die IGF-I-induzierte Phosphorylierung von IGF-1R und die Aktivität seiner nachgeschalteten Zielgene wie MAPK und Akt in U87- und U251-Zellen. Diese Chemikalie (<10 μM) verzögert das Wachstum von Tumorzellen und schwächt die G(2)-M-Zellzyklusprogression ab, die mit einer Abnahme der Cyclin B1- und phosphorylierten cdc2 (Tyr15)-Proteinexpression in U87- und U251-Zellen verbunden ist. Diese Verbindung (1 μM) hemmt die Tumorzellinvasion um mindestens 50 % im Vergleich zur Kontrolle in einem In-vitro-Matrigel-Invasionstest in Gliomzelllinien. Diese Chemikalie (1 μM) Behandlung von Gliomzelllinien, die Wildtyp-p53 enthalten, zeigt hauptsächlich einen G(2)-M-Arrest, während Gliomzelllinien, die mutiertes p53 tragen, Apoptose durchlaufen, wie durch den Nachweis von Caspase-3/7-Aktivierung und Poly(ADP-Ribose)-Polymerase-Spaltung und durch einen Annexin V Apoptosis Assay belegt wird. Diese Verbindung (5 μM) hemmt die Phosphorylierung von FAK in der menschlichen Neuroblastomzelllinie SK-N-AS. Diese Chemikalie (<10 μM) Behandlung der menschlichen Neuroblastomzelllinie SK-N-AS führt zu einer Abnahme der zellulären Viabilität, einem Zellzyklusarrest und einer Zunahme der Apoptose. Diese Verbindung (0,1 μM-10 μM) hemmt die Röhrenbildung von HMEC1-Zellen. | |||||||||||
| In vivo | TAE226 (NVP-TAE226) (75 mg/kg) erhöht die Überlebensrate von Mäusen mit intrakraniellen Gliom-Xenotransplantaten signifikant. Diese Verbindung (100 mg/kg, oral) bewirkt eine signifikante Abnahme der Mikrovaskulardichte in einem menschlichen Kolonkrebsmodell in SCID-Mäusen. Diese Chemikalie (100 mg/kg, oral) hemmt effizient das Wachstum von MIA PaCa-2 humanen Pankreastumoren ohne Gewichtsverlust im In-vivo-Modell. Es hemmt das Wachstum von 4T1 murinen Brusttumoren und die Metastasierung in die Lunge dosisabhängig im In-vivo-Modell, verbunden mit der Hemmung der FAK-Autophosphorylierung an Y397 und der Akt-Phosphorylierung an Serine473. |
Protokoll (aus Referenz)
| Zell-Assay:[1] |
|
|---|---|
| Tierstudie:[1] |
|
Referenzen
|
Kundenproduktvalidierung
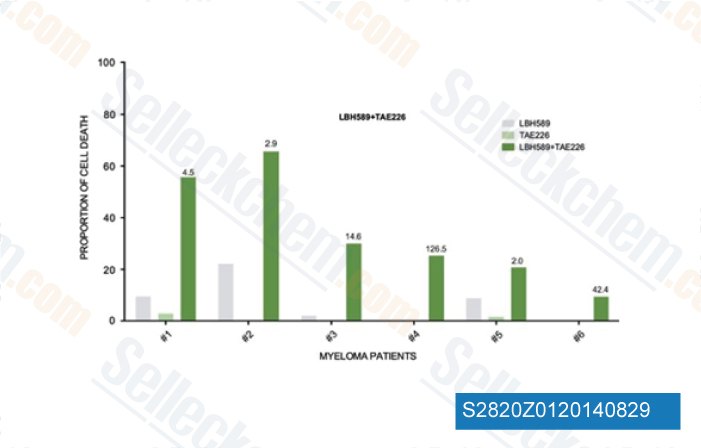
-
Daten von [ Cell Death Dis , 2014 , 5, e1134 ]
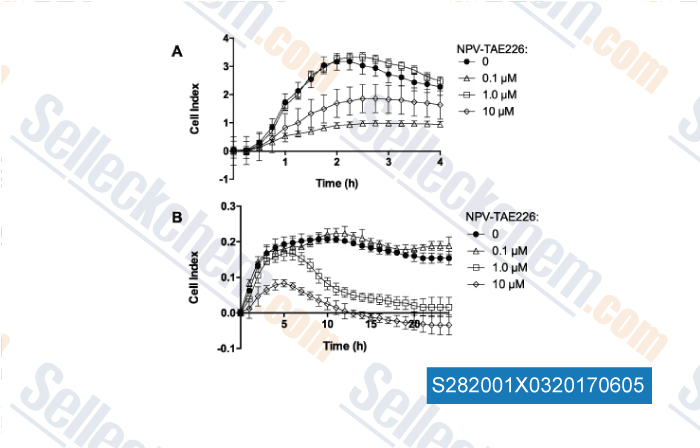
-
Daten von [ , , J Inorg Biochem, 2016, 160:225-35 ]
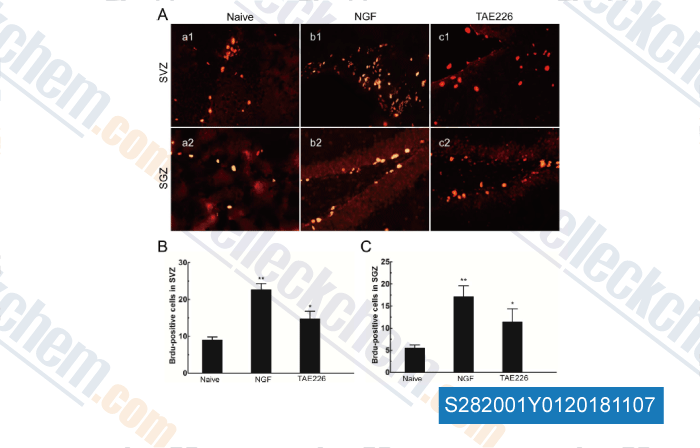
-
Daten von [ , , Neurosci Lett, 2018, 672:96-102 ]
Sellecks TAE226 (NVP-TAE226) Wurde zitiert von 26 Publikationen
| Aurora kinase A promotes epithelial‑mesenchymal transition by regulating P130 and P107 molecules in thyroid cancer cells [ Exp Ther Med, 2025, 29(5):93] | PubMed: 40162054 |
| Overexpression of BACH1 mediated by IGF2 facilitates hepatocellular carcinoma growth and metastasis via IGF1R and PTK2 [ Theranostics, 2022, 12(3):1097-1116] | PubMed: 35154476 |
| Mechanical coupling of supracellular stress amplification and tissue fluidization during exit from quiescence [ Proc Natl Acad Sci U S A, 2022, 119(32):e2201328119] | PubMed: 35914175 |
| Integrin αvβ3 Induces HSP90 Inhibitor Resistance via FAK Activation in KRAS-Mutant Non-Small Cell Lung Cancer [ Cancer Res Treat, 2022, 54(3):767-781] | PubMed: 34607394 |
| Three subtypes of lung cancer fibroblasts define distinct therapeutic paradigms [ Cancer Cell, 2021, S1535-6108(21)00492-X] | PubMed: 34624218 |
| TLR4 signalling via Piezo1 engages and enhances the macrophage mediated host response during bacterial infection [ Nat Commun, 2021, 12(1):3519] | PubMed: 34112781 |
| Focal adhesion kinase inhibition synergizes with nab-paclitaxel to target pancreatic ductal adenocarcinoma [ J Exp Clin Cancer Res, 2021, 91-2021)] | PubMed: None |
| Focal adhesion kinase inhibition synergizes with nab-paclitaxel to target pancreatic ductal adenocarcinoma [ J Exp Clin Cancer Res, 2021, 40(1):91] | PubMed: 33750427 |
| A first-in-class anticancer dual HDAC2/FAK inhibitors bearing hydroxamates/benzamides capped by pyridinyl-1,2,4-triazoles [ Eur J Med Chem, 2021, 222:113569] | PubMed: 34111829 |
| Campylobacter jejuni Triggers Signaling through Host Cell Focal Adhesions To Inhibit Cell Motility [ mBio, 2021, 12(4):e0149421] | PubMed: 34425711 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
