Technische Daten
| Formel | C13H11N3O4 |
||||||||||
| Molekulargewicht | 273.24 | CAS-Nr. | 19171-19-8 | ||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 55 mg/mL (201.28 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Pomalidomide hemmt die LPS-induzierte TNF-α-Freisetzung mit einer IC50 von 13 nM in PBMCs. Pomalidomide kann in PROTAC als Ligand zum Targeting von E3-Ligase und zur Hemmung des E3-Ligase-Proteins Cereblon (CRBN) eingesetzt werden. Pomalidomide fördert die Apoptose und den Zellzyklusarrest. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | Pomalidomide hemmt die durch Lipopolysaccharid (LPS) stimulierte TNF-alpha-Freisetzung in menschlichen PBMC und in menschlichem Vollblut mit IC50-Werten von 13 nM bzw. 25 nM. Diese Verbindung hemmt das Wachstum von durch IL-2 stimulierten T-regulatorischen Zellen mit einer IC50 von ~1 μM. Die Behandlung mit dieser Chemikalie (6,4 nM-10 μM) erhöht die Produktion von IL-2 in menschlichen peripheren Blut-T-Zellen und ist in der CD4+-Untergruppe etwas potenter als in der CD8+-Untergruppe. Es ist signifikant potenter als CC-5013 bei der Erhöhung von IL-2-, IL-5- und IL-10-Spiegeln, aber nur geringfügig potenter als CC-5013 bei der Erhöhung von IFN-γ-Spiegeln. Dieses Mittel verstärkt die SEE- und Raji-Zellen induzierte AP-1-Transkriptionsaktivität in Jurkat-Zellen dosisabhängig, mit einer maximalen Verstärkung von 4-fach bei 1 μM. Die Exposition von Raji-Zellen gegenüber verschiedenen Konzentrationen dieser Verbindung (2,5-40 μg/mL) über 48 Stunden führt zu einer signifikanten Abnahme der Zellproliferation und DNA-Synthese. Es gibt eine Reduktion von ~40% im Vergleich zu Vehikel-behandelten Kontrollen. |
||||
| In vivo | Pomalidomide verstärkt die Antitumorwirkung von Rituximab gegen B-Zell-Lymphome in Mäusen mit schwerem kombiniertem Immundefekt. Die Verabreichung dieser Verbindung in Kombination mit Rituximab verleiht den Mäusen eine mediane Überlebenszeit von 74 Tagen im Vergleich zu 58 Tagen bei CC5013/Rituximab-Behandlung und 45 Tagen bei Rituximab-Monotherapie. Der synergistische Effekt dieser Verbindung und Rituximab kann durch die Depletion von NK-Zellen vollständig aufgehoben werden, was die Annahme unterstützt, dass die Expansion von NK-Zellen ein Mechanismus ist, durch den diese Verbindung die Antitumoraktivität von Rituximab verstärken kann. |
||||
| Merkmale | Ein Derivat von Thalidomid und bis zu 10.000 Mal potenter als Thalidomid. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
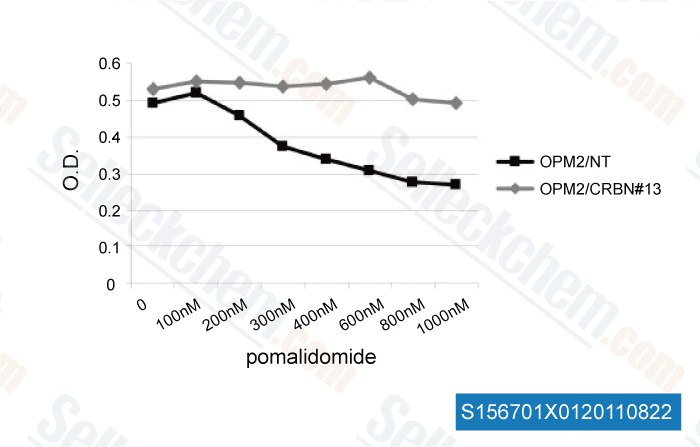
-
Daten von [ Blood , 2011 , 118, 4771-4779 ]
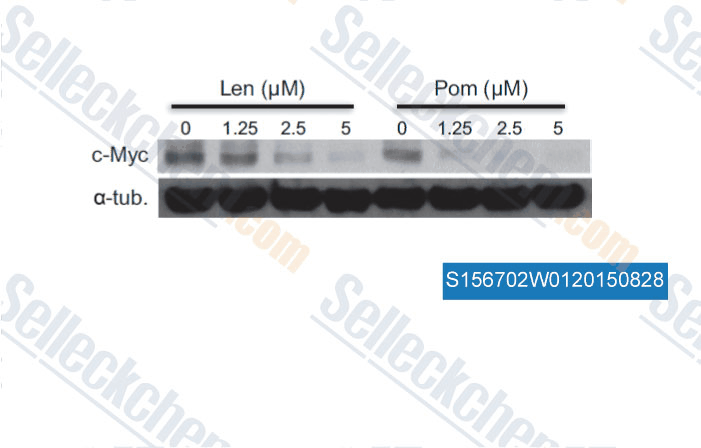
-
Daten von [ , , Blood Cancer Journal, 2015, 5: e312 ]
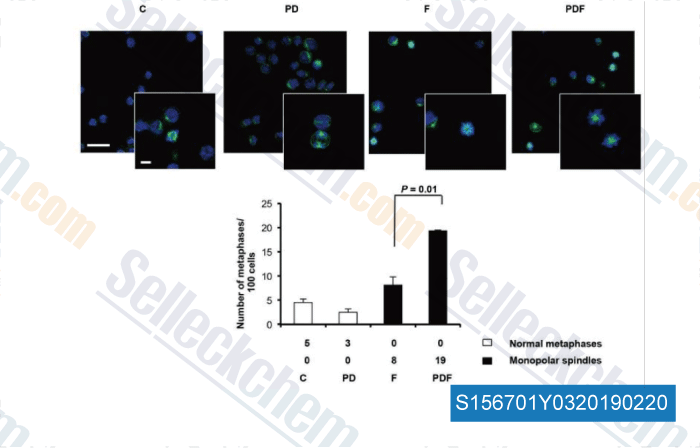
-
Daten von [ , , Haematologica, 2017, 102(12):2113-2124 ]
Sellecks Pomalidomide (CC-4047) Wurde zitiert von 124 Publikationen
| Systematic comparison and base-editing-mediated directed protein evolution and functional screening yield superior auxin-inducible degron technology [ Nat Commun, 2025, 16(1):6631] | PubMed: 40681502 |
| A patient-derived T cell lymphoma biorepository uncovers pathogenetic mechanisms and host-related therapeutic vulnerabilities [ Cell Rep Med, 2025, S2666-3791(25)00102-8] | PubMed: 40147445 |
| Novel Cereblon-Binding Immunomodulators Have Increased Potency Against Gammaherpesvirus- Associated Lymphomas In Vitro [ J Med Virol, 2025, 97(8):e70537] | PubMed: 40767544 |
| The Prolonged Half-Life of the p53 Missense Variant R248Q Promotes Accumulation and Heterotetramer Formation with Wildtype p53 to Exert the Dominant-Negative Effect [ Cancer Res, 2025, 10.1158/0008-5472.CAN-24-1136] | PubMed: 40163352 |
| Controlling CRISPR-Cas9 genome editing in human cells using a molecular glue degrader [ Mol Ther Nucleic Acids, 2025, 36(3):102640] | PubMed: 40799508 |
| Enhancing T cell cytotoxicity in multiple myeloma with bispecific αPD-L1 × αCD3 T cell engager-armed T cells and low-dose bortezomib therapy [ Biomed Pharmacother, 2025, 184:117878] | PubMed: 39891948 |
| Discovery of Novel, Potent, and Orally Bioavailable SMARCA2 Proteolysis-Targeting Chimeras with Synergistic Antitumor Activity in Combination with Kirsten Rat Sarcoma Viral Oncogene Homologue G12C Inhibitors [ J Med Chem, 2025, 68(9):9202-9219] | PubMed: 40280558 |
| Pharmacologically induced proteolysis of histone deacetylase-6 attenuates influenza virus replication despite limited anti-tumor effects [ Life Sci, 2025, 363:123401] | PubMed: 39814129 |
| Rapid and high-throughput screening of proteolysis targeting chimeras using a dual-reporter system expressing fluorescence protein and luciferase [ BMC Biol, 2025, 23(1):51] | PubMed: 39985000 |
| Role of Rac1 in p53-Related Proliferation and Drug Sensitivity in Multiple Myeloma [ Cancers (Basel), 2025, 17(3)461] | PubMed: 39941828 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
