Technische Daten
| Formel | C38H38N4O6 |
||||||||||
| Molekulargewicht | 646.73 | CAS-Nr. | 206873-63-4 | ||||||||
| Löslichkeit (25°C)* | In vitro | DMSO | 5.6 mg/mL (8.65 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Tariquidar ist ein potenter und selektiver nichtkompetitiver Inhibitor von P-Glykoprotein mit einem Kd von 5,1 nM in der CHrB30-Zelllinie, der die Arzneimittelresistenz in MDR-Zelllinien umkehrt. Phase 3. | ||
|---|---|---|---|
| Ziele |
|
||
| In vitro | Tariquidar zeigt eine hochaffine Bindung an P-gp mit einem Bmax von 275 pmol/mg. Diese Verbindung zeigt eine nicht-kompetitive Interaktion mit den P-gp-Substraten. Es erhöht die Steady-State-Akkumulation dieser Zytotoxika in CHrB30-Zellen auf Werte, die in nicht-P-gp-exprimierenden AuxB1-Zellen beobachtet werden, mit einer EC50 von 487 nM. Diese Chemikalie ist in der Lage, die Vanadat-sensitive ATPase-Aktivität von P-gp um 60-70% zu hemmen, mit potenten IC50-Werten von 43 nM. Bei höheren Konzentrationen kann es andere Resistenzmechanismen hemmen. 1 µM dieser Verbindung hebt die ABCG2 (BCRP)-vermittelte Resistenz gegen Camptothecine in vitro auf. Es verstärkt die Zytotoxizität mehrerer Medikamente, einschließlich Doxorubicin; eine vollständige Umkehr der Resistenz wird in Gegenwart von 25-80 nM dieser Chemikalie erreicht. In MC26, einer murinen Kolonkarzinom-Zelllinie mit intrinsischer Chemoresistenz, ist die Doxorubicin-IC50 in Gegenwart von 0,1 µM dieser Verbindung fünfmal niedriger (36 vs. 7 nM). In murinen Mammakarzinom-, humanen kleinzelligen Lungenkarzinom- und humanen Ovarialkarzinom-Zelllinien mit erworbener Chemotherapieresistenz (EMT6/AR1.0, H69/LX4 und 2780 AD) ist die In-vitro-Doxorubicin-IC50 in Gegenwart von 0,1 µM dieser Chemikalie 22-150-fach niedriger. Die P-gp-Hemmung bleibt 23 Stunden nach der Entfernung aus dem Kultursystem bestehen. Es stellte die Zytotoxizität von Doxorubicin im National Cancer Institute (NCI)/ADRRES multizellulären Tumorsphäroidmodell wieder her, das von der MCF7WT Brustkrebszelllinie abgeleitet wurde. |
||
| In vivo | Tariquidar (2-8 mg/kg p.o.) verstärkt nachweislich signifikant die Antitumoraktivität von Doxorubicin (5 mg/kg, i.v.) gegen MC26-Mauskolonkarzinome in vivo. In menschlichen Karzinom-Xenotransplantaten stellte die gleichzeitige Verabreichung dieser Verbindung (6-12 mg/kg p.o.) die Antitumoraktivität gegen zwei hochresistente MDR-menschliche Tumor-Xenotransplantate (2780AD, H69/LX4) in Nacktmäusen vollständig wieder her. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
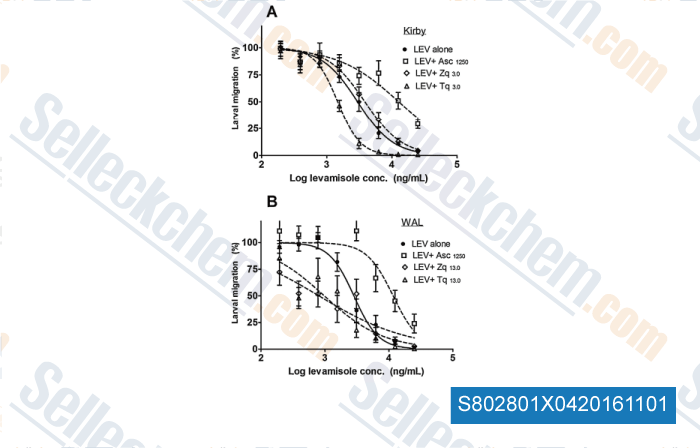
-
, , Vet Parasitol, 2015, 211(1-2):80-8.
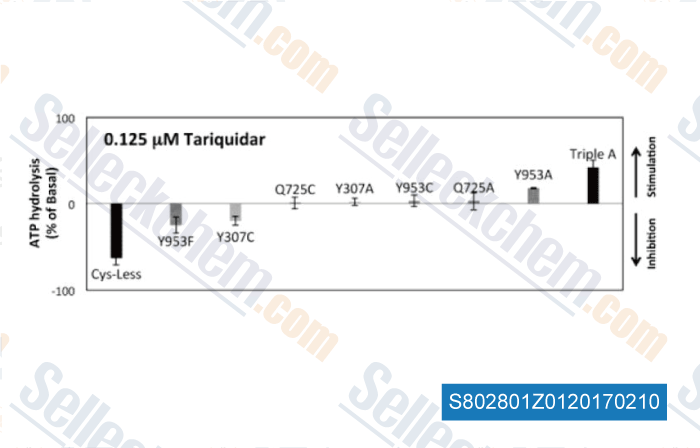
-
Daten von [ , , Biochem Pharmacol, 2016, 101:40-53. ]
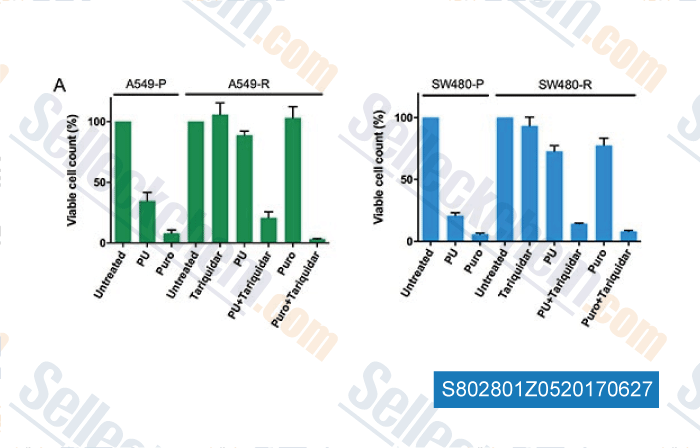
-
Daten von [ , , Oncotarget, 2017, 8(5):7678-7690 ]
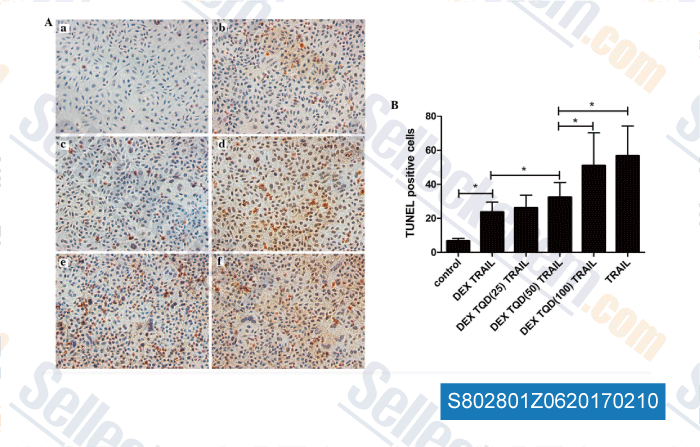
-
Daten von [ , , Mol Med Rep, 2015, 12(6):8093-100. ]
Sellecks Tariquidar (XR9576) Wurde zitiert von 55 Publikationen
| Identification of the Notch ligand DLK1 as an immunotherapeutic target and regulator of tumor cell plasticity and chemoresistance in adrenocortical carcinoma [ Nat Commun, 2025, 16(1):5511] | PubMed: 40595495 |
| Mitochondrial dysfunction fuels drug resistance in adult T-cell acute lymphoblastic leukemia [ J Transl Med, 2025, 23(1):542] | PubMed: 40369632 |
| Fibroblasts Attenuate Anti-Tumor Drug Efficacy in Tumor Cells via Paracrine Interactions with Tumor Cells in 3D Plexiform Neurofibroma Cultures [ Cells, 2025, 14(16)1276] | PubMed: 40862755 |
| Low-Dose Perifosine, a Phase II Phospholipid Akt Inhibitor, Selectively Sensitizes Drug-Resistant ABCB1-Overexpressing Cancer Cells [ Biomol Ther (Seoul), 2025, 33(1):170-181] | PubMed: 39632683 |
| Tumor-acquired somatic mutation affects conformation to abolish ABCG2-mediated drug resistance [ Drug Resist Updat, 2024, 73:101066] | PubMed: 38387283 |
| Enhanced anticancer effect of thymidylate synthase dimer disrupters by promoting intracellular accumulation [ Front Pharmacol, 2024, 15:1477318] | PubMed: 39611169 |
| Zosuquidar: An Effective Molecule for Intracellular Ca2+ Measurement in P-gp Positive Cells [ Int J Mol Sci, 2024, 25(6)3107] | PubMed: 38542082 |
| Cellular uptake of CPX-351 by scavenger receptor class B type 1-mediated nonendocytic pathway [ Exp Hematol, 2024, S0301-472X(24)00516-2] | PubMed: 39362576 |
| Ivermectin Enhances Paclitaxel Efficacy by Overcoming Resistance Through Modulation of ABCB1 in Non-small Cell Lung Cancer [ Anticancer Res, 2024, 44(12):5271-5282] | PubMed: 39626921 |
| The net electrostatic potential and hydration of ABCG2 affect substrate transport [ Nat Commun, 2023, 14(1):5035] | PubMed: 37596258 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
