Technische Daten
| Formel | C26H23FIN5O4 |
||||||
| Molekulargewicht | 615.39 | CAS-Nr. | 871700-17-3 | ||||
| Löslichkeit (25°C)* | In vitro | DMSO | 22 mg/mL (35.74 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Lösungsmittel einzeln und der Reihe nach zum Produkt hinzufügen.) |
|
||||||
|
* <1 mg/ml bedeutet schwer löslich oder unlöslich. * Bitte beachten Sie, dass Selleck die Löslichkeit aller Verbindungen intern testet und die tatsächliche Löslichkeit geringfügig von veröffentlichten Werten abweichen kann. Dies ist normal und ist auf geringfügige Batch-zu-Batch-Variationen zurückzuführen. * Versand bei Raumtemperatur (Stabilitätstests zeigen, dass dieses Produkt ohne Kühlmaßnahmen versendet werden kann.) |
|||||||
Vorbereitung von Stammlösungen
Biologische Aktivität
| Beschreibung | Trametinib (GSK1120212, JTP-74057) ist ein hochspezifischer und potenter MEK1/2-Inhibitor mit einer IC50 von 0,92 nM/1,8 nM in zellfreien Assays, und es hemmt die Kinaseaktivitäten von c-Raf, B-Raf, ERK1/2 nicht. Diese Verbindung aktiviert die Autophagy und induziert Apoptosis. | ||||
|---|---|---|---|---|---|
| Ziele |
|
||||
| In vitro | Trametinib (GSK1120212) hemmt die Phosphorylierung von MBP unabhängig vom Isotyp von Raf und MEK, mit IC50-Werten im Bereich von 0,92 nM bis 3,4 nM. Es zeigt keine Hemmung der Kinaseaktivitäten von c-Raf, B-Raf, ERK1 und ERK2. Darüber hinaus zeigt diese Verbindung keine drastische Hemmwirkung gegen die anderen 98 Kinasen. Es zeigt eine starke hemmende Aktivität gegen humane kolorektale Krebszelllinien. HT-29- und COLO205-Zellen, die bekanntermaßen eine konstitutiv aktive B-Raf-Mutante aufweisen, sind mit IC50 0,48 nM bzw. 0,52 nM am empfindlichsten. Die Zelllinien, die eine K-Ras-Mutation aufweisen, zeigen eine große Bandbreite an Empfindlichkeit gegenüber ihm mit IC50 von 2,2-174 nM. Im Gegensatz dazu sind COLO320 DM-Zellen, die das Wildtyp-Gen sowohl in B-Raf als auch in K-Ras tragen, selbst bei 10 μM resistent. Eine 24-stündige Behandlung induziert einen Zellzyklusarrest in der G1-Phase in allen empfindlichen Zelllinien. Konsistenterweise führt dies zu einer Hochregulation von p15INK4b und/oder p27KIP1 in den meisten kolorektalen Krebszelllinien. Es hemmt die konstitutive ERK-Phosphorylierung in allen empfindlichen Zelllinien. Diese Verbindung induziert Apoptosis sowohl in HT-29- als auch in COLO205-Zellen, wobei COLO205-Zellen hinsichtlich der Apoptosis-Induktion empfindlicher sind als HT-29-Zellen. Es blockiert die Produktion von Tumornekrosefaktor-α und Interleukin-6 aus peripheren mononukleären Blutzellen (PBMCs). |
||||
| In vivo | Die orale Verabreichung von Trametinib (GSK1120212) mit 0,3 mg/kg oder 1 mg/kg einmal täglich über 14 Tage ist wirksam bei der Hemmung des HT-29-Xenograft-Wachstums, und 1 mg/kg dieser Verbindung blockiert den Tumorzuwachs fast vollständig. Die Phosphorylierung von ERK1/2 ist in den etablierten Tumorgeweben durch eine einzelne orale Dosis von 1 mg/kg vollständig gehemmt, und sowohl die p15INK4b- als auch die p27KIP1-Proteinspiegel sind nach 14-tägiger Behandlung hochreguliert. Im COLO205-Xenograft-Modell wird eine Tumorregression selbst bei einer Dosis von 0,3 mg/kg beobachtet. Bei einer Dosis von 1 mg/kg wird eine vollständige Regression bei 4 von 6 Mäusen erreicht, bei denen sich der Tumor so weit zurückbildet, dass das Tumorvolumen nicht messbar ist. Die Verabreichung von 0,1 mg/kg unterdrückt die adjuvansinduzierte Arthritis (AIA) und die Typ-II-Kollagen-induzierte Arthritis (CIA) bei Lewis-Ratten bzw. DBA1/J-Mäusen fast vollständig. |
||||
| Merkmale | Wirksamer als PD0325901 oder AZD6244. |
Protokoll (aus Referenz)
| Kinase-Assay: |
|
|---|---|
| Zell-Assay: |
|
| Tierstudie: |
|
Referenzen
|
Kundenproduktvalidierung
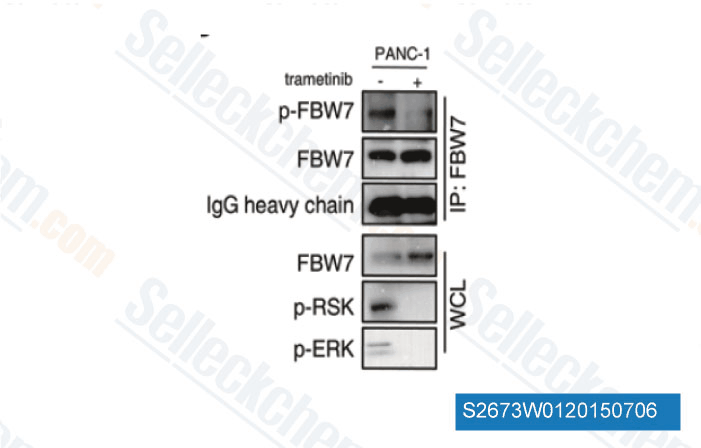
-
Daten von [ Cell Res , 2015 , 25(5), 561-73 ]

-
Daten von [ Nat Commun , 2015 , 5, 5694 ]
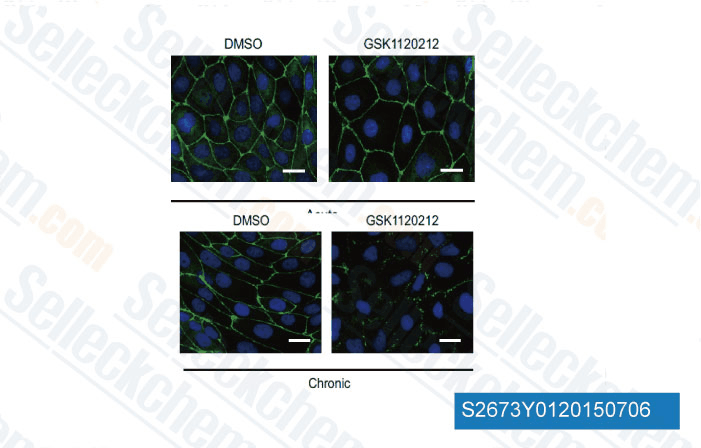
-
Daten von [ EMBO Rep , 2015 , 16(1), 87-96 ]
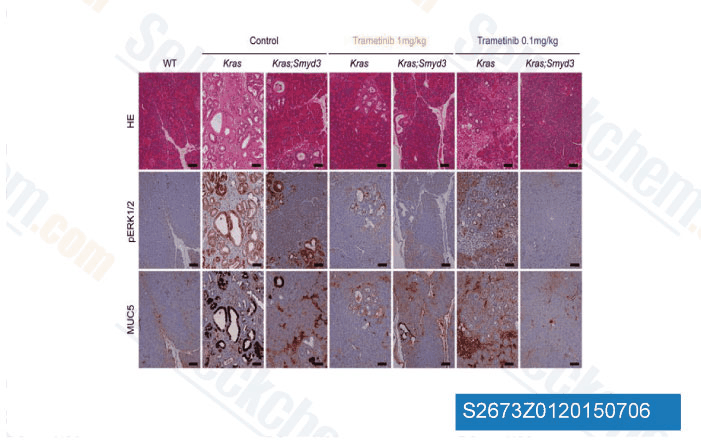
-
Daten von [ Nature , 2014 , 510(7504), 283-7 ]
Sellecks Trametinib (GSK1120212) Wurde zitiert von 1397 Publikationen
| Macropinocytosis maintains CAF subtype identity under metabolic stress in pancreatic cancer [ Cancer Cell, 2025, S1535-6108(25)00271-5] | PubMed: 40712568 |
| Anti-BCL2 therapy eliminates giant congenital melanocytic nevus by senolytic and immune induction [ Signal Transduct Target Ther, 2025, 10(1):161] | PubMed: 40374605 |
| Coinhibition of the MEK/RTK pathway has high therapeutic efficacy in KRAS-mutant non-small cell lung cancer [ Signal Transduct Target Ther, 2025, 10(1):299] | PubMed: 40935839 |
| Whole-exome tumor-agnostic ctDNA analysis enhances minimal residual disease detection and reveals relapse mechanisms in localized colon cancer [ Nat Cancer, 2025, 10.1038/s43018-025-00960-z] | PubMed: 40301653 |
| Pan-inhibition of super-enhancer-driven oncogenic transcription by next-generation synthetic ecteinascidins yields potent anti-cancer activity [ Nat Commun, 2025, 16(1):512] | PubMed: 39779693 |
| Loss of tumor cell MHC Class II drives MAPK-inhibitor insensitivity of BRAF-mutant anaplastic thyroid cancers [ J Clin Invest, 2025, e191781] | PubMed: 40828595 |
| EGFR TKIs suppress MUC1 glycosylation through the PI3K/AKT/SP1/C1GALT1 pathway to enhance TnMUC1 CAR-T efficacy in EGFR-mutant NSCLC [ Cell Rep Med, 2025, S2666-3791(25)00272-1] | PubMed: 40562040 |
| BRAF/MEK inhibition induces cell state transitions boosting immune checkpoint sensitivity in BRAFV600E-mutant glioma [ Cell Rep Med, 2025, 6(6):102183] | PubMed: 40505659 |
| System analysis links SMARCD3 regulons to growth signaling and MEK inhibitor response in everolimus-resistant ER+ breast cancer cells [ Cell Rep Med, 2025, 6(11):102425] | PubMed: 41260207 |
| Combined MEK and PARP inhibition enhances radiation response in rectal cancer [ Cell Rep Med, 2025, 6(8):102284] | PubMed: 40782795 |
RÜCKGABERICHTLINIE
Die bedingungslose Rückgaberichtlinie von Selleck Chemical gewährleistet unseren Kunden ein reibungsloses Online-Einkaufserlebnis. Wenn Sie in irgendeiner Weise mit Ihrem Kauf unzufrieden sind, können Sie jeden Artikel innerhalb von 7 Tagen nach Erhalt zurückgeben. Im Falle von Produktqualitätsproblemen, sei es protokollbezogene oder produktbezogene Probleme, können Sie jeden Artikel innerhalb von 365 Tagen ab dem ursprünglichen Kaufdatum zurückgeben. Bitte befolgen Sie die nachstehenden Anweisungen, wenn Sie Produkte zurücksenden.
VERSAND UND LAGERUNG
Selleck-Produkte werden bei Raumtemperatur transportiert. Wenn Sie das Produkt bei Raumtemperatur erhalten, seien Sie versichert, dass die Qualitätskontrollabteilung von Selleck Experimente durchgeführt hat, um zu überprüfen, dass die normale Temperaturplatzierung von einem Monat die biologische Aktivität von Pulverprodukten nicht beeinträchtigt. Nach dem Sammeln lagern Sie das Produkt bitte gemäß den in der Datenblatt beschriebenen Anforderungen. Die meisten Selleck-Produkte sind unter den empfohlenen Bedingungen stabil.
NICHT FÜR DIE ANWENDUNG AM MENSCHEN, FÜR VETERINÄRMEDIZINISCHE DIAGNOSTIK ODER THERAPEUTISCHE ZWECKE.
