réservé à la recherche
Tomivosertib (eFT508) Inhibiteur de MNK1/2
N° Cat.S8275
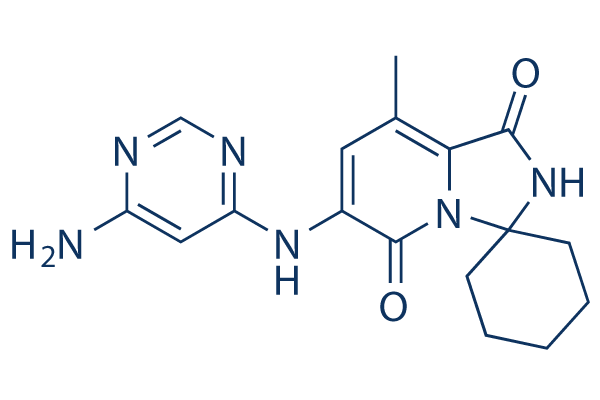
Structure chimique
Poids moléculaire: 340.38
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- SDS
- Fiche technique
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| TMD8 | Function assay | 0.01, 0.1, 1, 3 and 10 μM | 2 h | potent dose-dependent inhibition of eIF4E Ser209 phosphorylation | 29526098 | |
| TMD8 | Proliferation assay | 12 h | IC50=2.53 μM | 30824167 | ||
| MV4-11 | Proliferation assay | 12 h | IC50=14.49 μM | 30824167 | ||
| K562 | Proliferation assay | 12 h | IC50=13.54 μM | 30824167 | ||
| Vero E6 | Antiviral assay | 48 h | IC50 for antiviral activity against SARS-CoV-2 in the Vero E6 cell line at 48 h by immunofluorescence-based assay (detecting the viral NP protein in the nucleus of the Vero E6 cells)., IC50 = 0.34674 μM. | 32353859 | ||
| Cliquez pour voir plus de données expérimentales sur les lignées cellulaires | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 340.38 | Formule | C17H20N6O2 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 1849590-01-7 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CC1=C2C(=O)NC3(N2C(=O)C(=C1)NC4=NC=NC(=C4)N)CCCCC3 | ||
Solubilité
|
In vitro |
DMSO
: 13 mg/mL
(38.19 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
MNK2
(Cell-free assay) 1 nM
MNK1
(Cell-free assay) 2.4 nM
|
|---|---|
| In vitro |
Le Tomivosertib (eFT-508) a une concentration inhibitrice semi-maximale (IC50) de 1-2 nM contre les deux isoformes de MNK dans les essais enzymatiques et inhibe la kinase via un mécanisme d'action réversible et compétitif de l'ATP. Le traitement des lignées cellulaires tumorales avec ce composé entraîne une réduction dose-dépendante de la phosphorylation de l'eIF4E à la sérine 209 (IC50 = 2-16 nM). Dans un panel d'environ 50 cancers hématologiques, ce produit chimique montre une activité anti-proliférative contre plusieurs lignées cellulaires de DLBCL. La sensibilité à ce composé dans les lignées cellulaires de DLBCL TMD8, OCI-Ly3 et HBL1 est associée à des diminutions dose-dépendantes de la production de cytokines pro-inflammatoires, notamment le TNFα, l'IL-6, l'IL-10 et le CXCL10. |
| In vivo |
Le Tomivosertib (eFT-508) est bien toléré et montre une efficacité contre les modèles de DLBCL mutés MyD88 in vivo. Une activité antitumorale significative de ce composé est observée dans les modèles TMD8 et HBL-1 ABC-DLBCL (modèles de xénogreffe de lymphome humain sous-cutané), qui contiennent tous deux des mutations activatrices de MyD88.
|
Références |
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | p-eIF4E |
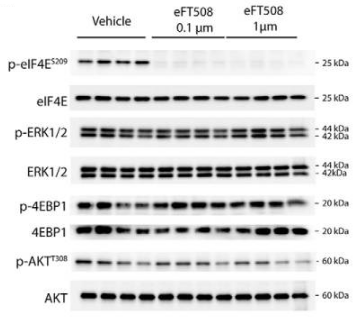
|
30459229 |
| Growth inhibition assay | Cell viability |
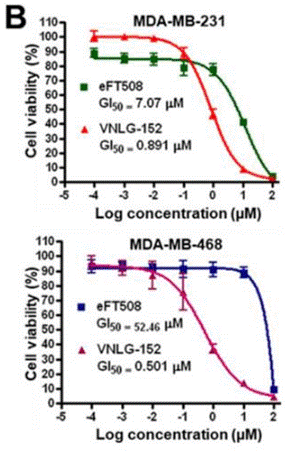
|
30832411 |
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT05744739 | Recruiting | Acute Myeloid Leukemia |
Northwestern University|National Cancer Institute (NCI)|EFFECTOR Therapeutics Inc. |
September 29 2023 | Phase 1 |
| NCT04261218 | Completed | Breast Cancer |
Translational Research in Oncology|Effector Therapeutics|Stand Up To Cancer |
August 25 2020 | Phase 1 |
| NCT02937675 | Terminated | Lymphoma |
Effector Therapeutics |
February 8 2017 | Phase 1|Phase 2 |
| NCT02605083 | Terminated | Cancer |
Effector Therapeutics |
December 3 2015 | Phase 1|Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
