réservé à la recherche
GW0742 PPAR agoniste
N° Cat.S8020
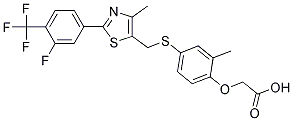
Structure chimique
Poids moléculaire: 471.49
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- SDS
- Fiche technique
| Cibles apparentées | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Autre PPAR Inhibiteurs | T0070907 GW9662 GW6471 WY-14643 (Pirinixic Acid) GSK3787 AZ6102 Harmine Astaxanthin Eupatilin GSK0660 |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| CV-1 cells | Function assay | 24 h | Agonist activity at mouse PPAR-alpha expressed in african green monkey CV-1 cells after 24 hrs by luciferase reporter gene assay | |||
| HEK293 cells | Function assay | Transactivation of PPARdelta (unknown origin) expressed in HEK293 cells co-transfected with PDK4-PPRE by luciferase reporter gene assay | ||||
| C2C12 cells | Function assay | 4 days | Agonist activity at PPARdelta in mouse C2C12 cells assessed as upregulation of TFAM gene expression after 4 days by real time PCR analysis | |||
| Cliquez pour voir plus de données expérimentales sur les lignées cellulaires | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 471.49 | Formule | C21H17F4NO3S2 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 317318-84-6 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CC1=C(C=CC(=C1)SCC2=C(N=C(S2)C3=CC(=C(C=C3)C(F)(F)F)F)C)OCC(=O)O | ||
Solubilité
|
In vitro |
DMSO
: 94 mg/mL
(199.36 mM)
Ethanol : 44 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Fonctionnalités |
Both GW0742 and L-165041 activate PPARβ, but not PPARγ or PPARα in platelets.
|
|---|---|
| Targets/IC50/Ki |
PPARδ
1 nM(EC50)
|
| In vitro |
GW0742 montre une activité contre hPPAR
lpha, hPPAR
lgamma et hPPAR
l
delta avec des EC50 de 1,1
l
l
l
M, 2
l
l
l
M et 1 nM, respectivement, dans un test de transactivation basé sur des cellules. Ce composé (0,2
l
l
l
M et 1
l
l
l
M) augmente significativement l'activité rapporteur de PPAR
lbeta/
l
delta dans les kératinocytes N/TERT-1. Il (1
l
l
l
M) entraîne une inhibition significative du nombre moyen de kératinocytes N/TERT-1. La substance chimique (1
l
l
l
M) entraîne une augmentation du nombre de cellules en phase G1 et une diminution du nombre de cellules en phase S. Elle (1
l
l
l
M) provoque une augmentation significative de l'ARNm codant pour l'ADRP, un gène cible connu de PPAR
lbeta/
l
delta, dans les kératinocytes N/TERT-1 ainsi que dans les kératinocytes primaires de souris. Cet agent (1
l
l
l
M) entraîne une phosphorylation significativement réduite du rétinoblastome (Rb) et un niveau significativement plus faible de p42/44 ERK dans les cellules N/TERT-1. Il (1
l
l
l
M) conduit à une augmentation de l'ARNm codant pour un certain nombre de marqueurs connus de différenciation terminale, y compris TG-I, SPR1A, K10 et l'involucrine. Ce composé à 100
l
l
l
M produit une réduction significative de la mort neuronale induite par un faible taux de KCl dans les neurones granulaires du cervelet. Il à 100
l
l
l
M induit une augmentation prononcée de la mort cellulaire, mesurée par la libération de LDH après 48 heures d'incubation. La substance chimique à 100
l
l
l
M produit une augmentation prononcée de l'expression de c-Jun à 6 heures dans les cultures de neurones granulaires du cervelet. Il à 100
l
l
l
M augmente la transactivation médiée par PPAR
lpha, dépendante de la présence de 1,5% de BSA dans les cellules MCF-7.
|
| In vivo |
GW0742 (10 mg/kg) favorise le transport inverse du cholestérol chez les souris C57BL6/J. Ce composé (10 mg/kg) augmente l'excrétion fécale du cholestérol dérivé du HDL, malgré l'absence d'effet sur le catabolisme du cholestérol HDL chez les souris C57BL6/J. Il diminue l'expression de l'ARNm de NPC1L1 dans l'intestin grêle des souris. Cette substance chimique (30 mg/kg), avant l'induction de l'inflammation pulmonaire médiée par le LPS, entraîne une diminution significative du recrutement des leucocytes dans l'espace pulmonaire chez les souris mâles BALB/c. Elle (30 mg/kg) diminue significativement les niveaux de protéines et d'ARNm des cytokines pro-inflammatoires IL-6, IL-1beta et TNF
lpha dans le liquide de lavage bronchoalvéolaire des souris.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
