réservé à la recherche
Methotrexate disodium DHFR inhibiteur
N° Cat.S5097
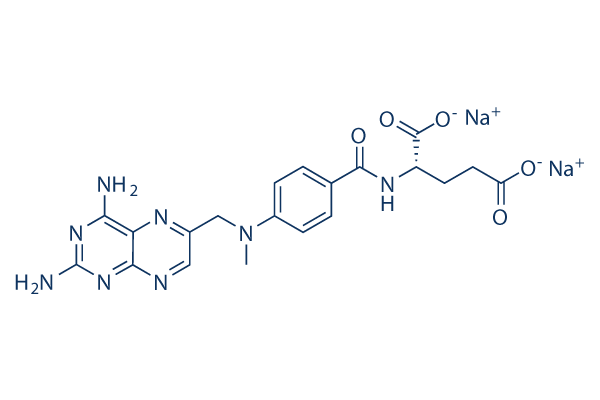
Structure chimique
Poids moléculaire: 498.4
Contrôle qualité
| Cibles apparentées | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Autre DHFR Inhibiteurs | Calcium Folinate Aminopterin Diaveridine |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 498.4 | Formule | C20H20N8O5.2Na |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 7413-34-5 | -- | Stockage des solutions mères |
|
|
| Synonymes | Amethopterin disodium; CL14377 disodium; WR19039 disodium | Smiles | CN(CC1=CN=C2C(=N1)C(=NC(=N2)N)N)C3=CC=C(C=C3)C(=O)NC(CCC(=O)[O-])C(=O)[O-].[Na+].[Na+] | ||
Solubilité
|
In vitro |
Water : 99 mg/mL
DMSO
: Insoluble
|
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
hDHFR
(Activated peripheral T cells) 24 nM
|
|---|---|
| In vitro |
Methotrexate (0,1-10 mM) induit l'apoptose des lymphocytes T activés in vitro provenant du sang périphérique humain. Methotrexate réalise la délétion clonale des lymphocytes T activés dans les réactions lymphocytaires mixtes. Methotrexate peut éliminer sélectivement les lymphocytes T activés du sang périphérique par une voie indépendante de CD95. Methotrexate est capté par les cellules via le transporteur de folate réduit et est ensuite converti en polyglutamates à l'intérieur des cellules. Methotrexate entraîne une production diminuée de leucotriène B4 par les neutrophiles stimulés ex vivo. Les polyglutamates de Methotrexate inhibent l'enzyme aminoimidazolecarboxamidoadenosineribonucleotide (AICAR) transformylase plus puissamment que les autres enzymes impliquées dans la biosynthèse des purines. Methotrexate est également connu pour supprimer l'activité du TNF en supprimant l'activation du facteur nucléaire-κB induite par le TNF in vitro, en partie liée à une réduction de la dégradation et de l'inactivation d'un inhibiteur de ce facteur, IκBα, et probablement liée à la libération d'adénosine. Methotrexate supprime la production de TNF et d'IFN-γ par les lymphocytes T amorcés par le récepteur des cellules T provenant de donneurs humains sains et de patients atteints de PR. Le traitement par Methotrexate est associé à une diminution significative des lymphocytes T CD4+ positifs au TNF-α, tandis que le nombre de lymphocytes T exprimant la cytokine anti-inflammatoire IL-10 a augmenté.
|
| In vivo |
Le Methotrexate augmente le contenu en AICAR des splénocytes, augmente les concentrations d'adénosine dans les exsudats de poches aériennes enflammées par la carragénine, et inhibe de manière marquée l'accumulation de leucocytes dans les poches aériennes enflammées chez les souris. La réduction de l'accumulation de leucocytes médiatisée par le Methotrexate est partiellement inversée par l'injection d'adénosine désaminase (ADA) dans la poche aérienne, complètement inversée par un antagoniste spécifique du récepteur A2 de l'adénosine, la 3,7-diméthyl-1-propargylxanthine (DMPX), mais n'est pas affectée par un antagoniste du récepteur A1 de l'adénosine, la 8-cyclopentyl-dipropylxanthine chez les souris.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
