réservé à la recherche
RO4929097 (RG-4733) inhibiteur de γ-Secretase
N° Cat.S1575
Structure chimique
Poids moléculaire: 469.4
Contrôle qualité
| Cibles apparentées | HDAC Caspase Proteasome MMP HCV Protease Cysteine Protease DPP Tyrosinase HIV Protease Serine Protease |
|---|---|
| Autre Secretase Inhibiteurs | DAPT LY411575 Nirogacestat (PF-03084014) Dibenzazepine (YO-01027) Avagacestat (BMS-708163) Semagacestat (LY450139) MK-0752 MDL-28170 L-685,458 NGP 555 |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| U87 | Cell Viability Assay | 30 μM | 4 d | decreases cell viability | 24495907 | |
| U87 R1 | Cell Viability Assay | 30 μM | 4 d | decreases cell viability | 24495907 | |
| MGG4 | Cell Viability Assay | 30 μM | 4 d | decreases cell viability | 24495907 | |
| MGG6 | Cell Viability Assay | 30 μM | 4 d | decreases cell viability | 24495907 | |
| MGG8 | Cell Viability Assay | 30 μM | 4 d | decreases cell viability | 24495907 | |
| MGG23 | Cell Viability Assay | 30 μM | 4 d | decreases cell viability | 24495907 | |
| SUM149 | Cell Viability Assay | 0-10 μM | 72 h | inhibits cell growth dose dependently | 22547109 | |
| Sum190 | Cell Viability Assay | 0-10 μM | 72 h | inhibits cell growth dose dependently | 22547109 | |
| WM35 | Function Assay | 10 uM | 24 h | DMSO | decreases the levels of NOTCH downstream target HES1 | 21980408 |
| WM98.1 | Function Assay | 10 uM | 24 h | DMSO | decreases the levels of NOTCH downstream target HES1 | 21980408 |
| WM115 | Function Assay | 10 uM | 24 h | DMSO | decreases the levels of NOTCH downstream target HES1 | 21980408 |
| WM983A | Function Assay | 10 uM | 24 h | DMSO | decreases the levels of NOTCH downstream target HES1 | 21980408 |
| WM3248 | Function Assay | 10 uM | 24 h | DMSO | decreases the levels of NOTCH downstream target HES1 | 21980408 |
| WM35 | Growth Inhibition Assay | 10 uM | 0-18 d | DMSO | inhibits cell growth time dependently | 21980408 |
| WM98.1 | Growth Inhibition Assay | 10 uM | 0-18 d | DMSO | inhibits cell growth time dependently | 21980408 |
| WM115 | Growth Inhibition Assay | 10 uM | 0-18 d | DMSO | inhibits cell growth time dependently | 21980408 |
| WM983A | Growth Inhibition Assay | 10 uM | 0-18 d | DMSO | inhibits cell growth time dependently | 21980408 |
| WM3248 | Growth Inhibition Assay | 10 uM | 0-18 d | DMSO | inhibits cell growth time dependently | 21980408 |
| A673 | qHTS assay | 29435139 | ||||
| DAOY | qHTS assay | 29435139 | ||||
| BT-37 | qHTS assay | 29435139 | ||||
| BT-12 | qHTS assay | 29435139 | ||||
| OHS-50 | qHTS assay | 29435139 | ||||
| SJ-GBM2 | qHTS assay | 29435139 | ||||
| SK-N-MC | qHTS assay | 29435139 | ||||
| NB-EBc1 | qHTS assay | 29435139 | ||||
| LAN-5 | qHTS assay | 29435139 | ||||
| Cliquez pour voir plus de données expérimentales sur les lignées cellulaires | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 469.4 | Formule | C22H20F5N3O3 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 847925-91-1 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | RG-4733 | Smiles | CC(C)(C(=O)NCC(C(F)(F)F)(F)F)C(=O)NC1C2=CC=CC=C2C3=CC=CC=C3NC1=O | ||
Solubilité
|
In vitro |
DMSO
: 94 mg/mL
(200.25 mM)
Ethanol : 50 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
γ secretase
(Cell-free assay) 4 nM
Notch
(Cell-free assay) 5 nM
Aβ40
(Cell-free assay) 14 nM
|
|---|---|
| In vitro |
RO4929097 diminue la quantité de peptides Aβ sécrétés dans le milieu de culture des cellules HEK293 avec un EC50 de 14 nM. Ce composé inhibe fortement le traitement de Notch avec un EC50 de 5 nM dans le test rapporteur basé sur les cellules Notch. La puissance de cette substance chimique dans les tests sans cellules et cellulaires est dans la plage nanomolaire basse avec une sélectivité >100 fois observée par rapport à 75 autres protéines de divers types, y compris les récepteurs, les canaux ioniques et les enzymes (panel CEREP). Après 5 jours de traitement, il réduit la production d'ICN dans les cellules humaines de CPNPC A549, induisant un phénotype de cellule tumorale aplati et moins transformé en culture tissulaire. Il bloque le traitement de Notch dans les cellules humaines de carcinome pulmonaire non à petites cellules et diminue l'expression du gène cible transcriptionnel de Notch Hes1. Le traitement avec ce composé révèle une diminution de deux à trois fois de l'expression des gènes cibles directs de Notch, Hes1, Hey1 et Heyl dans SUM149 et une diminution de 3,5 à huit fois de l'expression dans les cellules SUM190. Il inhibe modestement la croissance des cellules SUM149 de manière dose-dépendante. À une concentration de 1 μM de cette substance chimique, l'inhibition de la croissance est de 20% pour SUM149 et de 10% pour les cellules SUM190, par rapport aux contrôles traités par véhicule. Il diminue la production de cytokines inflammatoires par les lymphocytes T. De plus, avec ce traitement, il y a un déplacement en faveur des cytokines TH2 par rapport aux TH1. En outre, la production d'IL-6 induite par l'activation des lymphocytes T serait augmentée avec ce composé. Suite à ce traitement, les lignées cellulaires de mélanome sélectionnées révèlent une régulation négative de l'effecteur en aval de NOTCH HES1. Une diminution de la quantité de mélanosphères formées suite à ce traitement dans les lignées cellulaires de mélanome primaires est détectée.
|
| Kinase Assay |
Tests de puissance in vitro
|
|
Après l'utilisation de RO4929097, les peptides Aβ sont mesurés par des tests ECL utilisant une variété d'anticorps anti-Aβ et un analyseur Origen 1.5. Le mAb murin 4G8 se lie à un épitope du peptide Aβ (entre les acides aminés 18 et 21) qui est immédiatement distal au site de clivage de l'α-secretase. Le mAb murin G2–10 se lie à l'extrémité C qui est exposée après le clivage médiatisé par la γ-secretase pour générer l'acide aminé 40 du peptide Aβ40. L'anticorps de lapin FCA3542 se lie à l'extrémité C qui est exposée après le clivage médiatisé par la γ-secretase pour générer l'acide aminé 42 du peptide Aβ42. Le mAb 4G8 est biotinylé avec de l'ester de biotine-LC-sulfo-N-hydroxysuccinimide. Les anticorps G2–10 et FCA3542 sont ruthénylés avec de l'ester de TAG-N-hydroxysuccinimide. Aβ(x-40) est détecté avec 4G8 biotinylé et G2–10 ruthénylé. Aβ(x-42) est détecté avec 4G8 biotinylé et FCA3542 ruthénylé.
|
|
| In vivo |
L'injection orale de 3 à 60 mg/kg de RO4929097 une ou deux fois par jour à des souris nues porteuses de xénogreffes de CPNPC A549 pendant 7, 14 ou 21 jours selon un programme de 21 jours entraîne une inhibition significative de la croissance tumorale par rapport aux animaux traités par véhicule. Les valeurs d'inhibition de la croissance tumorale varient de 66% à 91%. Lorsque les souris sont traitées avec 60 mg/kg de ce composé deux fois par jour selon le programme 7+/14-, le traitement provoque initialement une régression des tumeurs A549 établies. À la fin du cycle de 21 jours (jour 47), la prévention de la croissance tumorale est toujours de 91% par rapport aux souris témoins traitées par véhicule. L'inhibition de la croissance tumorale reste prolongée et soutenue jusqu'à 34 jours après le traitement (jour 67). Au jour 67, ces souris sont à nouveau traitées avec la même dose de cette substance chimique pour un deuxième cycle (7 jours) jusqu'au jour 74. Il est important de noter que les effets antitumoraux sont maintenus après la fin de la posologie. Ce composé entraîne une expression réduite des gènes associés à l'angiogenèse dans le modèle de xénogreffe A549. En revanche, le xénogreffe H460a résistant à RO4929097 présente peu de changement dans l'expression de ces gènes, soulignant le mécanisme d'action anti-angiogenèse in vivo de cet agent. Pour les tumeurs surexprimant IL6 et IL8, il n'a plus d'impact sur l'angiogenèse ou l'infiltration des fibroblastes associés à la tumeur.
|
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | Hey1 Snail / N-cadherin / Twist / E-cadherin Akt / p-Akt / Notch / IGF1R / FBXW7 NICD / Hes1 / Hes3 / Hes5 |
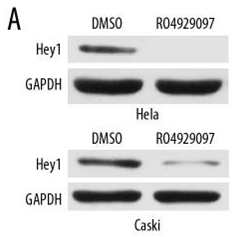
|
29899322 |
| Growth inhibition assay | Cell viability |
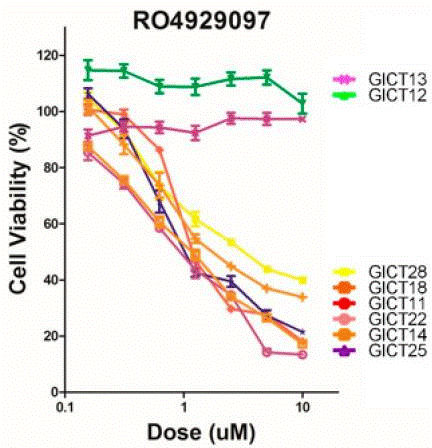
|
30669546 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
Questions fréquemment posées
Question 1:
How about its half-life?
Réponse :
Its half-life is about 20 hours based on the following paper: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3869895/
