réservé à la recherche
AM1241 Cannabinoid Receptor agoniste
N° Cat.S1544
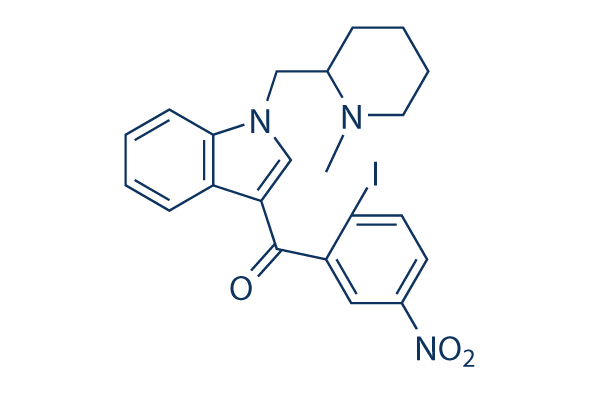
Structure chimique
Poids moléculaire: 503.33
Contrôle qualité
| Cibles apparentées | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Autre Cannabinoid Receptor Inhibiteurs | AM251 BML-190 Otenabant (CP-945598) HCl 6-Iodopravadoline (AM630) Org 27569 GW842166X CID16020046 WIN 55, 212-2 mesylate Yangonin (+)-Gallocatechin |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 503.33 | Formule | C22H22IN3O3 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 444912-48-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CN1CCCCC1CN2C=C(C3=CC=CC=C32)C(=O)C4=C(C=CC(=C4)[N+](=O)[O-])I | ||
Solubilité
|
In vitro |
DMSO
: 101 mg/mL
(200.66 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
CB2
3.4 nM(Ki)
CB1
280 nM(Ki)
|
|---|---|
| In vitro |
AM-1241 est un agoniste protéen du CB2 basé sur les différents effets observés dans divers essais (afflux de calcium, phosphorylation de la kinase régulée par le signal extracellulaire (ERK) et mesure du cAMP) et sur le passage de l'antagonisme neutre à l'agonisme dans l'essai cAMP lorsque la concentration de forskoline est abaissée. Dans les essais de liaison par compétition [3H]CP 55,940, ce composé présente une forte affinité pour le récepteur CB2 humain avec une valeur Ki d'environ 7 nM, tandis que son affinité pour le récepteur CB1 humain est plus de 80 fois plus faible, en utilisant des préparations membranaires de lignées cellulaires HEK et CHO stables exprimant respectivement les récepteurs CB2 et CB1 humains recombinants.
|
| Kinase Assay |
Tests de liaison
|
|
La liaison aux récepteurs cannabinoïdes est testée en utilisant la liaison par compétition-équilibre vs [3H]CP55,940. AM-1241 est dilué dans 25 mM Tris base (pH 7,4)/5 mM MgCl2/1 mM EDTA/0,1% BSA essentiellement sans acide gras et transféré dans des plaques à 96 puits traitées au Regisil. [3H]CP55,940 (DuPont_NEN ; activité spécifique 100–180 Ci/mmol ; 1 Ci =37 GBq) est ajouté à une concentration de 0,8 nM. Des membranes préparées à partir de cerveau de rat (contenant des récepteurs CB1) ou de rate de souris (contenant des récepteurs CB2) sont ajoutées (≈50 μg de protéines membranaires par puits), les plaques sont incubées à 30 °C pendant 1 heure, et le contenu est filtré sur des filtres Packard Unifilter GF/B à 96 puits à l'aide d'un moissonneur de cellules Packard Filtermate 196. Les filtres sont lavés avec 50 mM Tris base/5 mM MgCl2/0,5% BSA glacés et séchés. La radioactivité liée est quantifiée et corrigée pour la liaison non spécifique, et les résultats sont normalisés entre 0% et 100% de [3H]CP-55,940 spécifiquement lié. L'IC50 est déterminée par analyse de régression non linéaire à l'aide de GraphPad PRISM et transformée en valeur Ki. Toutes les données sont recueillies en double. Les valeurs IC50 et Ki sont déterminées à partir de trois expériences indépendantes.
|
|
| In vivo |
AM-1241 inverse de manière dose-dépendante l'hypersensibilité tactile et thermique produite par la ligature des nerfs spinaux L5 et L6 chez les rats. Ce composé est également actif pour bloquer l'hypersensibilité tactile et thermique induite par la ligature des nerfs spinaux chez les souris dépourvues de récepteurs CB1 (souris CB1-/ -), confirmant qu'il inverse l'hypersensibilité sensorielle indépendamment des actions sur les récepteurs CB1. Cette substance chimique (100, 330 μg/kg i.p.) supprime le développement de l'hyperalgésie et de l'allodynie thermiques et mécaniques évoquées par la carragénine. Et cette suppression est bloquée par l'antagoniste CB2 SR144528 mais pas par l'antagoniste CB1 SR141716A. Il produit une antinociception dose-dépendante à un stimulus thermique appliqué à la patte arrière, lorsqu'il est administré dans la patte arrière du côté du test (patte ipsilatérale), tandis qu'il est beaucoup moins actif dans le côté contralatéral. L'A50 (dose analgésique produisant un effet de 50%) de ce composé est de 847 μg/kg, l'effet maximal possible (100% MPE) étant atteint à 3,3 mg/kg. Il produit également une antinociception dose-dépendante lorsqu'il est administré par voie intrapéritonéale (i.p.), avec un A50 de 103 μg/kg. Les actions antinociceptives de cette substance chimique sont bloquées par l'antagoniste sélectif des récepteurs CB2 AM630, mais pas par l'antagoniste sélectif des récepteurs CB1 AM251. Ce composé ne produit pas les effets cannabinoïdes du SNC d'hypothermie, de catalepsie, d'inhibition de l'activité ou d'altération de la déambulation, tandis que cette tétrade d'effets est produite par l'agoniste mixte des récepteurs CB1/CB2 WIN55,212-2. Des injections quotidiennes de cette substance chimique par voie i.p., initiées au début des symptômes, augmentent l'intervalle de survie après l'apparition de la sclérose latérale amyotrophique (SLA) de 56% dans un modèle de souris transgénique de la SLA.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
