réservé à la recherche
Istradefylline Adenosine Receptor antagoniste
N° Cat.S2790
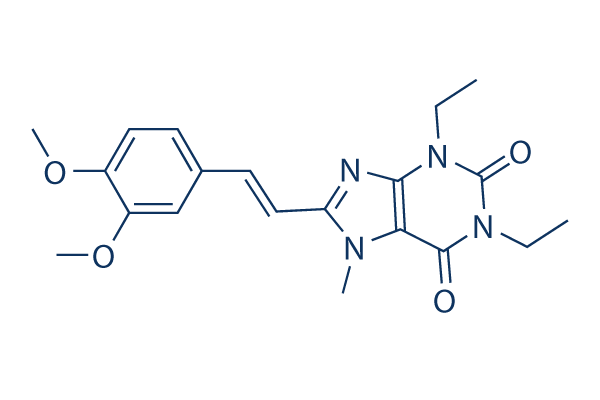
Structure chimique
Poids moléculaire: 384.43
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- SDS
- Fiche technique
| Cibles apparentées | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Autre Adenosine Receptor Inhibiteurs | Reversine CGS 21680 HCl ZM241385 SCH58261 Etrumadenant (AB928) A2AR antagonist 1 Ciforadenant (CPI-444) Imaradenant (AZD4635) DPCPX Proxyphylline |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 384.43 | Formule | C20H24N4O4 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 155270-99-8 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | KW-6002 | Smiles | CCN1C2=C(C(=O)N(C1=O)CC)N(C(=N2)C=CC3=CC(=C(C=C3)OC)OC)C | ||
Solubilité
|
In vitro |
DMSO
: 6 mg/mL
(15.6 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Adenosine A2A receptor
2.2 nM(Ki)
|
|---|---|
| In vitro |
L'affinité de l'Istradefylline pour l'A2AR est 70 fois supérieure à celle pour le récepteur A1 avec un Ki de 2,2 nM contre 150 nM. L'exposition d'astrocytes striataux primaires de rat à ce composé entraîne l'abolition dépendante de la concentration de l'induction de l'astrogliose par le bFGF in vitro. Les affinités de liaison (Ki) de cette substance chimique pour le récepteur A1, le récepteur A2A et le récepteur A3 chez l'homme sont respectivement >287 nM, 9,12 nM et >681 nM, pour le récepteur A1 et le récepteur A2A chez le rat respectivement 50,9 nM et 1,57 nM, et pour le récepteur A1 et le récepteur A2A chez la souris respectivement 105,02 nM et 1,87 nM. |
| In vivo |
L'Istradefylline inverse la catalepsie induite par le CGS21680 et la réserpine avec des ED50 de 0,05 mg/kg et 0,26 mg/kg, respectivement. Ce composé est plus de 10 fois plus puissant dans ces modèles par rapport à d'autres antagonistes de l'adénosine et aux médicaments agonistes de la dopamine. L'administration de cette substance chimique en association avec la LevoDOPA (50 mg/kg) exerce des effets proéminents sur la catalepsie induite par l'halopéridol et la réserpine. L'administration orale de ce composé à 10 mg/kg à des marmousets communs traités au MPTP produit une augmentation de l'activité locomotrice à environ le double de celle du contrôle et améliore l'incapacité motrice. L'administration de cette substance chimique (10 mg/kg, po, 90 minutes avant SKF80723/quinpirole/LevoDOPA) en association avec le SKF80723 (1 mg/kg, ip), le quinpirole (0,06 mg/kg ip) ou la LevoDOPA (2,5 mg/kg po) produit un effet additif significatif sur l'activité locomotrice et l'amélioration de l'incapacité motrice, mais pas la dyskinésie. Dans le modèle de souris MPTP, ce composé atténue significativement la déplétion de dopamine striatale dans diverses conditions. Le prétraitement avec cette substance chimique (3,3 mg/kg, i.p.) avant une dose unique de MPTP atténue les déplétions partielles de dopamine et de DOPAC mesurées dans les striata 1 semaine plus tard. L'administration orale de ce composé protège contre la perte de cellules neuronales dopaminergiques nigrales induite par la 6-hydroxydopamine chez les rats, et prévient la perte fonctionnelle des terminaisons nerveuses dopaminergiques dans le striatum et la gliose qui en résulte causée par le MPTP chez les souris. Le traitement chronique avec ce composé n'améliore pas les déficits de réversion chez les rats déplétés en dopamine. Les mouvements de la mâchoire tremblants induits par le pimozide sont significativement réduits par la co-administration de cette substance chimique ou de tropicamide. Les augmentations de l'expression de c-Fos striatal ventrolatéral induites par le pimozide sont réduites par une dose efficace sur le plan comportemental de ce composé, contrairement au tropicamide par lequel l'expression de c-Fos chez les rats traités au pimozide est en fait augmentée. |
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT05885360 | Active not recruiting | Parkinson Disease|Tremor |
Georgetown University|Kyowa Kirin Inc. |
January 20 2023 | Phase 4 |
| NCT02610231 | Completed | Idiopathic Parkinson''s Disease |
Kyowa Kirin Co. Ltd.|Kyowa Hakko Kirin Pharma Inc. |
December 2015 | Phase 3 |
| NCT02256033 | Completed | Hepatic Impairment |
Kyowa Kirin Co. Ltd.|Kyowa Hakko Kirin Pharma Inc. |
August 2014 | Phase 1 |
| NCT00455507 | Completed | Parkinson''s Disease |
Kyowa Kirin Co. Ltd. |
March 2007 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
