réservé à la recherche
Molidustat (BAY 85-3934) HIF modulateur
N° Cat.S8138
-chemical-structure-s8138.gif)
Structure chimique
Poids moléculaire: 314.30
Contrôle qualité
| Cibles apparentées | EGFR VEGFR JAK PDGFR FGFR Src FLT FLT3 HER2 Bcr-Abl |
|---|---|
| Autre HIF Inhibiteurs | PT2399 PX-478 Dihydrochloride BAY 87-2243 KC7F2 Lificiguat (YC-1) IOX2 CAY10585 (LW 6) PT2385 IDF-11774 MK-8617 |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 314.30 | Formule | C13H14N8O2 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 1154028-82-6 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | C1COCCN1C2=NC=NC(=C2)N3C(=O)C(=CN3)N4C=CN=N4 | ||
Solubilité
|
In vitro |
DMSO
: 10 mg/mL
(31.81 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
PHD2
(Cell-free assay) 280 nM
PHD3
(Cell-free assay) 450 nM
PHD1
(Cell-free assay) 480 nM
|
|---|---|
| In vitro |
In vitro, Molidustat (BAY 85-3934) induit la transcription des gènes sensibles à l'hypoxie dans les cellules HeLa, A549 et Hep3B. |
| Kinase Assay |
Essai de prolyl hydroxylase
|
|
Le HIF-1α 556–574 biotinylé (biotinyl-DLDLEMLAPYIPMDDDFQL) est lié à des plaques blanches 96 puits NeutrAvidin à haute capacité de liaison, qui sont pré-bloquées avec de la caséine bloquante et ensuite bloquées avec 1 mM de biotine. Le substrat peptidique immobilisé est incubé avec la quantité appropriée de HIF-PH dans un tampon contenant 20 mM Tris (pH 7.5), 5 mM KCl, 1.5 mM MgCl2, 20 µM 2-oxoglutarate, 10 µM FeSO4, 2 mM ascorbate, 4% d'inhibiteurs de protéase sans EDTA dans un volume final de 100 µl, avec ou sans Molidustat (BAY 85-3934) ajouté à des concentrations appropriées. Le temps de réaction est de 60 min. Pour arrêter la réaction, les plaques sont lavées trois fois avec un tampon de lavage. Le biotinyl-HIF-1α 556–574 hydroxylé est incubé avec Eu-VBC dans 100 µl de tampon de liaison (50 mM Tris [pH 7.5], 120 mM NaCl) pendant 60 min à température ambiante. Après six lavages avec le tampon de lavage DELFIA et l'ajout de 100 µl de solution d'amélioration, la quantité de VBC lié est déterminée en mesurant la fluorescence résolue dans le temps avec un lecteur de plaques Tecan infinite M200. Les mesures sont effectuées en triple ou plus, et les résultats sont exprimés en moyennes ± SEM. Les valeurs d'IC50 pour ce composé sont déterminées après ajustement de la courbe à l'aide du logiciel GraphPad Prism, en appliquant l'équation logistique à quatre paramètres aux ensembles de données.
|
|
| In vivo |
Chez les rats Wistar et les singes cynomolgus sains, le Molidustat (BAY 85-3934) (1.5 mg/kg, p.o.) induit une production d'EPO et une érythropoïèse dose-dépendante. Chez les rats atteints d'anémie rénale induite, ce composé (5 mg/kg, p.o.) est également efficace pour augmenter les niveaux d'hématocrite tout en stimulant la production endogène d'EPO sans effets hypertensifs. |
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | HIF-1α |
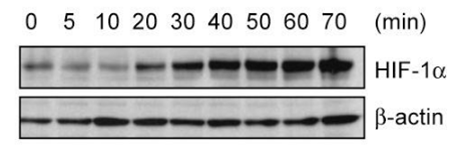
|
25392999 |
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT03418168 | Completed | Anemia|Renal Insufficiency Chronic |
Bayer |
February 22 2018 | Phase 3 |
| NCT03351166 | Completed | Anemia|Renal Insufficiency Chronic |
Bayer |
January 22 2018 | Phase 3 |
| NCT03350347 | Completed | Anemia|Renal Insufficiency Chronic |
Bayer |
December 13 2017 | Phase 3 |
| NCT02312973 | Completed | Renal Insufficiency Chronic |
Bayer |
January 14 2015 | Phase 1 |
| NCT01458028 | Completed | Anemia |
Bayer |
September 2011 | Phase 1 |
| NCT01332942 | Completed | Anemia |
Bayer |
April 2011 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
