nur für Forschungszwecke
Cyclophosphamide Monohydrate Alkylating Agent
Kat.-Nr.S2057
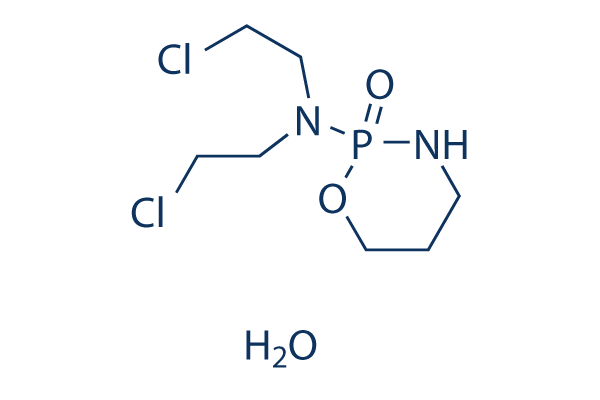
Chemische Struktur
Molekulargewicht: 279.1
Qualitätskontrolle
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HL60 cells | Cytotoxicity assay | Cytotoxicity against human HL60 cells by MTT assay, IC50=8.79 μM | 20850303 | |||
| BALB/c 3T3 cells | Cytotoxicity assay | In vitro cytotoxicity was evaluated in mouse embryo BALB/c 3T3 cells, IC50=37.6 μM | 9873412 | |||
| BALB/c 3T3 | Cytotoxicity assay | In vitro cytotoxicity against BALB/c 3T3 cells, IC50 = 37.6 μM. | 7877150 | |||
| T-cells | Immunosuppressive assay | 100 mg/kg | 8 days | Immunosuppressive activity against MAV-1 infected BALB/c mouse assessed as T cells suppression at 100 mg/kg, ip treated 8 days before infection for 4 weeks measured 14 days post infection by flow cytometry | 18268085 | |
| B-cells | Immunosuppressive assay | 100 mg/kg | 8 days | Immunosuppressive activity against MAV-1 infected BALB/c mouse assessed as B cells suppression at 100 mg/kg, ip treated 8 days before infection for 4 weeks measured 14 days post infection by flow cytometry | 18268085 | |
| U87 MG | Antitumor assay | 80 mg/kg | Antitumor activity in human U87 MG cells xenografted mouse at 80 mg/kg, iv administered in Q2D x 5 schedule | 18450456 | ||
| MX1 | Antitumor assay | 120 mg/kg | up to 3 weeks | Antitumor activity against human MX1 cells xenografted in nude mouse adjuvant model assessed as increase in mouse survival time at 120 mg/kg, po BID measured up to 3 weeks | 20726512 | |
| U87MG | Anticancer assay | 80 mg/kg | 6 days | Anticancer activity against human U87MG cells xenografted in athymic mouse assessed as tumor suppression at 80 mg/kg, iv Q2D for 6 days | 21106377 | |
| NCI-H522 | Antitumor assay | 50 mg/kg | 28 days | Antitumor activity against human NCI-H522 cells xenografted in Balb/c nude mouse assessed as tumor growth inhibition at 50 mg/kg, ig administered once daily for 28 days relative to control | 28092860 | |
| U2932 | Antitumor assay | 50 mg/kg | 5 consecutive days | Antitumor activity against human U2932 cells xenografted in SCID mouse assessed as reduction in tumor burden at 50 mg/kg, ip administered for 5 consecutive days measured up to day 40 post cell injection | 28605593 | |
| MDA-MB-231 | Cytotoxicity assay | 48 hr | Cytotoxicity against Homo sapiens (human) MDA-MB-231 cells after 48 hr by MTT assay, IC50 = 0.09 μM. | ChEMBL | ||
| K562 | Cytotoxicity assay | 48 hr | Cytotoxicity against Homo sapiens (human) K562 cells after 48 hr by MTT assay, IC50 = 0.15 μM. | ChEMBL | ||
| K562 | Antiproliferative assay | 48 hr | Antiproliferative activity against Homo sapiens (human) K562 cells after 48 hr by MTT assay, IC50 = 0.153 μM. | ChEMBL | ||
| MCF7 | Cytotoxicity assay | 48 hr | Cytotoxicity against Homo sapiens (human) MCF7 cells after 48 hr by SRB assay, IC50 = 10 mM. | 19372630 | ||
| HepG2 | Cytotoxicity assay | 48 hr | Cytotoxicity against Homo sapiens (human) HepG2 cells after 48 hr by MTT assay, IC50 = 0.24 μM. | ChEMBL | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 279.1 | Formel | C7H15Cl2N2O2P.H2O |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 6055-19-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | NSC-26271 Monohydrate | Smiles | C1CNP(=O)(OC1)N(CCCl)CCCl.O | ||
Löslichkeit
|
In vitro |
DMSO
: 55 mg/mL
(197.06 mM)
Water : 55 mg/mL Ethanol : 55 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Cyclophosphamide (CY) ist ein Chemotherapeutikum mit einem dosisabhängigen, bimodalen Effekt auf das Immunsystem. Die Cyclophosphamide-Behandlung verstärkt die Apoptose und verringert die homöostatische Proliferation von regulatorischen T-Zellen. Cyclophosphamide reguliert die Expression von GITR und FoxP3 herunter, die an der suppressiven Aktivität von T(REGs) beteiligt sind. Cyclophosphamide erhöht die CYP3A4-, CYP2C8- und CYP2C9-Proteinspiegel in primären menschlichen Hepatozytenkulturen, wodurch deren eigene Raten der 4-Hydroxylierung in den kultivierten Hepatozyten erhöht werden. Cyclophosphamide hat in Anwesenheit metabolischer Aktivierung Mutationen in Basenpaar-substituierenden Stämmen von Salmonella tryphimurium hervorgerufen, zeigte sich jedoch im E. coli Chromotest als negativ. Cyclophosphamide hat sich als fähig erwiesen, Genmutationen, Chromosomenaberrationen, Mikronuklei und Schwesterchromatidenaustausch in einer Vielzahl von kultivierten Zellen in Anwesenheit metabolischer Aktivierung sowie Schwesterchromatidenaustausch ohne metabolische Aktivierung zu erzeugen. |
|---|---|
| In vivo |
Cyclophosphamide hat auch Chromosomenschäden und Mikronuklei bei Ratten, Mäusen und chinesischen Hamstern sowie Genmutationen im Maus-Spot-Test und im transgenen lacZ-Konstrukt von Muta Mouse hervorgerufen. Cyclophosphamide, in einer definierten Reihenfolge mit einem GM-CSF-sezernierenden, neu-exprimierenden Ganzzellimpfstoff verabreicht, verstärkt das Potenzial des Impfstoffs, das Tumorwachstum bei neu-transgenen Mäusen zu verzögern. Cyclophosphamide vermittelt seine Wirkungen, indem es die Wirksamkeit des Impfstoffs verstärkt und nicht über einen direkten zytolytischen Effekt auf Krebszellen. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | PTEN / pAkt / Caspase 3 / GAPDH Caspase 3 / Cleaved-Caspase 3 / Cleaved-PARP / Tubulin Nuclear AIF / Cytosolic AIF / TBP / GAPDH LC3B I / LC3B II / GAPDH |
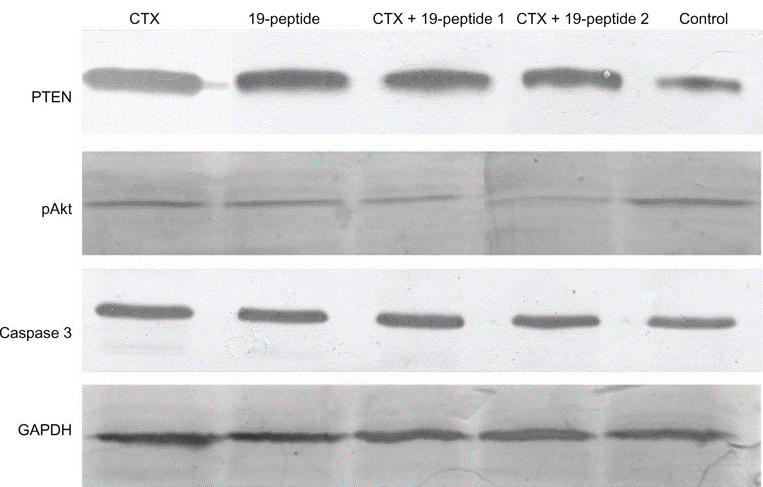
|
23874108 |
| Growth inhibition assay | Cell Viability Tumor Volume Tumor Volume |
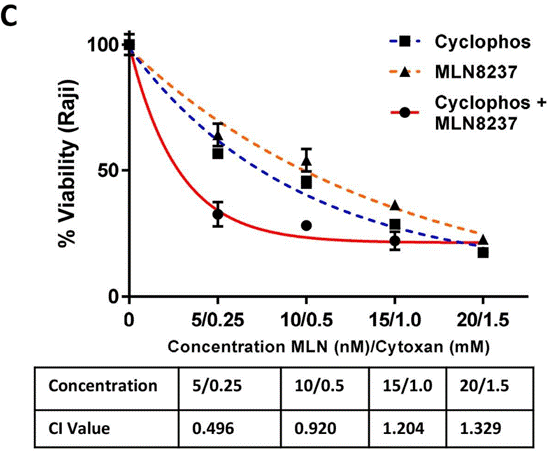
|
31429028 |
| IHC | tumor cell invasion TUNEL / Caspase 3 PTEN / pAkt / PCNA ovary of mice Caspase-3 |
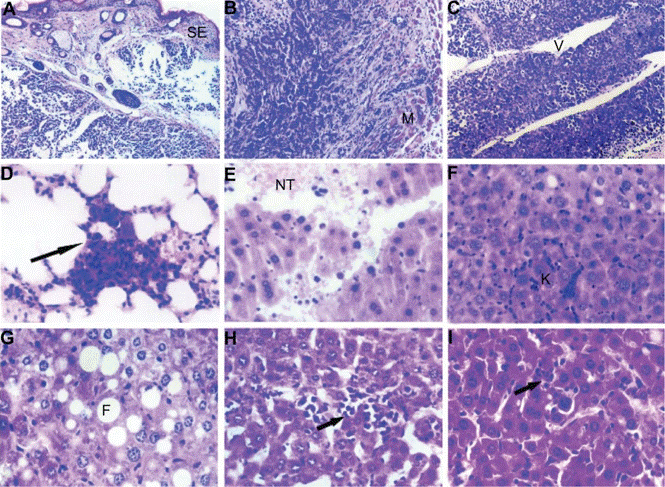
|
23874108 |
| Immunofluorescence | pAKT / pERK Ki-67 / UPK3 / KRT5 / pERK Ki-67 / KRT14 / KRT5 autophagy levels |
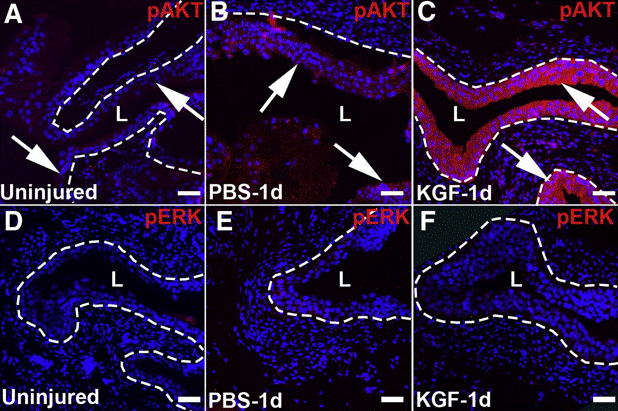
|
31654636 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06186700 | Active not recruiting | Breast Cancer Female |
Mansoura University |
December 25 2023 | Phase 2 |
| NCT06085742 | Recruiting | Breast Cancer |
University of Illinois at Chicago |
November 22 2023 | Phase 2 |
| NCT05800041 | Not yet recruiting | Gout Tophus |
RenJi Hospital|Westlake Therapeutics |
April 10 2023 | Early Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
Häufig gestellte Fragen
Frage 1:
Why does it show no activity in vitro assays?
Antwort:
The activity of this compound in vitro is controversial and has not been fully determined. It is a prodrug and may need Cytochrome P450 to convert it to the active form: 4-hydroxy cyclophosphamide. It is widely used in vivo, if you are going to use it in vitro, you may need to supplement Cytochrome P450 exogenously.
