nur für Forschungszwecke
Zanamivir Neuraminidase Inhibitor
Kat.-Nr.S3007
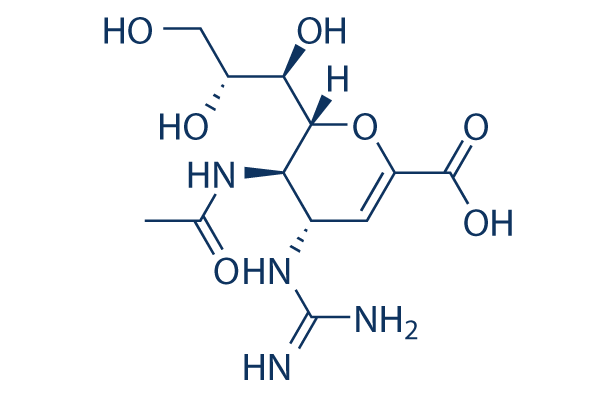
Chemische Struktur
Molekulargewicht: 332.31
Qualitätskontrolle
| Verwandte Ziele | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite Reverse Transcriptase HIV |
|---|---|
| Weitere Neuraminidase Inhibitoren | Laninamivir Octanoate Laninamivir |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 332.31 | Formel | C12H20N4O7 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 139110-80-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | GG167,GR 121167X | Smiles | CC(=O)NC1C(C=C(OC1C(C(CO)O)O)C(=O)O)N=C(N)N | ||
Löslichkeit
|
In vitro |
Water : 25 mg/mL
DMSO
: 2 mg/mL
(6.01 mM)
Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
neuraminidase
|
|---|---|
| In vitro |
Zanamivir, ein neuartiger Neuraminidase-Hemmer, ist wirksam bei der Verringerung der Virusreplikation in vitro. Diese Verbindung führt zu einer reduzierten Sensitivität bei Influenza A/H1N1-Varianten His274Asn sowie His274Gly, His274Ser und His274Gln. Es blockiert Influenza Neuraminidase und verhindert die Spaltung von Sialinsäureresten, wodurch die Ausbreitung der Nachkommenviren in den Schleimsekreten gestört und die virale Infektiosität reduziert wird. Dieses Mittel verhindert die Hämadsorption und Fusion von persistent infizierten Zellen mit nicht infizierten Zellen. Es reduziert die Anzahl (aber nicht die Fläche) der Plaques, wenn es nur während der Adsorptionsperiode vorhanden ist, und reduziert die Plaque-Fläche (aber nicht die Anzahl), wenn es erst nach der 90-minütigen Adsorptionsperiode in Plaque-Assays hinzugefügt wird. Die Verbindung reduziert auch die Fläche von Plaques, die von einer Neuraminidase-defizienten Variante gebildet werden, was bestätigt, dass ihre Interferenz mit der Zell-Zell-Fusion unabhängig von der Hemmung der Neuraminidase-Aktivität ist. Es hat keine Wirkung auf die Hämadsorption, hemmt aber die HA2b-Erythrozytenfusion, beurteilt sowohl durch Lipidmischung als auch durch Inhaltsmischung. |
| In vivo |
Zanamivir reduziert die Lungentiter des Virus und verringert Morbidität und Mortalität in einem Modell der tödlichen Infektion bei Mäusen. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT04597437 | Recruiting | Dengue Fever |
George Washington University|Naval Medical Research Center|Clinica de la Costa|Global Disease Research |
March 15 2024 | Early Phase 1 |
| NCT04494412 | Recruiting | Influenza Human|Arthralgia |
GlaxoSmithKline |
November 21 2022 | Phase 2 |
| NCT02377401 | Completed | Influenza Human |
GlaxoSmithKline |
April 28 2015 | Phase 1 |
| NCT01527110 | Completed | Influenza Human |
GlaxoSmithKline |
January 1 2012 | Phase 3 |
| NCT01353768 | Completed | Infections Respiratory Tract |
GlaxoSmithKline |
July 2011 | -- |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
