nur für Forschungszwecke
Amitriptyline HCl Serotonin Transporter Inhibitor
Kat.-Nr.S3183
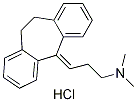
Chemische Struktur
Molekulargewicht: 313.86
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) |
|---|---|
| Weitere Serotonin Transporter Inhibitoren | Dapoxetine |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 313.86 | Formel | C20H23N.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 549-18-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CN(C)CCC=C1C2=CC=CC=C2CCC3=CC=CC=C31.Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 63 mg/mL
(200.72 mM)
Ethanol : 63 mg/mL Water : 15 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Histamine Receptor H1
0.5 nM(Ki)
SERT
3.45 nM(Ki)
Histamine receptor H4
7.31 nM(Ki)
NET
13.3 nM(Ki)
5-HT2
235 nM(Ki)
Sigma 1 receptor
287 nM(Ki)
|
|---|---|
| In vitro |
Amitriptyline hemmt die Forskolin-stimulierte Akkumulation von cyclischem AMP mit EC50-Werten von 16,2 μM in intakten CHO/DOR-Zellen. Diese Verbindung bewirkt eine konzentrationsabhängige Stimulation der ERK1/2- und GSK-3β-Phosphorylierung mit EC50-Werten von 9,0 μM in CHO/DOR-Zellen. Es (15 μM) bewirkt eine Stimulation der ERK1/2-Phosphorylierung in C6-Zellen. Diese Chemikalie (30 μM) hemmt die Forskolin-stimulierte Adenylylcyclase-Aktivität und antagonisiert die (−)-U50,488-hemmende Wirkung im Nucleus accumbens von Ratten. Es bindet an die extrazelluläre Domäne von sowohl TrkA als auch TrkB und fördert die TrkA-TrkB-Rezeptor-Heterodimerisierung. Diese Verbindung (< 500 nM) fördert die TrkA-Autophosphorylierung in primären Neuronen und induziert das Neuritenwachstum in PC12-Zellen. Es schützt T17-Zellen selektiv vor Apoptose mit einem EC50 von 50 nM. |
| In vivo |
Amitriptyline (15 mg/kg, i.p.) aktiviert TrkA- und TrkB-Rezeptoren und reduziert signifikant den durch Kaininsäure ausgelösten neuronalen Zelltod bei Mäusen. Diese Verbindung (15 mg/kg und 30 mg/kg, i.p.) verringert dosisabhängig die Immobilitätszeit im erzwungenen Schwimmtest (FST) von Mäusen. Diese Chemikalie (15 mg/kg, i.p.) zeigt einen signifikanten 24-Stunden-Rhythmus in der Immobilitätszeit im erzwungenen Schwimmtest (FST) von Mäusen. Es (1 mg/kg und 3 mg/kg) erhöht signifikant die insgesamt zurückgelegte Strecke von Mäusen in neuen Käfigen. Diese Verbindung (10 mg/kg p.o., zweimal täglich) dämpft die hypotherme Reaktion auf 8-OHDPAT und mCPP bei Mäusen erheblich. Es (10 mg/kg p.o., zweimal täglich) reduziert signifikant die Serotonin Transporter-Dichte um etwa 20% in der Kortikalregion von Mäusen. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06312813 | Recruiting | Rosacea |
Wright State University |
February 27 2024 | Phase 2 |
| NCT02519400 | Unknown status | Depression |
Asan Medical Center |
August 2015 | Phase 1 |
| NCT02101892 | Completed | Migraine|Preventive Treatment |
Rambam Health Care Campus|Migraine Research Foundation |
April 2014 | Not Applicable |
| NCT00516503 | Completed | Chronic Myeloproliferative Disorders|Leukemia|Lymphoma|Lymphoproliferative Disorder|Multiple Myeloma and Plasma Cell Neoplasm|Myelodysplastic Syndromes|Myelodysplastic/Myeloproliferative Neoplasms|Neurotoxicity|Pain|Unspecified Adult Solid Tumor Protocol Specific |
Alliance for Clinical Trials in Oncology|National Cancer Institute (NCI) |
February 2008 | Phase 3 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
