nur für Forschungszwecke
Subasumstat (TAK-981) SUMOylierungshemmer
Kat.-Nr.S8829
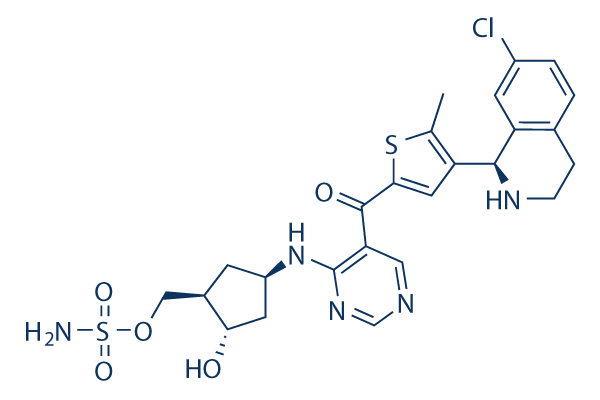
Chemische Struktur
Molekulargewicht: 578.10
Qualitätskontrolle
| Verwandte Ziele | Proteasome E1 Activating E3 Ligase DUB p97 E2 conjugating |
|---|---|
| Weitere SUMO Inhibitoren | 2-D08 Ginkgolic Acid momordin-Ic Ginkgolic Acid (C13:0) |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 578.10 | Formel | C25H28ClN5O5S2 |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS-Nr. | 1858276-04-6 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=C(C=C(S1)C(=O)C2=CN=CN=C2NC3CC(C(C3)O)COS(=O)(=O)N)C4C5=C(CCN4)C=CC(=C5)Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(172.98 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
SUMOylation enzymatic cascade
|
|---|---|
| In vitro |
Die Ex-vivo-Behandlung mit Subasumstat (TAK-981) induzierte Aktivierungs- und Reifungsmarker – einschließlich CD40, CD80 und CD86 – sowie eine erhöhte Sekretion entzündlicher Zytokine wie IP-10, MCP1, MIP-1α, MIP1β, IFNα und IFNβ, sowohl in dendritischen Zellen (DCs), die aus dem Knochenmark der Maus als auch aus peripheren mononukleären Blutzellen des Menschen stammen. |
| In vivo |
In vivo induzierte eine einzelne subkutane Injektion von Subasumstat (TAK-981) bei naiven Balb/c-Mäusen in den brachiale Lymphknoten die Aktivierung von DCs, gemessen als signifikante Zunahme der CD40- und CD86-Expression. Diese Verbindung zeigt Antitumoraktivität, einschließlich vollständiger Regression (CR) einiger Tumoren, bei immunkompetenten BALB/c-Mäusen mit syngenen A20-Lymphom-Tumoren. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT04381650 | Active not recruiting | Advanced or Metastatic Solid Tumors |
Takeda|Takeda Development Center Americas Inc. |
August 17 2020 | Phase 1|Phase 2 |
| NCT04074330 | Terminated | Lymphoma Non-Hodgkin |
Takeda |
October 15 2019 | Phase 1|Phase 2 |
| NCT03648372 | Terminated | Neoplasms|Lymphoma|Hematologic Neoplasms |
Takeda |
October 1 2018 | Phase 1|Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
