nur für Forschungszwecke
Indomethacin COX Inhibitor
Kat.-Nr.S1723
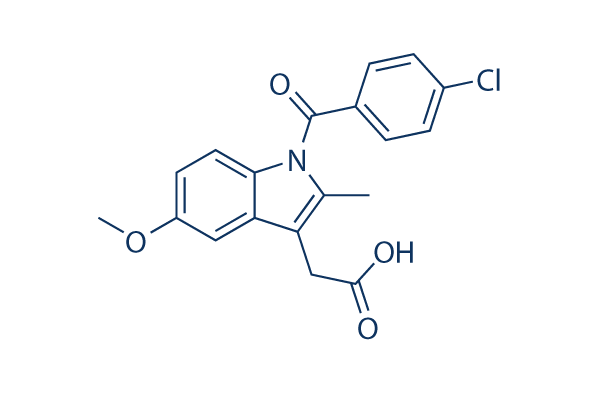
Chemische Struktur
Molekulargewicht: 357.79
Qualitätskontrolle
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HeLa cells | Function assay | 20 mins | Agonist activity at androgen receptor (unknown origin) expressed in HeLa cells co-expressing PSA-(ARE)4-Luc13 assessed as induction of DHT-induced luciferase activity after 20 mins by luciferase reporter gene assay, EC50=0.14 nM | |||
| J774 cells | Function assay | In vitro inhibitory activity against Prostaglandin G/H synthase 1 in murine J774 cells, IC50=2 nM | ||||
| U-937 cells | Function assay | In vitro inhibitory activity against human Prostaglandin G/H synthase 1 (COX-1) in U-937 cells, IC50=2 nM | ||||
| rat synovial cells | Function assay | In vitro inhibitory effect on production of prostaglandin E2 (PGE2) in rat synovial cells, IC50=2.9 nM | ||||
| 143982 cells | Function assay | In vitro inhibitory activity against human Prostaglandin G/H synthase 2 (COX-2) in 143982 cells, IC50=9 nM | ||||
| CHO cells | Function assay | In vitro inhibitory potency against human COX-1 in stably transfected chinese hamster ovary (CHO) cells, IC50=18 nM | ||||
| RBL-1 cell line | Function assay | Inhibition of Prostaglandin G/H synthase in intact RBL-1 cell line, IC50=0.5 μM | ||||
| SF-9 insect cells | Function assay | 20 Mins | Inhibition of human COX2 expressed in SF-9 insect cells assessed as conversion of [14C]-arachidonic acid to [14C]-prostaglandins preincubated for 20 mins by thin-layer chromatography analysis, IC50=0.75 μM | |||
| mouse RAW264.7 cells | Function assay | 24 h | Antiinflammatory activity in mouse RAW264.7 cells assessed as inhibition of LPS-induced NO production after 24 hrs by Griess assay, IC50=1.25 μM | |||
| mouse BV2 cells | Function assay | 24 h | Antiinflammatory activity in mouse BV2 cells assessed as inhibition of LPS-induced NO production after 24 hrs by Griess assay, IC50=7.1 μM | |||
| human 2008 cells | Function assay | Inhibition of human MRP1 in human 2008 cells, IC50=12 μM | ||||
| A549 cells | Function assay | 10 μM | Inhibition of mPGES1 in human A549 cells assessed as inhibition of IL-1-beta-induced PGE2 formation at 10 uM by cell-intact assay | |||
| HepG2 cells | Function assay | 100 μM | Inhibition of MRP1-mediated doxorubicin efflux in doxorubicin resistant human HepG2 cells at 100 uM by flow cytometry | |||
| THP1 cells | Function assay | 100 μM | 30 mins | Irreversible inhibition of COX-1 in human THP1 cells assessed as inhibition of arachidonic acid-induced TXB2 formation at 100 uM incubated for 30 mins followed by compound washout measured 30 mins post arachidonic acid challenge by radioimmunoassay | ||
| MDA-MB-231 cells | Function assay | 100 μM | 30 mins | Irreversible inhibition of COX-1 in human MDA-MB-231 cells assessed as inhibition of arachidonic acid-induced PGE2 formation at 100 uM incubated for 30 mins followed by compound washout measured 30 mins post arachidonic acid challenge by radioimmunoassay | ||
| LNCAP cells | Function assay | 30 μM | 48 h | Inhibition of AKR1C3 (unknown origin)-mediated testosterone-17beta-glucuronide formation expressed in human LNCAP cells at 30 uM after 48 hrs in presence of 4-androstene-3,17-dione | ||
| mouse BV2 cells | Cytotoxicity assay | 24 h | Cytotoxicity against mouse BV2 cells assessed as maximum non-toxic concentration after 24 hrs by MTT assay | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 357.79 | Formel | C19H16ClNO4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 53-86-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Indometacin,NSC-77541 | Smiles | CC1=C(C2=C(N1C(=O)C3=CC=C(C=C3)Cl)C=CC(=C2)OC)CC(=O)O | ||
Löslichkeit
|
In vitro |
DMSO
: 72 mg/mL
(201.23 mM)
Ethanol : 24 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
COX1
0.28 μM
COX-2
14 μM
|
|---|---|
| In vitro |
Indomethacin hemmt die Transkription eines Beta-Catenin/TCF-responsiven Reportergens dosisabhängig. Diese Verbindung reguliert auch das Beta-Catenin/TCF-transkriptionelle Zielgen Cyclin D1 herunter. Es schwächt die Transkription von Beta-Catenin/TCF-responsiven Genen ab, indem es die TCF-Aktivität moduliert, ohne die Beta-Catenin/TCF-Komplexbildung zu stören.
|
| In vivo |
Indomethacin erhöht die BrdU+-Zellen aller Linien und reduziert die Mikroglia-/Monozytenaktivierung bei Ratten nach fokaler zerebraler Ischämie. Diese Verbindung (7,5 mg/kg, eine Injektion) führt zu einer akuten Verletzung und Entzündung im distalen Jejunum und proximalen Ileum, die nach drei Tagen maximal ist und innerhalb einer Woche vollständig abklingt. Sie (zwei tägliche subkutane Injektionen) führt zu einer ausgedehnteren und chronischen Entzündung, die bei mehr als 75 % der Ratten mindestens zwei Wochen lang in aktiver Form anhält. Diese Chemikalie (4 ppm) reduziert die Tumorausbeute bei haarlosen SKH:HR-1-hrBr-Mäusen um 78 %. Sie (20 mg/kg, oral) erhöht die Gesamtfläche der Magenerosionen und die Konzentration von Lipidperoxiden in der Magenschleimhaut von Ratten. Diese Verbindung erhöht das Alpha-Tocopherol:Gesamtcholesterin-Verhältnis im Serum. Sie hemmt die Zunahme der Magenschleimhauterosionen und Lipidperoxide in der Magenschleimhaut sowie die Reduzierung von Alpha-Tocopherol im Serum.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06031363 | Completed | Pancreatitis|Cholangiopancreatography Endoscopic Retrograde|Indomethacin |
The First Affiliated Hospital of Soochow University |
November 1 2022 | Not Applicable |
| NCT04821323 | Completed | Healthy |
Janssen Research & Development LLC |
March 10 2021 | Early Phase 1 |
| NCT04025177 | Withdrawn | Patent Ductus Arteriosus After Premature Birth |
University of Manitoba|St. Boniface Hospital|Health Sciences Centre Winnipeg Manitoba|University at Buffalo |
January 2020 | Phase 2 |
| NCT03967483 | Unknown status | Headache Migraine |
Anne Ducros|French Society for the Study of Migraine Headache |
June 1 2019 | -- |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
