nur für Forschungszwecke
Ribavirin (ICN-1229) Antiviral chemisch
Kat.-Nr.S2504
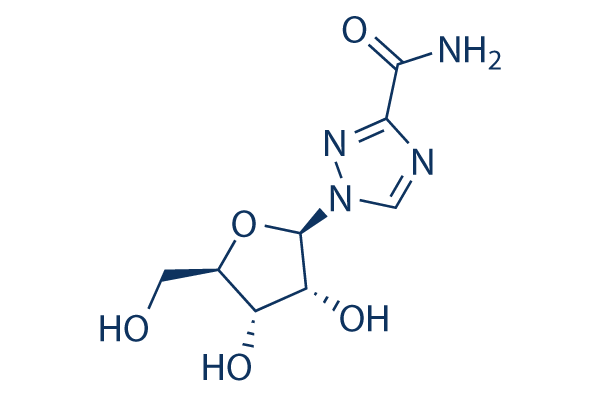
Chemische Struktur
Molekulargewicht: 244.20864
Qualitätskontrolle
| Verwandte Ziele | Integrase Bacterial Antibiotics Anti-infection Fungal COVID-19 Parasite Reverse Transcriptase HIV HCV Protease |
|---|---|
| Weitere Antiviral Inhibitoren | Moroxydine HCl Aloperine GS-441524 Oleanolic Acid Harringtonine NGI-1 U18666A Aloin B Saikosaponin B2 Lapachol |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| E6SM cell lines | Function assay | Effective concentration required to inhibit Herpes simplex virus-1(HSV-1) / thymine kinase deficient (TK-)B2006 / VMW1837 induced cytopathicity by 50% in E6SM cell lines, EC50=0.005 μM | ||||
| MDCK cells | Function assay | 3 days | Antiviral activity against Influenza B virus (B/HK/5/72) infected in MDCK cells assessed as virus-induced cytopathic effect after 3 days by microscopic analysis, EC50=0.094 μM | |||
| mouse L1210 cells | Function assay | 20-60 mins | Inhibition of IMPDH in mouse L1210 cells assessed as formation of [2,8-3H]hypoxanthine from [2,8-3H]IMP after 20 to 60 mins, IC50=1 μM | |||
| human CEM cells | Function assay | 20-60 mins | Inhibition of IMPDH in human CEM cells assessed as formation of [2,8-3H]hypoxanthine from [2,8-3H]IMP after 20 to 60 mins, IC50=1 μM | |||
| BHK21 cell line | Function assay | Inhibition of West Nile virus VLP replicon in BHK21 cell line, EC50=1.1 μM | ||||
| HeLa cell | Function assay | Effective concentration required to inhibit respiratory synaptial(RSV) virus-induced cytopathicity by 50% in HeLa cell lines, EC50=1.5 μM | ||||
| MDCK cells | Function assay | 36 h | Antiinfluenza activity against influenza A virus H1N1 infected in MDCK cells assessed as inhibition of virus-induced cytopathic effect after 36 hrs, IC50=1.9 μM | |||
| MDBK cells | Function assay | 2 days | Antiviral activity against Bovine viral diarrhea virus 1-NADL ATCC VR534 infected in MDBK cells assessed as reduction of viral cytopathic effect after 2 days bt MTS assay, EC50=4.6 μM | |||
| african green monkey Vero cells | Function assay | 5 days | Antiviral activity against RSV A2 infected in african green monkey Vero cells after 5 days by plaque reduction assay, EC50=7 μM | |||
| HEL cells | Function assay | 2-3 days | Antiviral activity against Herpes simplex virus 1 KOS infected in HEL cells assessed as protection from virus-induced cytopathogenicity after 2 to 3 days by MTT assay, EC50=10 μM | |||
| HEK293 cells | Function assay | 24 h | Inhibition of influenza A virus RNA-dependent RNA polymerase expressed in HEK293 cells after 24 hrs by dual luciferase reporter gene assay, EC50=15 μM | |||
| human BE(2)-C cells | Function assay | 18-20 h | Antiviral activity against Western equine encephalomyelitis virus infected in human BE(2)-C cells assessed as inhibition of viral RNA replication after 18 to 20 hrs by luciferase reporter gene assay, IC50=16 μM | |||
| human HuH7-J20 cells | Function assay | Antiviral activity against HCV JFH1 infected in human HuH7-J20 cells assessed as inhibition of viral life cycle by measuring secreted alkaline phosphatase level preincubated with cells for 1 hr followed by viral inoculation for 3 hrs measured at 72 hrs, EC50=30.4 μM | ||||
| human MT4 cells | Cytotoxic assay | 96 h | Cytotoxicity against human MT4 cells after 96 hrs by MTT assay, CC50=31 μM | |||
| human HuH7 cells | Cytotoxic assay | 3 days | Cytotoxicity against human HuH7 cells infected with HCV1b after 3 days by MTS assay, CC50=32 μM | |||
| human KB cells | Function assay | 72 h | Antiviral activity against Rhinovirus type 13 infected in human KB cells assessed as inhibition of virus-induced cytopathic effect after 72 hrs relative to control | |||
| human KB cells | Function assay | 1-1000 μg/ml | 72 h | Antiviral activity against Rhinovirus type 13 infected in human KB cells assessed as inhibition of virus-induced cytopathic effect at 1 to 1000 ug/ml after 72 hrs | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 244.20864 | Formel | C8H12N4O5 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 36791-04-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | NSC-163039, RTCA, Tribavirin | Smiles | C1=NC(=NN1C2C(C(C(O2)CO)O)O)C(=O)N | ||
Löslichkeit
|
In vitro |
DMSO
: 49 mg/mL
(200.64 mM)
Water : 49 mg/mL Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Ribavirin (ICN-1229) reduziert die Effizienz, mit der Nachkommen-Subgenom-Replikons neue Zellen im Replikon-System transfizieren, erheblich, obwohl es wenig Einfluss auf die HCV-Replikationsraten hat. Diese Verbindung erhöht die Mutationshäufigkeit von HCV, wobei die höchsten Mutationsraten in der NS5A-kodierenden Region gefunden werden. Es fördert TH1 und hemmt gleichzeitig die T2-Zytokinproduktion durch stimulierte T-Zellen. Ribavirin zeigt antivirale Aktivität gegen eine Vielzahl von RNA-Viren und wird in Kombination mit Interferon-alpha zur Behandlung von Hepatitis-C-Virusinfektionen eingesetzt. Es reduziert die Produktion von infektiösem Poliovirus in Zellkulturen auf bis zu 0,00001 %. Seine antivirale Aktivität wird direkt durch letale Mutagenese des viralen genetischen Materials ausgeübt. Diese Verbindung reduziert die viral induzierten Parameter der Makrophagenaktivierung bei physiologischen Konzentrationen (bis zu 500 mg/mL) erheblich. Es hemmt die Produktion von IL-4 durch Th2-Zellen, während es die Produktion von IFN-gamma in Th1-Zellen nicht verringert. Ribavirin zeigt in vitro antivirale Aktivität gegen eine breite Palette von DNA- und RNA-Viren. Es ist ein zytostatisches Mittel und verursacht eine Reduzierung der Synthese von DNA, RNA und Proteinen in exponierten Zellen. Es wird angenommen, dass es einen Wechsel im T-Helfer-Zellphänotyp von Typ 2 zu Typ 1 induziert.
|
Literatur |
|
|---|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | p53 / p-p53 / p21 / Mdm2 EZH2 / p-ERK / ERK / p-eIF4E / eIF4E / p21 Cyclin D1 p-AKT / AKT / pBP1 / BP1 |

|
22962590 |
| Growth inhibition assay | Cell number |
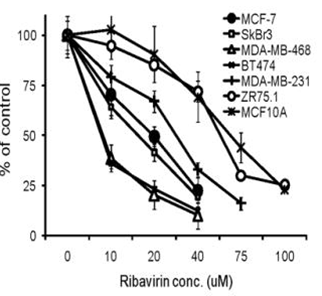
|
21415224 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05940545 | Recruiting | CCHF |
Liverpool School of Tropical Medicine |
July 12 2023 | Phase 1|Phase 2 |
| NCT04283513 | Not yet recruiting | Hemorrhagic Fever |
U.S. Army Medical Research and Development Command |
October 31 2022 | Phase 2 |
| NCT04335123 | Completed | COVID-19 |
University of Kansas Medical Center |
April 4 2020 | Phase 1 |
| NCT04285034 | Completed | Lassa Fever |
University of Oxford |
November 26 2019 | -- |
| NCT03889106 | Terminated | Lassa Fever |
University of Oxford|National Institute for Health Research United Kingdom|Kenema Government Hospital|London School of Hygiene and Tropical Medicine|Public Health England |
March 1 2019 | -- |
| NCT03585725 | Terminated | Follicular Lymphoma|Mantle Cell Lymphoma |
Weill Medical College of Cornell University|Memorial Sloan Kettering Cancer Center |
September 26 2018 | Early Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
