nur für Forschungszwecke
Bacitracin Selection Antibiotics for Transfected Cell Inhibitor
Kat.-Nr.S4146
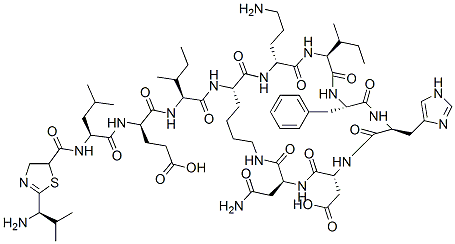
Chemische Struktur
Molekulargewicht: 1408.67
Qualitätskontrolle
- Antibiotic Titer > 65 IU/mg
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- Datenblatt
- SDS
| Verwandte Ziele | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite Reverse Transcriptase HIV |
|---|---|
| Weitere Selection Antibiotics for Transfected Cell Inhibitoren | Blasticidin S Hydrochloride Ribostamycin Sulfate D-Cycloserine |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 1408.67 | Formel | C65H101N17O16S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1405-87-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CCC(C)C1C(=O)NC(C(=O)NC(C(=O)NC(C(=O)NC(C(=O)NCCCCC(C(=O)NC(C(=O)N1)CCCN)NC(=O)C(C(C)CC)NC(=O)C(CCC(=O)O)NC(=O)C(CC(C)C)NC(=O)C2CSC(=N2)C(C(C)CC)N)CC(=O)N)CC(=O)O)CC3=CN=CN3)CC4=CC=CC=C4 | ||
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Bacitracin ist ein potentes Antibiotikum gegen grampositive Kokken, Staphylokokken, Streptokokken, Corynebakterien, Treponema pallidum, T. vincenti, Actinomyces israeli, anaerobe Kokken, Clostridien, Neisserien, die meisten Gonokokken und Meningokokken, ist aber relativ unwirksam gegen die meisten anderen gramnegativen Bakterien. Archaebacteria ist auch empfindlich gegenüber dieser Verbindung. Von dieser Gruppe zeigten Methanobacterium arbophilicum, M. M.O.H., M. O.H.G. und M. formicium eine Hemmung durch dieses Antibiotikum, während Methanospirilum und Methanosarcina unempfindlich sind. Diese Verbindung beeinflusst eine Reihe biochemischer Prozesse in Bakterien, einschließlich Metallionentransport, Peptidoglykansynthese, Membranpermeabilität und Biosynthese induzierbarer Enzyme. Viele der biologischen Eigenschaften dieser Chemikalie können ihrer hohen Affinität zu Polyisoprenylpyrophosphaten zugeschrieben werden. Abgesehen von der antibiotischen Aktivität der Bacitracine haben sich diese Peptide als nützliches Werkzeug zur Untersuchung von Lipid-Protein-Wechselwirkungen auf molekularer Ebene erwiesen.
Es ist auch ein bekannter Inhibitor des Insulinabbaus sowohl durch isolierte Zellen als auch durch subzelluläre Organellen, der die Fähigkeit der gereinigten Glutathion-Insulin-Transhydrogenase hemmt, Insulin in seine Bestandteile A- und B-Ketten zu spalten. Bei Konzentrationen von 90 und 300μM hemmt diese Verbindung 50 bzw. 90% der abbauenden Aktivität des gereinigten Enzyms. Ähnlich wird der Abbau durch Rohleberlysate durch 70 bzw. 250 μM dieser Chemikalie um 50 bzw. 90% gehemmt. Es verringert sowohl die Vmax als auch die Affinität des Enzyms für Insulin.
Dieser Wirkstoff ist in der Lage, die reduktive Funktion der Plasmamembran durch die Wirkung gegen Proteindisulfid-Isomerase zu hemmen. Er ist in der Lage, die Spaltung eines disulfidverknüpften Iodotyramin/Poly(D-Lysin)-Konjugats zu inhibieren, das unspezifisch an die Oberfläche von CHO-Zellen bindet. Er hemmt auch die Zytotoxizität von Diphtherietoxin, einem disulfidverknüpften Heterodimer, das an einen spezifischen Oberflächenrezeptor bindet und eine Kettentrennung durchlaufen muss, um seine Zytotoxizität auszuüben.
|
Literatur |
|
|---|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
