nur für Forschungszwecke
Niflumic acid COX Inhibitor
Kat.-Nr.S3018
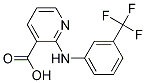
Chemische Struktur
Molekulargewicht: 282.22
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 282.22 | Formel | C13H9F3N2O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 4394-00-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Nifluril | Smiles | C1=CC(=CC(=C1)NC2=C(C=CC=N2)C(=O)O)C(F)(F)F | ||
Löslichkeit
|
In vitro |
DMSO
: 56 mg/mL
(198.42 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
COX-2
GABA receptor
|
|---|---|
| In vitro |
Niflumic acid hemmt Ca2+-aktivierte Cl-Kanäle mit einer Hemmkonstante von 17 mM. Diese Verbindung hemmt auch ICl(Ca), die durch die Badapplikation von Ca2+ auf Oozyten hervorgerufen wird, die mit dem Ca2+-Ionophor A23187 permeabilisiert wurden, was zeigt, dass die Hemmung von ICl(Ca) auf eine direkte Wechselwirkung mit dem Cl-Kanal und nicht auf eine Interferenz mit dem Ca2+-Eintritt durch spannungsabhängige Ca2+-Kanäle zurückzuführen ist. Es blockiert Ca2+-aktivierte, nicht-selektive Kationenkanäle in Inside-out-Patches aus der basolateralen Membran von exokrinen Pankreaszellen der Ratte mit einem IC50-Wert von 50 μM. Diese Chemikalie aktiviert dosisabhängig und reversibel Calcium-aktivierte K+ (KCa)-Kanäle mit großer Leitfähigkeit. Sie bewirkt eine konzentrationsabhängige Hemmung der Amplitude des spontanen transienten Einwärtsstroms (STIC, Calcium-aktivierter Chloridstrom). Diese Verbindung hemmt Noradrenalin- und Koffein-evozierte IO(Ca) mit einer ICM50 von 6,6 μM, d.h. sie ist weniger wirksam gegen evozierte Ströme im Vergleich zu spontanen Strömen. Sie hemmt die Amplitude des spontanen transienten Einwärtsstroms (STIC) spannungsabhängig mit einem IC50 von 2,3 μM und 1,1 μM bei -50 bzw. +50 mV. Sie hemmt nicht nur die IL-13-induzierte Becherzellhyperplasie, sondern auch die bronchiale Hyperreagibilität und die eosinophile Infiltration. Diese Chemikalie unterdrückt die Eotaxinspiegel in bronchoalveolären Spülflüssigkeiten und die Überexpression des MUC5AC-Gens, einem Marker für die Becherzellhyperplasie, in der Lunge nach IL-13-Instillation. Sie unterdrückt die JAK2-Aktivierung, die STAT6-Aktivierung und die Eotaxinexpression in Epithelzellen. |
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
