nur für Forschungszwecke
d4T (Stavudine) Reverse Transcriptase Inhibitor
Kat.-Nr.S1398
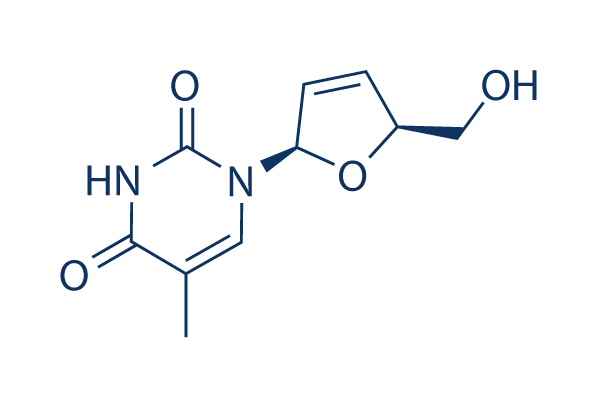
Chemische Struktur
Molekulargewicht: 224.21
Qualitätskontrolle
| Verwandte Ziele | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite HIV HCV Protease |
|---|---|
| Weitere Reverse Transcriptase Inhibitoren | Dapivirine (TMC120) Fangchinoline Salicylanilide 3'-Fluoro-3'-deoxythymidine (Alovudine) Ulonivirine Lersivirine (UK-453061) Bifendate 4-Chloro-2-(trifluoroacetyl)aniline hydrochloride |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 224.21 | Formel | C10H12N2O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 3056-17-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | BMY-27857, Sanilvudine, NSC 163661,d4T | Smiles | CC1=CN(C(=O)NC1=O)C2C=CC(O2)CO | ||
Löslichkeit
|
In vitro |
DMSO
: 49 mg/mL
(218.54 mM)
Ethanol : 24 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Reverse transcriptase
|
|---|---|
| In vitro |
Stavudine (d4T) verändert den Lipidphänotyp, indem es den Lipidgehalt und die Expression von Markern, die am Lipidstoffwechsel beteiligt sind, verringert, nämlich C/EBPalpha, Peroxisom-Proliferator-aktivierter Rezeptor gamma, Adipozyten-Lipid-Bindungsprotein 2, Fettsäure-Synthase und Acetyl-Coenzym A-Carboxylase. Es treibt 5-10% der 3T3-F442A-Zellen in die Apoptose und reduziert den Lipidgehalt und das Überleben von differenzierten 3T3-L1-Adipozyten. Diese Verbindung erhöht die mitochondriale Masse um das Zwei- bis Vierfache und senkt das mitochondriale Membranpotential (JC-1-Färbung). Es hemmt die p24-Antigenproduktion durch HIV-I in PBMC mit ED50-Werten von 0,04 μM bis 0,2 μM. Es verursacht auch eine signifikante mitochondriale Dysfunktion mit einem 1,5-fachen Anstieg der zellulären Laktat-zu-Pyruvat-Verhältnisse. Stavudine (d4T) verursacht eine dosisabhängige Abnahme der mtDNA-Amplifikation und einen korrelativen Anstieg der Abundanz von Markern für mitochondrialen oxidativen Stress. Seine Behandlung erhöht die mitochondrialen reaktiven Sauerstoffspezies (ROS), verstärkt den mitochondrialen oxidativen Stress und trägt mechanistisch zur NRTI-induzierten Toxizität bei.
|
| In vivo |
Stavudine (d4T) (500 mg/kg/Tag) führt zu einem Mangel an signifikanten oxidativen mtDNA-Läsionen (gemessen durch lange Polymerase-Kettenreaktionsexperimente) und normalen Blutlaktat-/Pyruvat-Verhältnissen bei mageren Mäusen. Es kann die hepatische und muskuläre mtDNA bei mageren Mäusen verringern und während des Fastens auch Ketoazidose verursachen, ohne die mtDNA zu verändern. Diese Verbindung erschöpft die WAT-mtDNA nur bei fettleibigen Mäusen.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT01178684 | Completed | HIV |
SEARCH Research Foundation|University of Hawaii |
May 2010 | -- |
| NCT00455585 | Completed | HIV Infections |
Makerere University|Department of Foreign Affairs Ireland |
January 2007 | Phase 4 |
| NCT00235222 | Unknown status | HIV |
Groupe Hospitalier Pitie-Salpetriere|Bristol-Myers Squibb |
June 2004 | Phase 4 |
| NCT00116116 | Completed | HIV Infections|AIDS |
Bristol-Myers Squibb |
March 2002 | Phase 4 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
