nur für Forschungszwecke
A-317491 P2 Receptor Antagonist
Kat.-Nr.S8519
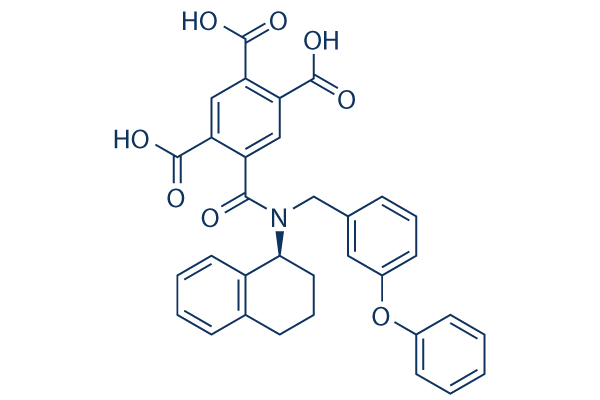
Chemische Struktur
Molekulargewicht: 565.57
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- SDS
- Datenblatt
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) |
|---|---|
| Weitere P2 Receptor Inhibitoren | A-438079 Hydrochloride A-804598 MRS 2578 A-740003 5-BDBD Gefapixant AF-353 Minodronic acid Diquafosol Tetrasodium BX430 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 565.57 | Formel | C33H27NO8 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 475205-49-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1CC(C2=CC=CC=C2C1)N(CC3=CC(=CC=C3)OC4=CC=CC=C4)C(=O)C5=CC(=C(C=C5C(=O)O)C(=O)O)C(=O)O | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(176.81 mM)
Ethanol : 100 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Human P2X2/3
(Cell-free assay) 9 nM(Ki)
Human P2X3
(Cell-free assay) 22 nM(Ki)
Rat P2X3
(Cell-free assay) 22 nM(Ki)
Rat P2X2/3
(Cell-free assay) 92 nM(Ki)
|
|---|---|
| In vitro |
A-317491 blockiert potent rekombinanten menschlichen und Ratten-P2X3- und P2X2/3-Rezeptor-vermittelten Kalziumfluss (Ki = 22-92 nM) und ist hochselektiv (IC50 >10 μM) gegenüber anderen P2-Rezeptoren und anderen Neurotransmitter-Rezeptoren, Ionenkanälen und Enzymen. Diese Verbindung erfährt in In-vitro-Assays unter Verwendung menschlicher und Ratten-Lebermikrosomen keinen nachweisbaren Metabolismus (Oxidation oder Glucuronidierung).
|
| In vivo |
A-317491 reduziert dosisabhängig (ED50 = 30 μmol/kg s.c.) die durch komplettes Freund-Adjuvans induzierte thermische Hyperalgesie bei der Ratte. Diese Verbindung ist am potentesten (ED50 = 10-15 μmol/kg s.c.) bei der Abschwächung sowohl der thermischen Hyperalgesie als auch der mechanischen Allodynie nach chronischer Nervenkompressionsverletzung. Obwohl in chronischen Schmerzmodellen aktiv, ist diese Chemikalie unwirksam (ED50 >100 μmol/kg s.c.) bei der Reduzierung der Nozizeption in Tiermodellen für akute Schmerzen, postoperative Schmerzen und viszerale Schmerzen. Vorläufige pharmakokinetische Studien an Ratten zeigen, dass 10 μmol/kg dieser Verbindung nach s.c.-Verabreichung eine hohe (≈80%) systemische Bioverfügbarkeit aufwiesen (geschätzte Plasmakonzentration = 15 μg/ml, >99% proteingebunden) und eine Plasmahalbwertszeit von 11 h. Es ist wirksam bei der Reduzierung von schmerzassoziiertem Verhalten in mehreren Tiermodellen von entzündlichem und neuropathischem Schmerz, wenn es systemisch verabreicht wird. Diese Verbindung dringt nicht signifikant in das ZNS ein.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
