nur für Forschungszwecke
Anamorelin GHSR Agonist
Kat.-Nr.S4980
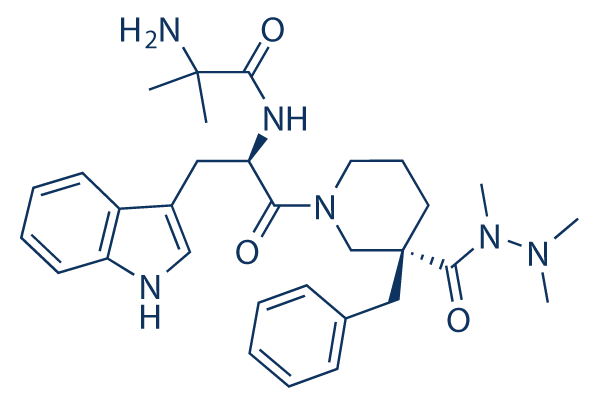
Chemische Struktur
Molekulargewicht: 546.70
Qualitätskontrolle
| Verwandte Ziele | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Weitere GHSR Inhibitoren | AnaMorelin hydrochloride |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 546.70 | Formel | C31H42N6O3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 249921-19-5 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | ONO-7643, RC-1291, ST-1291 | Smiles | CC(C)(C(=O)NC(CC1=CNC2=CC=CC=C21)C(=O)N3CCCC(C3)(CC4=CC=CC=C4)C(=O)N(C)N(C)C)N | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(182.91 mM)
Ethanol : 50 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
ghrelin receptor
(HEK293/GRLN FLIPR assay) 0.74 nM(EC50)
|
|---|---|
| In vitro |
Anamorelin zeigt eine signifikante agonistische und bindende Aktivität am Ghrelin-Rezeptor und stimuliert die Freisetzung von Wachstumshormonen (GH) in vitro. Durch seine Ghrelin- und GH-freisetzende Aktivität besitzt diese Verbindung sowohl orexigene als auch anabole Eigenschaften. Bei der Untersuchung seiner Aktivität zeigt 10 μM dieser Chemikalie eine schwache Bindung an die L-Typ-Kalziumkanalrezeptoren, den Serotonintransporter und den Natriumkanal. Daher weist es eine hohe Selektivität gegenüber Ghrelin-Rezeptoren auf. Durch die Hemmung des nukleären Faktors κB reduziert dieser Wirkstoff die Produktion von proinflammatorischen Zytokinen und stoppt den Muskelabbau (hemmt die Proteolyse).
|
| In vivo |
Bei Ratten erhöht Anamorelin signifikant und dosisabhängig die Nahrungsaufnahme und das Körpergewicht bei allen Dosisstufen im Vergleich zur Kontrolle und erhöhte signifikant die Wachstumshormon (GH)-Spiegel bei Dosen von 10 oder 30 mg/kg. Wachstumshormon- und IGF-1-Spiegel steigen nach Verabreichung dieser Verbindung bei Schweinen an. Es ist oral aktiv und hat eine längere Halbwertszeit (ca. 7 h) als Ghrelin. Es stimuliert neuroendokrine Reaktionen und kann schnelle positive Auswirkungen auf Appetit und Stoffwechsel hervorrufen. Die Plasmaclearance von radiomarkiertem Anamorelin zeigt, dass der größte Teil des Arzneimittels in den Fäkalien (92%) ausgeschieden wird. Nahrung verringert die Fläche unter der Kurve (AUC) dieser Chemikalie um das 4-fache. Der Metabolismus erfolgt durch CYP3A4. In Maus-Tumormodellen, wie Lewis-Lungen- und menschlichem Bronchioalveolarkarzinom, fördert es das Tumorwachstum nicht.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
