nur für Forschungszwecke
Rofecoxib COX Inhibitor
Kat.-Nr.S3043
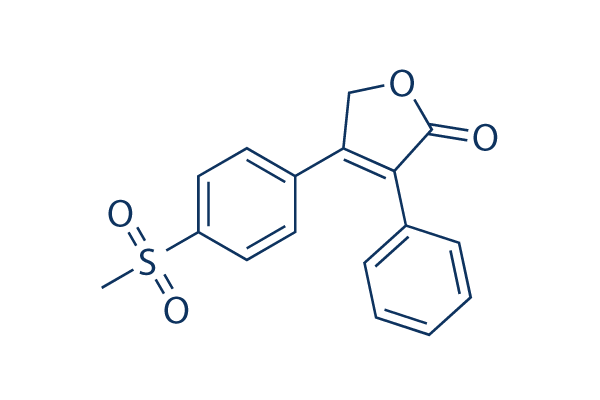
Chemische Struktur
Molekulargewicht: 314.36
Qualitätskontrolle
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| J774 | Function assay | In vitro inhibitory activity against Prostaglandin G/H synthase 2 in murine J774 cells, IC50=0.012 μM | ||||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 314.36 | Formel | C17H14O4S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 162011-90-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | MK-0966 | Smiles | CS(=O)(=O)C1=CC=C(C=C1)C2=C(C(=O)OC2)C3=CC=CC=C3 | ||
Löslichkeit
|
In vitro |
DMSO
: 63 mg/mL
(200.4 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
COX-2
18 nM
|
|---|---|
| In vitro |
Rofecoxib hemmt die COX-2-abhängige Produktion von PGE2 in menschlichen Osteosarkomzellen mit einer IC50 von 26 nM. Diese Verbindung ist ein zeitabhängiger Inhibitor der gereinigten humanen rekombinanten COX-2 mit einer IC50 von 0,34 μM. Es verursacht eine Hemmung der gereinigten humanen COX-1 auf nicht-zeitabhängige Weise. In einem menschlichen Vollbluttest hemmt diese Chemikalie selektiv die Lipopolysaccharid-induzierte, COX-2-abgeleitete PGE2-Synthese mit einem IC50-Wert von 0,53 μM im Vergleich zu einem IC50-Wert von 18,8 μM für die Hemmung der COX-1-abgeleiteten Thromboxan B2-Synthese nach Blutgerinnung. Es hemmt moderat die Phenacetin-O-Deethylierung mit einer IC50 von 23 μM. Eine 30-minütige Präinkubation mit Mikrosomen und NADPH erhöht den hemmenden Effekt dieser Verbindung erheblich mit einer IC50 von 4,2 μM. Die Inaktivierung von CYP1A2 durch Rofecoxib erfordert NADPH und ist durch einen Ki von 4,8 μM gekennzeichnet.
|
| Kinase-Assay |
In vitro biochemische und pharmakologische Assays, Hemmstudien mit rekombinanter humaner COX-1 und COX-2
|
|
Mikrosomale Präparationen von rekombinanter humaner COX-1 und COX-2 werden aus einem Vacciniavirus-COS-7-Zell-Expressionssystem hergestellt. Rekombinante humane COX-1 und COX-2 werden in Baculovirus-Sf9-Zellen exprimiert, und die Enzyme werden gereinigt. Die enzymatische Aktivität wird kontinuierlich entweder durch einen Fluoreszenzassay, der das Auftreten der oxidierten Form des Reduktionsmittel-Cosubstrats Homovanillinsäure misst, oder durch Sauerstoffverbrauch überwacht. Der HPLC-Assay zur Beurteilung der Hemmung der gereinigten COX-1 durch diese Verbindung mit einer Substratkonzentration von 0,1 μM Arachidonsäure, die Bestimmung der Stöchiometrie des Komplexes zwischen COX-2 und dieser Chemikalie, die Dissoziationsratenkonstante des Enzym-Inhibitor-Komplexes durch Wiederherstellung der enzymatischen Aktivität und die Gewinnung der intakten Verbindung aus diesem Komplex werden alle wie zuvor beschrieben durchgeführt. Das Lösungsmittelsystem für die HPLC-Analyse dieser Chemikalie ist 15:85 MeOH/wässriges Kaliumphosphat (1 g/Liter), mit Elution durch einen linearen Gradienten von 15 bis 75 % MeOH über 25 Minuten mit Detektion bei 275 nm an einer Novapak C18-Säule.
|
|
| In vivo |
Rofecoxib hemmt stark Carrageenan-induziertes Pfotenödem, Carrageenan-induzierte Pfotenschmerzhaftigkeit und Lipopolysaccharid-induzierte Pyrese mit einer IC50 von 1,5 mg/kg, 1,0 mg/kg bzw. 0,24 mg/kg. Diese Verbindung blockiert auch Adjuvans-induzierte Arthritis mit einer IC50 von 0,74 mg/kg/Tag. Es hat auch eine schützende Wirkung auf die Adjuvans-induzierte Zerstörung von Knorpel- und Knochenstrukturen bei Ratten. Die orale Verabreichung dieser Chemikalie senkt den Pfortaderdruck bei Ratten, die 8 Wochen lang mit CCl4 behandelt wurden. Darüber hinaus reduziert ihre Verabreichung die Anzahl der aktivierten HSCs und reguliert die hepatischen Proteinspiegel von drei nachgewiesenen Kollagentypen, Laminin, VEGF und CTGF bei CCl4-behandelten Ratten herunter.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT00637988 | Completed | Barrett''s Esophagus |
AstraZeneca |
April 2002 | Phase 4 |
| NCT00038389 | Terminated | Glioma|Brain Neoplasms |
M.D. Anderson Cancer Center |
October 2001 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
